дефицит глюкозо 6 фосфатдегидрогеназы что это такое
Дефицит глюкозо 6 фосфатдегидрогеназы что это такое
Этиология и встречаемость недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД). Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) (MIM №305900), наследственная склонность к гемолизу, — Х-сцепленное заболевание антиоксидантного гомеостаза, вызванное мутациями в гене G6PD. В областях, эндемичных по малярии, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) имеет распространенность от 5-25%; в неэндемичных областях распространенность менее 0,5%.
Подобно серповидноклеточной анемии, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) имеет высокую частоту на некоторых территориях, поскольку вызывает у гетерозиготных носителей повышенную сопротивляемость к малярии, и таким образом дает им селективное преимущество.
Патогенез недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)
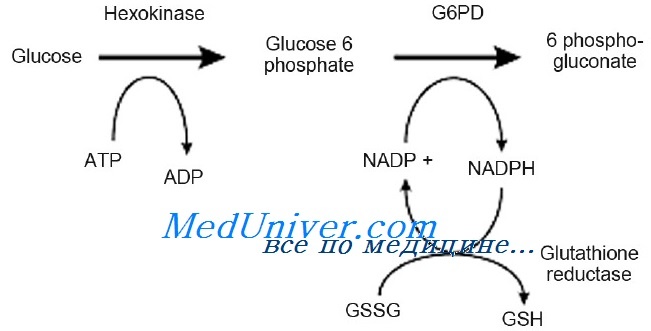
Глюкозо-6-фосфат дегидрогеназы (Г6ФД) — первый фермент в гексозомонофосфатном шунте, метаболическом пути, критически важном для синтеза НАДФ. НАДФ необходим для восстановления окисленного глутатиона. В эритроцитах восстановленный глутатион используется для детоксикации оксидантов, образующихся при взаимодействии гемоглобина и кислорода с внешними факторами, такими как лекарства, инфекции или метаболический ацидоз.
Чаще всего недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) возникает вследствие мутаций в Х-сцепленном гене G6PD, снижающих либо каталитическую активность, либо устойчивость фермента, либо и то и другое. Когда активность глюкозо-6-фосфат дегидрогеназы (Г6ФД) достаточно низкая, дефицит НАДФ приводит к недостаточному восстановлению окисленного глутатиона во времени окислительного стресса. Это вызывает окисление и накопление внутриклеточных белков (телец Хайнца) и образование ригидных эритроцитов, легко подвергающихся гемолизу.
Наиболее частые аллели G6PD, приводящие к неустойчивости белка, вызывают преждевременное старение эритроцитов. Поскольку эритроциты не имеют ядра, новая мРНК глюкозо-6-фосфат дегидрогеназа (Г6ФД) не синтезируется; поэтому эритроциты не в состоянии заменять глюкозо-6-фосфат дегидрогеназу (Г6ФД) по мере его деградации. Следовательно, при действии окислительных агентов гемолиз начинается с более старых эритроцитов и постепенно захватывает все более молодые эритроциты, в зависимости от степени окислительного стресса.
Фенотип и развитие недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)
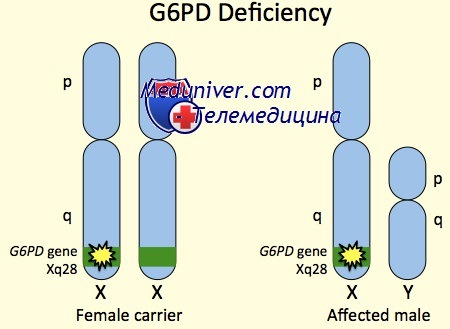
Так как заболевание Х-сцепленное, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) преимущественно и наиболее сильно поражает мужчин. Редкие женщины с клинической симптоматикой имеют смещение инактивации Х-хромосомы, у которых в предшественниках эритроцитов активна Х-хромосома, несущая аллель болезни недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД).
Кроме пола, тяжесть недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) зависит от конкретной мутации гена G6PD. В общих чертах мутации, часто встречающиеся в Средиземноморском бассейне (Г6ФД В или средиземноморские), приводят к более тяжелым формам, чем африканские (Г6ФД А- варианты). В эритроцитах пациентов со средиземноморскими вариантами активность глюкозо-6-фосфат дегидрогеназы (Г6ФД) падает до недостаточного уровня за 5-10 дней после их появления в кровотоке, тогда как в эритроцитах пациентов с глюкозо-6-фосфат дегидрогеназы (Г6ФД) А- вариантами активность ГбФд снижается до недостаточного уровня только через 50-60 дней.
Чаще всего недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) обнаруживается или как неонатальная желтуха, или как острая гемолитическая анемия. Максимальная встречаемость неонаталь-ной желтухи происходит в течение 2-3-го дня жизни. Тяжесть желтухи колеблется от преклинической до ядерной желтухи; связанная анемия редко бывает тяжелой.
Эпизоды острой гемолитической анемии обычно начинаются во время окислительного стресса и заканчиваются после гемолиза эритроцитов с недостаточностью глюкозо-6-фосфат дегидрогеназы (Г6ФД); следовательно, тяжесть анемии, связанной с острыми гемолитическими кризами, прямо пропорциональна степени недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) и выраженности окислительного стресса.
Наиболее частые пусковые механизмы — вирусные и бактериальные инфекции, но также к гемолизу могут приводить множество лекарственных средств и токсинов. Название заболевания — «фавизм» происходит от гемолиза, вызванного употреблением конских бобов Vicia fava пациентами с тяжелыми формами недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД), например, средиземноморскими; бобы содержат b-гликозиды, оксиданты естественного происхождения.
Помимо неонатальной желтухи и острой гемолитической анемии, недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) иногда вызывает врожденную или хроническую несфероцитарную гемолитическую анемию. Пациенты с хронической не-сфероцитарной гемолитической анемией обычно имеют выраженную недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД), вызывающую хроническую анемию и повышенную предрасположенность к инфекциям. Предрасположенность к инфекциям возникает в связи с тем, что поступления НАДФ в гранулоциты недостаточно, чтобы поддерживать окислительную реакцию, необходимую для разрушения фагоцитированных бактерий.
Особенности фенотипических проявлений недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД):
• Возраст начала: неонатальный
• Гемолитическая анемия
• Неонатальная желтуха
Лечение недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)
Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) следует заподозрить у пациентов африканского, средиземноморского или азиатского происхождения, имеющих острый гемолитический эпизод или неонатальную желтуху. Недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) диагностируют измерением активности глюкозо-6-фосфат дегидрогеназы (Г6ФД) в эритроцитах; эта активность должна быть измерена только в том случае, если пациент не имел переливаний крови или острого гемолиза (поскольку недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД) первоначально развивается в более старых эритроцитах, измерение активности глюкозо-6-фосфат дегидрогеназы (Г6ФД) преимущественно в молодых эритроцитах во время или немедленно после гемолитического эпизода, часто дает ложноотрицательный результат).
Ключ к оказанию помощи при недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД) — предотвращение гемолиза быстрым лечением инфекций и исключением лекарств с оксидантным эффектом (например, сульфаниламидов, сульфонов, нитрофуранов) и токсинов (например, нафталина). Хотя большинство пациентов во время гемолитического эпизода не нуждаются в медицинском вмешательстве, в случае выраженной анемии и гемолиза может потребоваться переливание эритроцитарной массы и интенсивное наблюдение. Пациенты с неонатальной желтухой хорошо отвечают на такую же терапию, как и при неонатальной желтухе другого генеза (регидратацию, светотерапию и обменные переливания крови).
Риски наследования недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД)
Все мальчики у матери, несущей мутацию в гене G6PD, имеют 50% шансы быть больными, а все дочери — 50% шансов оказаться носительницами. Все дочери больного отца будут носительницами, но сыновья будут здоровы, поскольку больной отец не передает X хромосому сыновьям. Риск того, что девочки-носительницы будут иметь клинически значимые симптомы, низкий, так как достаточное смещение инактивации Х-хромосомы встречается сравнительно редко.
Пример недостаточности глюкозо-6-фосфат дегидрогеназы (Г6ФД). Л.М., ранее здоровый 5-летний мальчик, поступил в неотложное отделение с лихорадкой, бледностью, тахикардией, одышкой, заторможенностью; в остальном результаты его клинического осмотра оказались без особенностей. Утром перед поступлением он был здоров, но в течение дня появились боли в животе, головная боль, поднялась температура тела; вечером начались одышка и заторможенность. Он не принимал никаких лекAPCтвенных средств или известных токсинов, результаты токсикологического анализа мочи оказались отрицательными. Результаты других лабораторных тестов показали огромный внутрисосудистый гемолиз и гемоглобинурию.
После реанимации ребенок переведен в отделение; гемолиз разрешился без дальнейшего вмешательства. Пациент по этнической принадлежности — грек; его родители были не осведомлены о случаях гемолиза в семье, хотя мать имела несколько дальних родственников в Европе с «проблемами крови». Дальнейший опрос выяснил, что утром перед заболеванием ребенок поел конские бобы в саду, пока мать работала во дворе.
Врач объяснил родителям, что ребенок, вероятно, имеет недостаточность глюкозо-6-фосфат дегидрогеназы (Г6ФД), из-за чего и заболел после употребления конских бобов. Последующее измерение активности глюкозо-6-фосфат дегидрогеназы (Г6ФД) в эритроцитах подтвердило недостаточность фермента. Родителям даны рекомендации относительно риска острого гемолиза у ребенка после применения определенных лекарств и токсинов, дан список веществ, которых необходимо избегать.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Дефицит глюкозо-6-фосфатдегидрогеназы. Причины. Симптомы. Диагностика. Лечение
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Дефицит глюкозо-6-фосфатдегидрогеназы неравномерно распределен среди населения разных стран: чаще всего встречается у жителей европейских государств, расположенных на побережье Средиземного моря (Италия, Греция), у евреев-сефардов, а также в Африке и Латинской Америке. Недостаток глюкозо-6-фосфатдегидрогеназы широко регистрируется в бывших малярийных районах Средней Азии и Закавказья, особенно в Азербайджане. Известно, что больные тропической малярией, имеющие дефицит глюкозо-6-фосфатдегидрогеназы, реже погибали, поскольку эритроциты с недостаточностью фермента содержали меньше малярийных плазмодиев, чем нормальные эритроциты. Среди русского населения дефицит активности глюкозо-6-фосфатдегидрогеназы встречается приблизительно у 2 % людей.
Частота разных типов недостаточности глюкозо-6-фосфатдегидрогеназы колеблется в различных странах. Поэтому частота лиц, «отвечающих» гемолизом на действие провоцирующих факторов, варьирует от 0 до 15 %, а в некоторых местностях достигает 30 %.
Недостаточность глюкозо-6-фосфатдегидрогеназы наследуется рецессивно, сцеплена с Х-хромосомой. Женщины могут быть как гомозиготными (активность фермента в эритроцитах отсутствует), так и гетерозиготными (активность фермента составляет 50 %) носителями дефекта. У мужчин активность фермента обычно ниже 10 /о, что обусловливает выраженные клинические проявления болезни.
Заболевание может обнаруживаться у ребенка любого возраста. Выявляют пять клинических форм проявления недостаточности глюкозо-6-фосфатдегидрогеназы в эритроцитах.
Ассоциируется с вариантами глюкозо-6-фосфатдегидрогеназы В (средиземноморский) и Canton.
Наиболее часто встречается у новорожденных итальянцев, греков, евреев, китайцев, таджиков, узбеков. Возможными провоцирующими факторами заболевания являются прием матерью и ребенком витамина К; использование при обработке пупочной ранки антисептиков или красителей; использование пеленок, обработанных нафталином.
У новорожденных с дефицитом глюкозо-6-фосфатдегидрогеназы в эритроцитах наблюдается гипербилирубинемия с признаками гемолитической анемии, но доказательства серологического конфликта между матерью и ребенком обычно отсутствуют. Выраженность гииербилирубинемии может быть различной, возможно развитие билирубиновой энцефалопатии.
Наблюдается у детей более старшего возраста PI взрослых; усиление гемолиза отмечается под влиянием интеркуррентных инфекций и после приема лекарств. Клинически отмечается постоянная умеренная бледность кожи, легкая иктеричность, незначительная спленомегалия.
Возникает у внешне здоровых детей после приема лекарств, реже в связи с вакцинацией, вирусной инфекцией, диабетическим ацидозом.
В настоящее время установлено 59 потенциальных гемолитиков при дефиците глюкозо-6-фосфатдегидрогеназы. К группе лекарственных средств, обязательно вызывающих гемолиз, относятся: противомалярийные препараты, сульфаниламидные препараты, нитрофураны.
Острый внутрисосудистый гемолиз развивается, как правило, через 48-96 ч после приема больным лекарственного препарата, обладающего окислительными свойствами.
Лекарственные препараты, вызывающие гемолиз у лиц с недостаточностью активности глюкозо-6-фосфатдегидрогеназы в эритроцитах

 [1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11]
[1], [2], [3], [4], [5], [6], [7], [8], [9], [10], [11]