декремент тест что это такое
Как распознать миастению? Все о диагностике и лечении
Миастения – это болезнь, которая характеризуется нарушением нервно-мышечной передачи (то есть нарушением процесса сокращения мышцы, возникающим в ответ на импульс, идущий по нервному волокну). Причиной миастении зачастую является аутоиммунный процесс, в результате которого в организме вырабатываются антитела к структурам нервно-мышечного синапса. Согласно статистике, миастения встречается у каждого 5-го из 100 тысяч человек. Это хроническое заболевание с острым или постепенным началом. Основным проявлением является преходящая мышечная слабость, так же может возникать птоз (опущение) верхних век, нарушение глотания, «гнусавость» голоса. В тяжелых случаях и при прогрессировании заболевания может возникнуть слабость дыхательных мышц, вплоть до остановки дыхания.
Опасный недуг быстро прогрессирует, клинические проявления могут утихать и вновь обостряться. Диагностируют патологическую мышечную утомляемость чаще у женщин, чем у мужчин, много реже у детей. Средний возраст пациентов от 15 до 45 лет, таким образом, максимальное количество случаев регистрируется у самой активной части населения.
О причинах
В настоящее время причины развития миастении изучены не до конца. Иногда нельзя однозначно сказать, почему у того или иного пациента возникло заболевание. Принято считать, что весомую роль играют следующие факторы:
При появлении злокачественных новообразований в яичниках, в органах дыхания или в молочных железах говорят о миастеническом синдроме Ламберта-Итона. Мышечная слабость, иногда принимаемая за миастению, возникает при болезни Шарко-Мари, при дерматомиозите (разрушении соединительной ткани), различных формах миопатий, синдроме БАС (боковой амиотрофический склероз) и многих других патологиях.
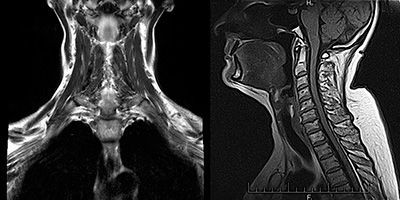
Сложность диагностики состоит в том, что у пациентов с миастенией в начале заболевания может не быть каких-либо четких жалоб и симптоматики. При нейровизуализации (КТ или МРТ) нет значимых отклонений в структурах центральной нервной системы. Только у 30% заболевших тимус увеличивается, либо в нем выявляются новообразования. Мышцы при осмотре так же никак не изменены, патология может выявляться только при микроскопическом исследовании.
Классификация
Врожденная миастения может быть обусловлена генетическими мутациями. Так же плод может получить антитела к рецепторам постсинаптической мембраны от матери, в этом случае речь идет о неонатальной миастении.
Приобретенная миастения может развиться у пациентов любого возраста. Данный диагноз ставят подросткам, молодым людям и пенсионерам. Наиболее часто недуг встречается в активном возрасте, от 20 до 30 лет. Причины могут быть внешними (инфекционные агенты) и внутренними (хронические заболевания, наследственность).
Условно, по распространенности мышечной слабости, миастения подразделяется на следующие виды:
Данное деление относительно, так как при углубленном исследовании чаще всего выявляется поражение всех мышц, но клинические проявления миастении могут возникать только в отдельных группах мышц определенной локализации.
По характеру течения различают:
Симптомы
Клинические проявления миастении зависят от формы заболевания.
Симптомы, характерные для генерализованной формы:
Симптомы, характерные для глазной формы:
Сложность диагностики миастении связана с тем, что вышеперечисленные симптомы могут появляться и пропадать. Наиболее выражено они проявляются, когда человек занимается спортом, длительно читает или работает за компьютером. То есть в те моменты, когда поперечнополосатые мышцы задействованы больше всего. Ведь даже поддержание определенной позы или чтение требуют постоянного напряжения определенных групп мышц.
При отсутствии адекватного лечения существует риск не только инвалидизации, но и смерти. В то время, когда уровень развития медицины не позволял проводить длительную искусственную вентиляцию легких, от миастении умирали 8 из 10 заболевших. При обнаружении тревожных симптомов миастении, необходимо записаться на прием к неврологу. При необходимости специалист направит на обследование и подберет эффективную терапию.
Диагностика
Врач-невролог ставит диагноз миастения на основе жалоб, данных анамнеза, осмотра и исследований. Специалист сравнивает жалобы пациента с симптомами, характерными для этой болезни. Для подтверждения диагноза проводят диагностические исследования.
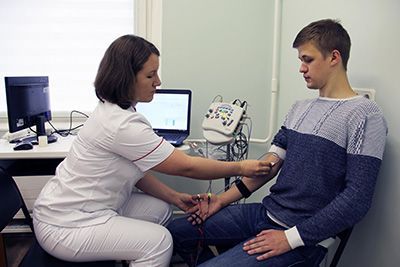
Электронейромиография при миастении является «золотым стандартом» и обязательным исследованием. Используется специальный режим ЭНМГ – «декремент-тест». При проведении обследования с помощью электрической стимуляции исследуемую мышцу заставляют сокращаться с высокой частотой. В результате при миастении или миастеническом синдроме регистрируется уменьшение интенсивности мышечного сокращения.
Прозериновая проба. Выполняется самостоятельно или после проведения декремент-теста. Прозерин — вещество, улучшающее нервно-мышечную передачу. Подкожно вводится небольшое его количество, через 30 минут после этого пациент вновь осматривается врачом или проводится повторная ЭНМГ. Проба считается положительной, если отмечается клиническое улучшение или позитивная динамика при выполнении декремент-теста.
Лабораторная диагностика. Анализ крови на содержание специфических антител к рецепторам, мышцам. Антитела выявляются далеко не во всех случаях миастении.
Как правило, этих методов в сочетании с консультацией невролога бывает достаточно для установления диагноза.
Во время осмотра врач может провести пробы на повышенную мышечную утомляемость. Сначала на определенную группу мышц дается нагрузка, затем оценивается их состояние. При глазной форме миастении нагружают глазодвигательные мышцы, для этого больного просят в течение 30 секунд смотреть в одну точку. При жалобах на патологическую усталость мышц шеи, пациента укладывают на спину и просят держать голову поднятой в течение 1 минуты. При слабости в ногах, больному нужно сделать несколько приседаний либо походить на носочках. Для определения степени утомляемости мышц кисти и предплечья, человека просят несколько раз интенсивно согнуть и разогнуть кисть.
Исследование нервной системы с помощью функциональной диагностики. Часть 2. Электронейромиография и электромиография
Структура статьи
В предыдущей части статьи я немного рассказал о таком методе функциональной диагностики нервной системы, как регистрация вызванных потенциалов головного мозга. Данный метод позволяет изучить различные отделы центральной нервной системы.
Что такое «периферическая нервная система»?
Но ведь представить себе функционирование нашего организма без периферической нервной системы тоже невозможно. Для ее обследования используется электронейромиография.
Периферические нервы берут свое начало в спинном мозге и нервных узлах, расположенных рядом с ним в виде «корешков». По своим функциям периферические нервы делятся на моторные (отвечающие за работу мышц), сенсорные (обеспечивающие чувствительность) и вегетативные (в компетенции которых работа внутренних органов).
Нервные корешки, выходя из спинного мозга, распадаются на парные сплетения (шейные, плечевые, поясничные и крестцовые), которые, в свою очередь, распадаются на сами периферические нервы. Сенсорные нервы получают информацию от рецепторов (для каждого «типа» ощущений – боли, температуры, прикосновения, давления и т.д. – существуют свои виды рецепторов), моторные нейроны связаны с мышечными волокнами посредством нервно-мышечных синапсов. С помощью специальных синапсов контактируют с клетками внутренних органов и вегетативные нервы.
Очень упрощенно, типичный периферический нерв можно представить в виде электрического кабеля, состоящего из множества мелких проводов, объединенных одной оболочкой. «Электричество», то есть нервный импульс, в нерве передается по оболочке, а не по внутренней части «проводов». «Провод» называется аксоном и является отростком самой нервной клетки (нейрона), расположенной в спинном мозге (длина аксона, иннервирующего мышцу стопы может достигать метра и более). «Оболочка» провода – вещество миелин, обеспечивающее передачу нервного импульса по аксону.
Я намеренно так остановился на описании строения периферической нервной системы, чтобы ЭНМГ (электронейромиография) не казалась Вам в дальнейшем каким-то странным, загадочным, «шаманским» методом. Итак, в нашем организме есть хитросплетение кабелей, проводящих ток, кабели состоят из проводов, имеющих оболочку. Поломка этой системы возможна на любом уровне (от клетки в спинном мозге до нервно-мышечного синапса) и может возникнуть как за счет повреждения самого провода, так и его оболочки. Цель ЭНМГ – найти место повреждения и определить его характер.
Конечно, электронейромиография не является волшебным и универсальным диагностическим методом (как не является им ни одна из других, более известных в широких кругах методик, например МРТ ). Не все нервы и мышцы доступны изучению, не на всех участках их можно проверить. Но при грамотном подходе со стороны врача, назначающего или проводящего ЭНМГ, данный метод может дать много полезной информации.
Так что же представляет из себя стимуляционная ЭНМГ?
Стандартный метод исследования моторных и сенсорных волокон периферических нервов внешне выглядит несложно. Над поверхностью мышцы или на участок кожи, иннервируемой изучаемым нервом, накладываются электроды (чаще всего они похожи на маленький пластырь или наклейку), электроды подключаются к аппаратуре (электронейромиографу). На участках, где нерв находится не очень глубоко, с помощью специального стимулятора (отдаленно напоминающего штекер любого электроприбора) нерв раздражается разрядами электрического тока. Ток слабый и абсолютно безопасен, хотя ощущения могут быть и неприятными. В результате электрического раздражения происходит сокращение мышцы или возникает ответ в кожных покровах (в случае исследования сенсорных волокон). Этот ответ или сокращение мышцы и регистрируется наклейками-электродами. Полученные данные и анализируются врачом.
Декремент-тест
Исследование и анализ состояния большинства крупных нервов конечностей обычно не вызывает сложностей. Оценка состояния сплетений и нервных корешков более сложна, ведь, как рассказывалось выше, они образуются из множества периферических нервов, и возникает необходимость исследовать почти каждый из них.
Для диагностики заболеваний нервно-мышечного синапса используется метод ритмической стимуляции или «декремент-тест». При выполнении декремент-теста нерв стимулируется несколько раз (обычно пять) с высокой частотой стимулов (около 1 в секунду), мышца вынуждена сократиться пять раз подряд за пять секунд. Если синапс функционирует нормально, то все пять раз импульс от нерва вызывает сокращение мышцы с одинаковой силой. Если синапс поврежден – мышца с каждым разом сокращается слабее. Разумеется – это очень упрощенное разъяснение сути ритмической стимуляции (декремент-теста).
Игольчатая ЭНМГ
Для исследования мышц, а это бывает необходимо при подозрении на патологию двигательного нейрона спинного мозга, при заболеваниях мышц, определении степени поражения мышцы при неврологической патологии, используется игольчатая электромиография. Тонкая игла-электрод вводится в исследуемую мышцу (напоминает внутримышечный укол). Регистрируют электрическую активность мышцы в покое и при умеренном напряжении. Игольчатая ЭНМГ – более сложный с точки зрения интерпретации метод и часто занимает больше времени, требует от врача большей квалификации.
Возможности электронейромиографии
Итак, при правильном использовании электронейромиография позволяет:
Показания для исследования
Почему же ЭНМГ редко назначается врачами? Может быть, мало показаний для назначения исследования?
Ниже приведен список симптомов, синдромов, состояний и заболеваний, при которых может быть назначена электронейромиография.
Вот неполный список заболеваний, при которых может быть целесообразно провести электронейромиографию:
Как видно, список не маленький, а главное включает в себя не только чисто неврологические заболевания. Заболевания внутренних органов не редко дают осложнения в виде поражения нервной системы. К примеру, атрофический гастрит может привести к дефициту витамина группы В, тем самым спровоцировать возникновение полинейропатии или поражения спинного мозга. Ну а самый известный пример – это поражение нервов ног при сахарном диабете (диабетическая полинейропатия).
Представляется, что основной причиной малого использования ЭНМГ и ЭМГ является затруднение при интерпретации результатов врачами. Дело в том, что максимальное количество информации можно получить только тогда, когда врач, проводящий ЭНМГ, хорошо разбирается в неврологических заболеваниях и симптомах, а лечащий врач знает о всех нюансах и особенностях электромиографии. В противном случае врач-диагност может провести исследование не в полном объеме, а лечащий доктор может неверно интерпретировать результат, что приведет к постановке ошибочного диагноза.
Таким образом, диагност в любом случае должен быть еще и неврологом, в идеале обследование должен выполнять сам лечащий врач-невролог или ЭНМГ должно проводиться в том учреждении, где лечится обследуемый (в таком случае имеется обратная связь между врачом и диагностом).
Как правильно – ЭНМГ или ЭМГ?
И в завершении немного о путанице в терминологии. Часто встречаются два названия исследования: «электронейромиография» (т.е. ЭНМГ) и «электромиография» (ЭМГ). Как говорилось выше, есть стимуляционная электромиография и игольчатая. Именно игольчатую иногда называют «ЭМГ» или «электромиография», а стимуляционную – «электронейромиография» или «ЭНМГ». В конечном итоге, как таковой разницы нет, потому что именно сочетание стимуляционного и игольчатого методов позволяет всесторонне изучить патологический процесс. К тому же, если доктор направляет Вас на обследование, то правильнее было бы с его стороны либо указать, какие именно нервы и мышцы он хочет исследовать и с какой целью, либо (в том случае если врач, проводящий ЭНМГ – невролог) оставить определение необходимого объема обследования на усмотрение диагноста.
В двух частях этой статьи мы коротко ознакомились с функциональной диагностикой центральной и периферической нервной системы. Точнее, всего с двумя методами – вызванными потенциалами и электронейромиографией. Но, конечно, таких методов много больше – это и известная многим электроэнцефалография (ЭЭГ), и различные виды длительного мониторирования ЭЭГ, полисомнография, кардиореспираторный скрининг и многие другие. О них мы поговорим в другой раз.
Диагностическая и прогностическая значимость исследования надежности нервно-мышечной передачи при миастении
В статье анализируются результаты исследования нервно-мышечной передачи (декремент-теста) у больных миастенией. Обсуждаются проблемы, возникающие при проведении данного исследования. Проводится оценка информативности метода в зависимости от полноты обследования, выбора исследуемой мышцы. Выявлена взаимосвязь показателей декремент-теста, проведенного в начальном периоде заболевания, с рядом особенностей течения миастении в дальнейшем.
Diagnostic and prognostic value for reliability studies of neuromuscular transmission in myasthenia
The analysis of data of the repetitive nerve stimulation (decrement-test) in patients with myasthenia is carried out. The problems arising at carrying out of this research are discussed. Diagnostic value of the method depending on completeness of inspection, a choice of an investigated muscle is spent. The interrelation of parameters the decrement-test with a number of features of current of myasthenia in the further is revealed.
Электромиографическое исследование нервно-мышечной передачи (декремент-тест) проводится всем пациентам с подозрением на миастению [1, 2, 3, 4, 5]. Использование электрической стимуляции мышц для диагностики миастении восходит своими истоками к работам F. Jolly [6]. Однако широкое клиническое применение метода стало возможным только во второй половине ХХ века на фоне появления высокоточной регистрирующей аппаратуры и разработки морфо-функциональной концепции организации нервно-мышечной системы. Применяется непрямая ритмичная стимуляция наиболее пораженной мышцы супрамаксимальными импульсами. Оценивают амплитуду и площадь полученных мышечных ответов. Начальная амплитуда мышечного ответа (М-ответ) может быть нормальной, но при повторной стимуляции наблюдается падение амплитуды и площади М-ответов более чем на 10% (декремент) [1, 4, 7]. Используют стимуляцию редкими (3 Гц) и частыми (50 Гц) импульсами. Высокочастотная стимуляция называется «тетанической». Оцениваются посттетанические феномены в виде уменьшения степени декремента – посттетаническое облегчение (ПТО) и увеличения декременты — посттетаническое истощение (ПТИ). При выявлении декремента, превышающего 10%, исследование повторяют через 30-40 мин. после введения 1,5-2 мл 0,05% прозерина внутримышечно.
Для углубленной оценки состояния периферического двигательного нейрона при миастении используют исследование потенциалов действия двигательных единиц (ПД ДЕ) и миографию одиночного мышечного волокна (джиттер-феномен) [8, 9, 10]. Чувствительность метода исследования единичного мышечного волокна достигает 90%, а суммарная чувствительность комбинации из трех методов (декремент-теста, исследования единичного мышечного волокна и исследования антител к ацетилхолиновым рецепторам) составляет 99% [11].
Целью настоящей работы явилась оценка диагностической и прогностической значимости исследования надежности нервно-мышечной передачи путем анализа всех протоколов исследований, проведенных пациентам, включенным в регистр больных миастенией Самарской области.
Материалы и методы
В Самарской области на базе областной клинической больницы им. М.И. Калинина с 1999 года работает региональный миастенический центр. К 2009 году был создан регистр больных миастенией Самарской области. На 1 января 2011 года регистр содержал информацию о 373 пациентах. Женщины составили 70,5%, мужчины – 29,5% от общего количества больных. Средний возраст пациентов – 51,3+17,4 года (от 13 от до 85 лет).
Исследование состояния нервно-мышечной передачи (декремент-тест) проводилось на электромиографах «Medelec sapphire 4ME» (Англия), «Нейроэкспедитор» фирмы МБН (Россия) и «Viking» фирмы «Nikolet» (США).
На лице исследовалась круговая мышца глаза и/или назальная мышца, на руке –дельтовидная мышца и/или короткий сгибатель пальцев кисти. Диагностический комплекс исследования состояния нервно-мышечной передачи включал несколько этапов:
1. Исследование амплитуды негативной фазы М-ответа в ответ на одиночный супрамаксимальный стимул.
2. Исследование величины амплитуды пятого М-ответа по отношению к первому в процентах (декремент/инкремент) при стимуляции мышцы частотой 3 имп/с.
3. Исследование величины декремента (или инкремента) амплитуды М-ответа при стимуляции мышцы частотой 50 имп/с в процентах по отношению 150-го М-ответа к 1-му («тетаническая стимуляция»).
4. Исследование изменения амплитуды М-ответа степени декремента при стимуляции частотой 3 имп/с сразу после окончания «тетанической серии» или после максимального произвольного усилия (в течение 10 с) по отношению к исходным данным (посттетаническое или постактивационное облегчение — ПТО, ПАО).
5. Исследование изменения амплитуды М-ответа и степени декремента при стимуляции частотой 3 имп/с через 2-3 минуты после окончания «тетанической» серии или максимального произвольного усилия по отношению к исходным данным (посттетаническое или постактивационное истощение — ПТИ, ПАИ).
При выявлении декремента, превышающего 10%, проба на наличие нервно-мышечного утомления считалась положительной. В таком случае проводилось введение 1,5-2 мл 0,05% прозерина внутримышечно, и через 30-45 минут исследование повторялось в том же порядке.
Статистическая обработка результатов исследований проводилась в операционной системе Windows XP с использованием программы MS Excel, пакета прикладных программ Statistica 6.0. Средние значения показателей представлены co стандартными ошибками (Мср. + m). Достоверность различий средних значений показателей оценивалась с использованием t-критерия Стьюдента для 5% и 1% критерия значимости (p + 10,8*
Лечение миастении в Юсуповской больнице
Миастения – аутоиммунное заболевание, которое проявляется слабостью мышц. Болезнь развивается вследствие нарушения передачи импульса между нейронами и мышечными волокнами. Патологический процесс развивается одновременно с гиперплазией вилочковой железы. Чаще заболевание диагностируют у женщин после двадцати лет, но в отдельных случаях оно встречается у детей, юношей и лиц престарелого возраста.
Неврологи Юсуповской больницы проводят диагностику миастении с помощью современных методов инструментальной диагностики. Для лечения используют новейшие лекарственные препараты и немедикаментозные методы терапии. Специалисты клиники физической реабилитации индивидуально составляют комплекс гимнастических упражнений, способствующих увеличению силы мышц.
Причины
Учёные выделяют две основные причины миастении: врождённую генную патологию и воздействие провоцирующих факторов. Врождённая форма заболевания связана с мутацией в геноме пациента, в результате которой по синапсам (специальным переходникам, которые доставляют импульс по назначению) прекращается передача информации.
Мнение эксперта
Автор: Ольга Владимировна Бойко
Врач-невролог, доктор медицинских наук
По последним данным, на долю миастении приходится 0,5-5% случаев на 100 тысяч населения. Миастения в 2-3 раза чаще поражает женщин. В большинстве случаев заболевание дебютирует в возрасте до 40 лет. Пациенты с миастенией становятся инвалидами 1 или 2 группы в 30% случаев. В России на долю болезни приходится 2,5% случаев. Точные причины развития миастении до сих пор неизвестны. Врачи выделяют предрасполагающие факторы, наличие которых повышает риск развития заболевания.
Диагностика миастении может затягиваться в связи с разнообразием клинических проявлений. В Юсуповской больнице для обследования пациентов используется новейшее оборудование: КТ, МРТ, ЭЭГ. Для уточнения диагноза проводится серологическое исследование крови в условиях современной лаборатории. Благодаря комплексному подходу опытные врачи выявляют миастению на любых этапах развития. Каждому пациенту разрабатывается индивидуальный план лечения. Такой подход позволяет добиться положительных результатов за минимальное количество времени.
Также в Юсуповской больнице доступно купирование миастенического криза в условиях реанимации и интенсивной терапии. Используемые препараты отвечают стандартам безопасности и качества.
Признаки заболевания у взрослых
Клинические признаки миастении могут проявляться эпизодически. В остальное время пациент находится в состоянии ремиссии (симптомы заболевания не выражены). Это характерно для глазной формы миастении.
Записаться на приём к неврологу Юсуповской больницы следует при наличии следующей неврологической симптоматики:
Быстрой утомляемости при пережёвывании пищи, ходьбе, работе за компьютером или чтении;
Нарушением мимики лица, речи, голоса;
Расстройства двигательной функции.
В дебюте заболевания клиническая картина настолько не выражена, что человек не обращает особого внимания на имеющиеся отклонения. Из-за постоянной занятости и сильной загруженности дома, на работе больные обращаются к врачу, когда проявления болезни становятся заметными.
Неврологи выделяют 3 группы симптомов миастении у взрослых:
К глазным проявлениям болезни относится птоз (опущение века), диплопия (двоение в глазах), отклонение в сторону глазных яблок при их движении. При увеличении нагрузки нервная симптоматика усугубляется, пациент ощущает головную боль, болезненность в глазах.
Мышечные признаки миастении проявляются слабостью в различных группах мышц:
Гипомимией – слабостью мимической мускулатуры, когда у пациента возникают проблемы с надуванием щёк, улыбкой, зажмуриванием;
Бульбарным синдромом – нарушением глотания, которое приводит к тому, что пациент закашливается во время приёма пищи, давится, гнусавит во время разговора, а его речь становится малопонятной;
Жевательной слабостью – у пациента возникают трудности с пережёвыванием пищи, он быстро устаёт, а нарушение процесса питания усугубляется при отвисании нижней челюсти;
Слабостью в шее и туловище – больному всё тяжелее становится удерживать голову, которая запрокидывается или свисает;
Слабостью в конечностях – в связи с тем, что преимущественно страдают разгибательные мышцы, у пациента возникает бессилие после сильных нагрузок.
Дыхательные нарушения проявляются ослаблением мышц диафрагмы, гортанной и межреберной мускулатуры. В этом случае возникает необходимость в подключении больного к аппарату искусственной вентиляции лёгких. Пациентов госпитализируют в отделение реанимации и интенсивной терапии круглосуточно независимо от дня недели.
Формы болезни
Неврологи выделяют следующие формы миастении у взрослых:
Глазная форма миастении проявляется поражением мышечных волокон, отвечающих за движения глазного яблока, поднятие и удерживание верхнего века. Эти функции нарушаются при возрастании физической нагрузки, стрессовой ситуации, после приёма антихолинэстеразных средств.
Для бульбарной формы миастении характерно нарушение процесса пережевывания пищи, глотания, речи. Голос пациента становится охриплым, гнусавым. Поскольку мимика выражена минимально, создаётся впечатление, что человек внешне выглядит значительно моложе своих лет. Его улыбка напоминает оскал.
При генерализованной форме миастении поражаются все мышцы. Они вовлекаются в патологический процесс постепенно. Сначала нарушаются движения глазными яблоками, затем функция мимических и шейных мышц. Спустя некоторое время в патологический процесс вовлекается мускулатура опорно-двигательного аппарата.
Миастенический криз может развиться независимо от формы заболевания и степени тяжести двигательных нарушений. У пациента внезапно возникает двоение в глазах, резкая слабость и нарушение активности гортани. Ему становится трудно говорить, дышать, глотать. Пульс учащается. Усиливается слюноотделение. В тяжёлых случаях расширяются зрачки, учащается сердцебиение, наступает паралич с сохранением чувствительности.
Редкая разновидность миастении – синдром Ламберта-Итона. Заболевание характеризуется нарушением нервно-мышечной передачи. Это приводит к утомляемости, миалгии (боли в мышцах), параличу глазодвигательной мышцы, вегетативным расстройствам. Этот синдром развивается у больных мелкоклеточным раком лёгких, другими злокачественными опухолями. У пациентов часто возникает затруднение при подъеме из сидячего или лежачего положения.
Миастения Гравис, или псевдопаралитическая миастения, развивается на фоне нарушения функции эндокринной системы и аутоиммунных заболеваний – волчанки, ревматоидного артрита. Она бывает следующих видов: врождённая, новорождённых, юношеская, генерализованная миастения взрослых.
Детская миастения
Симптомы миастении у детей отличаются от признаков заболевания у взрослых. Врождённую миастению определяют уже на этапе внутриутробного развития плода: он почти или совсем неактивен. После рождения вследствие того, что ребёнок не может дышать, он погибает. Миастения новорожденных проявляется следующими признаками:
Ранняя детская миастения диагностируется у детей в возрасте до двух лет. Симптомы заболевания схожи с проявлениями миастении у взрослых:
При вовлечении в патологический процесс дыхательных мышц ребёнок становится пассивным. Если поражаются жевательные мышцы, он может полностью отказаться от еды.
Детская и юношеская миастения поражает детей в возрасте от двух до десяти лет. Заболевание чаще выявляют у девочек. Симптомы схожи с ранним детским типом болезни. Отличие заключается в диагностике: ребёнка старшего возраста проще расспросить о симптомах, что позволяет скорее начать терапию.
Методы диагностики
Чтобы установить точный диагноз и выяснить причины возникновения нарушений нервных функции, неврологи Юсуповской больницы проводят комплексное обследование пациента. Оно включает:
Общий и неврологический осмотр;
Пальпацию, перкуссию и аускультацию;
Врачи клиники неврологии назначают следующие лабораторные и инструментальные исследования:
Клинический и биохимический анализ крови;
Электромиографию, с помощью которой проводят оценку состояния мышц;
Генетический скрининг, позволяющий установить наличие мутационного гена в цепочке ДНК;
Электронейрографию, с помощью которой проверяют скорость передачи импульсов;
Магнитно-резонансную томографию, предоставляющую данные о наличии гиперплазии вилочковой железы, опухолевидных новообразований.
Также проводят тест на скорость утомляемости. Врач предлагает пациенту быстро выполнить жевательные движения челюстью, махать конечностями, сжимать и разжимать кисти на руках, быстро приседать. При выполнении протеиновой пробы пациенту под кожу вводят специальное вещество. В течение получаса человек ощущает значительный физический подъем. У него проходит усталость. Это состояние длится недолго. После действия препарата симптомы миастении возвращаются.
Декремент-тест представляет собой метод исследования процесса передачи нервно-мышечного импульса. Он направлен на изучение пяти групп мышц. На каждую из них воздействуют искусственным провокатором, вызывающим ритмическое сокращение мышечных волокон. При любой форме миастении частота ответов будет низкой.
Для проведения серологического теста пациент за 4 часа до приёма пищи сдаёт кровь для получения сыворотки. Лаборанты проводят иммуноферментный анализ. С помощью этого теста у 90% больных миастенией обнаруживают антитела к ацетилхолиновому рецептору.
К фармакологическим критериям диагностики относится прозериновая проба. Врачи для её проведения используют прозерин или калимин-форте. У 15% больных миастенией при проведении процедуры полностью компенсируются двигательные расстройства.
Комплексная терапия
Неврологи Юсуповской больницы проводят терапию миастении новейшими лекарственными препаратами, которые оказывают эффективное действие и обладают минимальным спектром побочных эффектов. Все медикаменты зарегистрированы в РФ. Благодаря сотрудничеству врачей Юсуповской больницы с научно-исследовательскими институтами пациенты клиники неврологии имеют уникальную возможность получать новейшие препараты, которые проходят последний этап клинического исследования.
Неврологи для лечения миастении применяют следующие фармакологические препараты:
В большинстве случаев врачи клики неврологии избирают трёхступенчатую тактику лечения миастении. Она включает компенсацию нервно-мышечной передачи, коррекцию аутоиммунных нарушений, воздействие на вилочковую железу. Компенсацию нервно-мышечной передачи осуществляют препаратами калия. Они усиливают синтез ацетилхолина. Лекарства этой фармакологической группы могут использоваться на всех этапах терапии. При длительных периодах ремиссии их назначают с целью профилактики обострения.
Пульс-терапию глюкокортикоидами неврологи проводят при неэффективности предыдущих лекарственных средств, в процессе подготовки к оперативному вмешательству и для борьбы с бульбарными осложнениями. Дозировку врач рассчитывает индивидуально каждому пациенту.
Для воздействия на вилочковую железу используют цитостатики. При кризах или дыхательной недостаточности в Юсуповской больнице больным миастенией проводят сеансы плазмафероза. Одной из новых методик терапии является криофероз. Использование низких температур позволяет очистить кровь и избавиться от вредных веществ.
Также для лечения миастении применяют иммуносорбцию (извлечение антител из крови), гамма-облучение тимуса (воздействие на вилочковую железу радиоактивным излучением), физиотерапевтические процедуры:
Стимуляцию мышц током;
При неэффективности консервативной терапии хирурги выполняют операцию тимэктомию – удаление вилочковой железы. Существуют три основных метода проведения данного хирургического вмешательства:
Транстернальный – вилочковую железу удаляют через разрез грудины;
Трансцервикальный – удаление тимуса выполняют через надрез у основания шеи;
Роботизированная хирургия – операция выполняется с использованием роботизированных манипуляторов.
У 75% пациентов после хирургического вмешательства отмечается значительное улучшение состояния здоровья.
Диетотерапия и коррекция образа жизни
Больным миастенией неврологи назначают специальную диетотерапию. Её цель – повышение защитной функции организма. Блюда должны содержать большое количество калия, фосфора, кальция и витаминов.
Из меню исключают жирные и жареные блюда, копчения, консервы. Пациентам рекомендуют отказаться от употребления спиртных напитков. Также пациентам следует выполнять следующие рекомендации врача:
Отказаться от вредных привычек;
Контролировать массу тела;
Уменьшить время пребывания под прямыми солнечными лучами;
Избегать физических и эмоциональных перегрузок;
Чередовать работу с отдыхом.
Без консультации с лечащим врачом больным миастенией не следует употреблять следующие лекарства: мочегонные препараты, фторхинолы, транквилизаторы, нейролептики, препараты, содержащие фтор, магний, хинин.
Профилактика и прогноз
Заболевание протекает хронически, но врачи клиники неврологии Юсуповской больницы проводят адекватную терапию, позволяющую предотвратить прогрессирование болезни и развитие осложнений:
Криза с остановкой дыхания;
Паралича отдельных мышц или их групп;
Расстройств речевой и зрительной функций;
Нарушений опорно-двигательного аппарата.
Миастения ухудшает качество жизни человека. У людей повышается раздражительность, может возникнуть апатия. Для того чтобы состояние было стабильным, пациенту следует находиться под наблюдением невролога, следить за своим состоянием, при появлении новых симптомов обращаться за консультацией. Ему нужно постоянно контролировать уровень артериального давления, глюкозы крови.
Физическая активность должна быть умеренной. Пациенту рекомендуют делать зарядку, осуществлять пешие прогулки на свежем воздухе. Важно придерживаться прописанной врачом схемы лечения, вовремя принимать лекарственные препараты, соблюдать рекомендованные неврологом дозы медикаментов.
Прогноз при глазной форме миастении наиболее благоприятный. Длительной ремиссии удаётся достичь с помощью тщательно подобранной терапии. Опорно-двигательные нарушения не приводят к летальному исходу, но нарушают качество жизни пациента. Самые опасные последствия отмечаются при нарушении дыхательной функции. Пациент может задохнуться или подавиться пищей. Врачи отделения реанимации и интенсивной терапии в тяжёлых случаях заболевания выполняют искусственную вентиляцию лёгких с помощью дыхательной аппаратуры экспертного класса.
Для того чтобы диагностировать миастению на ранней стадии заболевания, при появлении первых признаках нарушения функции мышц записывайтесь на приём к неврологу Юсуповской больницы онлайн или позвонив по телефону. Специалисты контакт-центра подберут удобное вам время консультации ведущего специалиста в области патологии нервно-мышечной системы.