денатурированная соль что это такое
ДЕНАТУРИРОВАНИЕ
Полезное
Смотреть что такое «ДЕНАТУРИРОВАНИЕ» в других словарях:
денатурирование — денатурация Словарь русских синонимов. денатурирование сущ., кол во синонимов: 1 • денатурация (1) Словарь синонимов ASIS. В.Н. Тришин … Словарь синонимов
денатурирование — Изменение конформации молекул [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN denaturation … Справочник технического переводчика
денатурирование — denatūravimas statusas T sritis chemija apibrėžtis Biopolimero natūralios aktyvios struktūros suardymas. atitikmenys: angl. denaturating; denaturation rus. денатурирование … Chemijos terminų aiškinamasis žodynas
денатурирование — denatūravimas statusas T sritis chemija apibrėžtis Priemaišų, darančių medžiagą netinkamą įprastiniam vartojimui, įmaišymas. atitikmenys: angl. denaturating; denaturation rus. денатурирование … Chemijos terminų aiškinamasis žodynas
Денатурирование — ср. 1. процесс действия по несов. гл. денатурировать 2. Результат такого действия. Толковый словарь Ефремовой. Т. Ф. Ефремова. 2000 … Современный толковый словарь русского языка Ефремовой
денатурирование — денатур ирование, я … Русский орфографический словарь
денатурирование — см. денатурировать 2); я; ср … Словарь многих выражений
Денатурация спирта — (денатурирование) см. Спирт денатурированный … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
2-меркаптоэтанол — 2 меркаптоэтанол … Википедия
ХИМИЯ ОРГАНИЧЕСКАЯ. КЛАССЫ СОЕДИНЕНИЙ — Органические соединения (углеводороды и их производные) можно разделить на два типа: ациклические (или алифатические, т.е. с открытой углеродной цепью) и циклические; последние в свою очередь подразделяются на алициклические, в молекулах которых… … Энциклопедия Кольера
ДЕНАТУРАЦИЯ
ДЕНАТУРАЦИЯ — существенные изменения природных свойств вещества под влиянием химических или физических воздействий. Термин «денатурация» применяется обычно к белкам (см.). Нарушение нативной уникальной структуры под влиянием повышения температуры, высокого гидростатического давления, ультразвука, ионизирующих излучений, резких сдвигов pH, добавления некоторых химических веществ, разрывающих нековалентные связи (напр., мочевины, солей гуанидина, трифторуксусной или трихлоруксусной к-т), называется общим термином «денатурация белков». Молекуле нативного белка свойственна внутренняя упорядоченность, поддерживаемая системой нековалентных связей между многочисленными структурными элементами. При Денатурации такая упорядоченность нарушается. Ковалентные (химические) связи в молекуле белка при Денатурации не затрагиваются, и первичная структура белка сохраняется. Структуры высоких порядков — вторичная или третичная — нарушаются полностью или в значительной степени. Изменение нативного состояния молекул, аналогичное Денатурации белков, известно также и для нуклеиновых кислот (см.).
Биологически активные белки — ферменты, антитела и др.— при Д. инактивируются. Причиной этого является то, что в процессе Д. нарушаются активные центры — точно организованные участки белковых молекул, непосредственно ответственные за соответствующую биол, функцию. Физ.-хим. изменения, сопровождающие Д., также связаны с нарушением упорядоченной структуры белка. Так, при Д. нарушаются (в различной степени) спирализованные участки полипептидной цепи, что фиксируется соответствующими спектрополяриметрическими сдвигами. Переход полипептидной цепи белка из плотно упакованного в беспорядочное и подвижное состояние вызывает изменение вязкости и других гидродинамических свойств их р-ров. В состоянии Д., когда полипептидная цепь становится более подвижной, общая реактивность хим. групп увеличивается. Нетитрующиеся (т. е. не вступающие в реакцию) сульфгидрильные (SH-) и некоторые другие группы, присутствующие во многих нативных белках, обычно титруются после Д. Взаимодействие белков с нек-рыми красителями резко усиливается в результате Д. Из-за повышения доступности и увеличения реактивности различных хим. групп при Д. очень сильно возрастает степень взаимодействия между отдельными белковыми молекулами. В денатурированном состоянии белки легко агрегируют, т. е. денатурированные белки легко осаждаются, свертываются или же латинизируются. Для сохранения белка в растворенном состоянии после Д. приходится применять солюбилизирующие вещества — детергенты (см.), мочевину и др.
Д. белков обычно сопровождается значительным увеличением теплосодержания и энтропии (см. Термодинамика), хотя эти изменения зависят от условий среды. В простейших случаях система при Д., по-видимому, содержит всего две формы белка — нативную и полностью денатурированную. По мере Д. белок переходит из одной формы в другую без заметного образования каких-либо промежуточных форм и, следовательно, весь денатурационный переход белковой молекулы протекает как единый скачок. В других случаях кинетика денатурации указывает на образование в ходе реакции нескольких относительно стабильных не нативных форм белка, что соответствует более сложной схеме перехода. Но если при Д. молекула белка претерпевает несколько конформационных превращений, то каждое из них является кооперативным, т. е. включает большое число взаимозависимых реакций, заключающихся в образовании и разрыве нековалентных связей.
В прошлом Д. рассматривали как необратимый процесс, как переход белка в состояние, имеющее минимальный уровень свободной энергии. Теперь хорошо известно, что Д. обратима. Фактически наступающая необратимость создается, как оказалось, сопутствующими реакциями — агрегацией белка, окислением SH-групп с образованием новых дисульфидных (S—S) связей и пр. Если эти реакции в достаточной мере исключены, то тенденция к возвращению белка в нативное состояние (ренатурация) проявляет себя сразу же по прекращении действия денатурирующего агента.
Если Д. по существу представляет собой физ. переход упорядоченность — беспорядок, то в ренатурации ярко проявляется биол, особенность белков — способность к самоорганизации, путь к-рой определен строением полипептидной цепи, т. е. наследственной информацией. В условиях живой клетки данная информация, вероятно, является решающей для преобразования беспорядочной полипептидной цепи во время или после ее биосинтеза на рибосоме в нативную молекулу белка.
Библиография: Белицер В. А. Макроструктура и денатурационные превращения белков, Укр. биохим, журн., т. 24, в. 2, с. 290, 1962, библиогр.;
Птицын О. Б. Физические принципы самоорганизации белковых цепей, Усп. совр, биол., т. 69, в. 1, с. 26, 1970, библиогр.; Anfinsen С. В. The formation and stabilization of protein structure, Biochem. J., v. 128, p. 737, 1972, bibliogr.; Anfinsen G. B. a. Scheraga H. A. Experimental and theoretical aspects of protein folding, Advanc. Protein Chem., v. 29, p. 205, 1975, bibliogr.; Morawetz H. Rate of conformational transitions in biological macromolecules and their analogs, ibid., v. 26, p. 243, 1972, bibliogr.
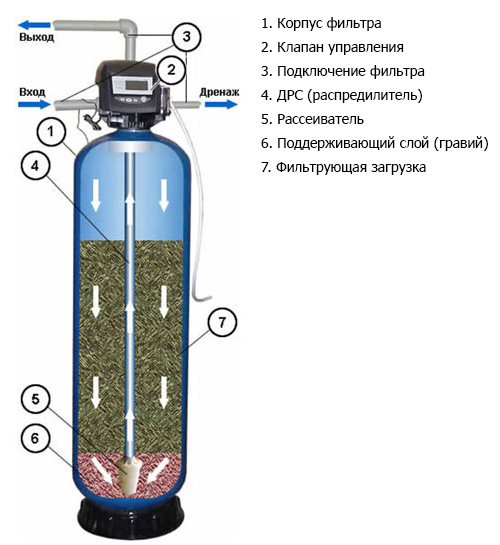
Зачем соль таблетированная для водоочистки?
Как работает таблетированная соль в системах водоочистки?
Этот Процесс выглядит вот так:
Преимущества таблетированной соли
Бессолевые умягчители воды. Слишком хорошо, чтобы быть правдой?
Наряду с различными технологиями в интернете и других источниках, продавцы используют различные методы рекламы и маркетинга, чтобы привнести новые идеи в нашу жизнь. Обращение к идее бессолевого умягчения воды понятно. Было бы трудно найти человека, который не хотел бы сэкономить деньги. Был момент, когда я так же был привлечен рекламой и обломался. Я купил лезвия для бритвы, которые не затупляются. Но продукт оказался обманом и не смог сэкономить мои деньги, скорее наоборот. Тогда я вспомнил совет моего деда «Я все, что я слышу, и только половина того, что я вижу». Как он был прав.
Как-то вечером я слушал радио. Мою любимую мелодию прервала реклама. Это была реклама о «мягкой» воде без использования таблетированных солей, смягчающих воду. В рекламе речь шла о том, что FreeSalt-смягчитель оставляет все хорошие минералы в воде, и не нужно использовать таблетированную и дорогую соль для фильтра.
Что такое «хорошие минералы»? Из школьной программы я знал, что нет хороших или плохих минералов. Реклама заинтересовала меня, потому что зачем платить больше, если можно платить меньше.
И вот, что я выяснил.
Факты о FreeSalt-умягчителях воды
Цикл регенерации 
После того, как ресурс ионообменной смолы исчерпался, фильтр умягчитель начинает автоматически восстанавливать свои фильтрующие свойства. Этот цикл называется циклом регенерации, в котором тот истраченный на умяшчение натрий мы получим из таблетированной соли.
Купить соль для умягчения воды можно лишь в специализированных магазинах. Один из таких магазинов это Фильтромир.
Звоните:
+7 (952) 877-02-37 (Краснодар)
+7-961-290-45-54 (Ростов)
Спасибо, что дочитали статью.
Будьте здоровы! Пейте чистую и проверенную воду!
Действуйте! Выбирайте, консультируйтесь, подбирайте, сравнивайте, покупайте, радуйтесь в месте с ФильтроМиром!
Денатурация: особенности процесса, влияющие факторы, механизмы и последствия
Что такое белки?
Человеческий организм нуждается в различных типах молекул, и наиболее важными являются молекулы белков, которые содержат азот и состоят из аминокислот. Молекулы белка образуют основной строительный блок мышц и других тканей в организме человека. Их название указывает на то, что они имеют решающее значение для здоровья человека. Слово «белок» происходит от греческого «протеос», что означает «первый» или «первом месте». Каждый белок имеет свое место действия и задачи, которые он выполняет. Функции белка можно разделить на 9 основных:
Молекулы белка имеют разные размеры, в зависимости от количества аминокислот. Малые молекулы включают, например, инсулин из 51 аминокислоты, в то время как очень большие молекулы включают титан из почти 27 000 аминокислот.Однако размер молекул не имеет значения, для правильного функционирования они должны быть в подходящей форме. Каждый тип белка имеет уникальную форму, которая определяет роль белка в организме. Попробуйте представить белки как ключи, которые принадлежат только определенным дверям в человеческом организме.
Человеческий метаболизм расщепляет белки на более простые частицы – аминокислоты. 20 аминокислот необходимы для роста мышц и обмена веществ, 11 из которых не являются необходимыми. Это означает, что наш организм может создавать их сам, и их не нужно употреблять в пищу. Остальные аминокислоты помечены как незаменимые, и организм человека получает их из пищи и пищевых добавок. Мышечная ткань не может расти или регенерировать без них.
Что такое денатурация белка?
Денатурация – это процесс, при котором структура белковой молекулы нарушается, тем самым теряя свою функцию. Различия в форме белка могут быть вызвать:
Денатурация меняет форму белка, но последовательность аминокислот остается прежней. Цель протеина в форме пищевой добавки состоит в том, чтобы восполнить достаточное количество белка, и чтобы пищеварительная система могла разрушиться, тем самым снабжая мышечную ткань. Эта функция не теряется при термообработке белков.
Хорошим примером также является белок пепсин, который действует как фермент и расщепляет белки в желудке. Он работает только при низком pH, теряет свою функцию в среде с высоким pH и денатурирует. По этой причине pH желудка поддерживается на очень низком уровне, чтобы обеспечить правильное функционирование пепсина.
Тепло используется для разрыва водородных связей и неполярных гидрофобных взаимодействий в молекуле белка. Более высокая температура увеличивает кинетическую энергию и заставит молекулы вибрировать очень быстро, пока связи между ними не будут разрушены. Молекула белка разворачивается из своей трехмерной структуры, обеспечивая лучший доступ пищеварительного фермента к белковым связям.
Вот почему мы готовим продукты, чтобы изменить структуру белка и облегчить его переваривание. Например, этот процесс происходит, когда вы готовите яйца. В это время белок из яиц денатурируется и во время варки. После употребления вареных яиц переваривание и усвоение содержащихся в них питательных веществ происходит быстрее. Вы можете быть удивлены тем, что такой же процесс происходит при стерилизации медицинских инструментов. Тепло денатурирует белки в бактериях, которые затем уничтожают бактерии и дезинфицируют объекты.
Особенности процесса
Он сопровождается разворачиванием полипептидной связи, которая в растворе изначально представлена в виде беспорядочного клубка.
Процесс денатурации белка сопровождается утрачиванием гидратной оболочки, выпадением белка в осадок, утрачиванием им нативных свойств.
Среди основных факторов, которые провоцируют процесс денатурации, выделим физические параметры: давление, температуру, механическое действие, ионизирующее и ультразвуковое излучение.
Денатурация белка происходит под воздействием органических растворителей, минеральных кислот, щелочей, солей тяжелых металлов, алкалоидов.
Свойства денатурированных белков, виды денатурации
При денатурации утрачивается гидратная оболочка и белок выпадает в осадок и при этом утрачивает нативные свойства.
Денатурацию вызывают физические факторы: температура, давление, механические воздействия, ультразвуковые и ионизирующие излучения; химические факторы: кислоты, щелочи, органические растворители, алкалоиды, соли тяжелых металлов.
Различают 2 вида денатурации:
Свойства денатурированных белков:
Ферментные методы гидролиза основаны на избирательности действия протеолитических ферментов расщепляющих пептидные связи между определенными аминокислотами.
Пепсин расщепляет связи, образованные остатками фенилаланина, тирозина и глутаминовой кислоты.
Трипсин расщепляет связи между аргинином и лизином.
Химотрипсин гидролизует связи триптофана, тирозина и фенилаланина.
Гидрофобные взаимодействия, а также ионные и водородные связи относятся к числу слабых, тк энергия их лишь ненамного превосходит энергию теплового движения атомов при комнатной температуре(т е уже при данной температуре возможен разрыв связей ).
Поддержание характерной для белка конформации возможно благодаря возникновению множества слабых связей между различными участками полипептидной цепи.
Факторы, вызывающие денатурацию белков
Факторы, которые вызывают денатурацию белков, можно разделить на физические и химические.
Воздействие факторами денатурации применяют для стерилизации оборудования и инструментов, а также как антисептики.
Что происходит в процессе денатурации белков
Beyond Meat запускает продажу веганского мяса в Украине
В процессе денатурации белка имеет место разрыв химических связей (дисульфидных, водородных, ван-дер-ваальсовых, электростатических и др.), которые стабилизируют высшие уровни организации белковой молекулы, что обуславливает изменение пространственной структуры белка. Следует отметить, то в большинстве случаев первичная структура белка в процессе денатурации не нарушается, поэтому после раскрутки цепи полипептидов (стадия нити), протеин может снова стихийно скручиваться, при этом образуя «случайный клубок», то есть переходит к хаотическому состоянию, отличного от нативной конформации.
Процесс денатруации белков происходит при температуре выше, чем 56 °С.
Типичными признаками необратимой денатурации белков является снижение гидрофильности и растворимости белков, увеличение оптической активности, изменение изоэлектрической точки, уменьшение устойчивости белковых растворов и молекулярной массы и изменение формы белковых молекул, увеличение вязкости и усиление способности к расщеплению ферментами, переход молекулы в хаотическое состояние, при котором наблюдается агрегация частиц белка и выпадение их в осадок.
Схема денатурации белка: а — нативная молекула; б — развертывание полипептидной цепи; в — стадия нити; г — случайный клубок
При непродолжительном действии денатурирующего агента (например, органического растворителя) возможно восстановление нативной структуры белка. Этот процесс называется ренатурацией. При ренатурации происходит восстанавлениене только структуры, но и биологических функций белка. С денатурацией связаны процессы переработки продуктов питания, изготовления одежды, обуви, консервирования и сушки овощей и фруктов. Результатом необратимой денатурацией протеинов является потеря способности к прорастанию семян при длительном хранении, особенно при неблагоприятных условиях. Процесс денатурации белков широко применяется в медицине, ветеринарии, фармации, клинике и биохимических исследованиях с целью осаждения протеина в биологическом материале с целью дальнейшей идентификации в нем низкомолекулярных и небелковых субстанций, с целью как установления наличия протеина, так и его количественного определения, для обеззараживания слизистых покровов и кожи, для конъюгации солей тяжелых металлов при терапии отравлений солями свинца, ртути, меди и т.п. или с целью профилактики подобных токсикозов на предприятии.
Процесс денатурации белков происходит также при приеме фармакологических препаратов танальбина и танина, на чем базируются их противовоспалительное и вяжущее действие. Вяжущие свойства танина базируются на его способности осаждать протеины с синтезом плотных альбуминатов, защищающих от раздражения тканей, в частности чувствительные нервные окончания. При этом уменьшается проявление воспалительной реакции, а также снижаются болевые ощущения и происходит непосредственное уплотнение мембран клеток. Препарат танальбин представляет собой продукт взаимодействия белка казеина с танином — в отличие от танина, данный препарат не оказывает вяжущего действия на слизистую оболочку желудка и ротовой полости. Только после попадания в кишечник он поддается процессу расщепления, выделяя при этом свободный танин. Применяется в медицине и ветеринарии как вяжущее лекарственное средство при хронических и острых болезнях кишечника, в частности у детей.
В практике фармацевтики использование процессов денатурации белка дает возможность контролировать качество протеиновых препаратов, например, в ампулах.
Последствия
После денатурации происходит переход нативной компактной структуры в рыхлую развернутую форму, упрощается проникновение к пептидным связям ферментов, необходимых для разрушения.
Конформация белковых молекул определяется возникновением достаточного количества связей между разными участками определенной полипептидной цепочки.
Белки, состоящие из достаточного количества атомов, которые находятся в непрерывном хаотичном движении, способствует определенным перемещениям частей полипептидной цепи, что вызывает нарушение общей структуры белков, снижение его физиологических функций.
Белки имеют конформационную лабильность, то есть предрасположенность к незначительным изменениям конформации, происходящим в результате обрыва одних и образования других связей.
Денатурация белка приводит к изменениям его химических свойств, способности вступать во взаимодействие с другими веществами. Наблюдается изменение пространственной структуры и участка, непосредственно контактирующего с иной молекулой, и всей конформацией в целом. Наблюдаемые конформационные изменения имеют значение для функционирования белков в живой клетке.
Механизмы денатурации
Практически любое заметное изменение внешних условий, например, нагревание или обработка белка щелочью приводит к последовательному нарушению четвертичной, третичной и вторичной структур белка. Обычно денатурация вызывается повышением температуры, действием сильных кислот и щелочей, солей тяжелых металлов, некоторых растворителей (спирт), радиации и др.
Денатурация часто приводит к тому, что в коллоидном растворе белковых молекул происходит процесс агрегации частиц белка в более крупные. Визуально это выглядит, например, как образование «белка» при жарке яиц.
Пищевая химия
Пищевая химия (лекция 8)
1. Белки мяса и молока
Наиболее распространенным белком в животном мире является коллаген (кожа, сухожилия, кровеносные сосуды, кости, роговица глаз, хрящи). Он обеспечивает внеклеточную структуру в соединительной животной ткани, существуя не менее чем в пяти различных типах. Коллаген внеклеточный белок, но синтезируется он внутри клетки в виде молекул-предшественников.
Близкий по свойствам к коллагену, в эластичных фибриллах соединительной ткани обнаружен белок эластин, содержащийся в связках и стенках кровеносных сосудов. Этот белок беден пролином.
Мясо, содержащее много соединительной ткани, остается жестким и после тепловой обработки; усвояемость коллагена и эластина в нем очень низкая. Однако при необходимости усилить двигательную функцию кишечника целесообразно использовать продукты, богатые соединительной тканью.
Желатин – продукт неполного гидролиза коллагена. По аминокислотному составу желатин неполноценен, но желеобразные продукты из него перевариваются без напряжения секреции пищеварительных органов. Данное свойство позволяет применять желатин в диетах щадящего режима.
Молоко – это гетерогенная система, в которой в качестве дисперсной фазы выступают эмульгированные жировые глобулы и коллоидные мицеллы казеина, а в роли дисперсионной среды – раствор белков, лактозы, солей и витаминов. Общее содержание белков в молоке колеблется от 2,9 до 3,5 %. Среди них выделяют две основные группы: казеины и сывороточные белки.
В молоке содержится более 20 ферментов, а также гормоны и белки в составе оболочек жировых шариков.
Основными белками молока являются казеины, которые легко перевариваются и являются источниками незаменимых аминокислот, кальция, фосфора и ряда физиологически активных пептидов. Например, при действии в желудке на κ-казеин химозина высвобождаются глико- и фосфопептиды, которые регулируют секрецию желудочного сока, моделируют физико-химические свойства белков, осуществляют защиту от протеолиза и влияют на проницаемость мембран клеток. Важнейшими физиологическими функциями обладают сывороточные белки. Иммуноглобулины выполняют защитную функцию, лактоферрин и лизоцим являются носителями антибактериальных свойств, лактоферрин и β-лактоглобулин выполняют транспортную роль, перенося в кишечник микро- и макроэлементы, витамины и липиды.
Казеин в молоке содержится в виде казеинаткальциевого фосфатного комплекса.
Кальций в составе комплекса выполняет роль структурообразователя, создавая мостик между серинфосфатными группами двух молекул казеина. Казеин молока осаждается при рН 4,6-4,7, когда на его молекулах наступает равенство положительных и отрицательных зарядов. Нерастворимый казеин обладает способностью связывать воду в достаточно больших количествах, что важно для устойчивости частиц белка в сыром, пастеризованном или стерилизованном молоке. Гидрофильные свойства казеина усиливаются при взаимодействии его с β-лактоглобулином, которые наблюдаются в процессе тепловой обработки молока, и от них зависят структурно-механические свойства сгустков, образующихся при кислотном свертывании или получении сырной массы при созревании сыров.
Промышленные казеины получают из обезжиренного молока действием кислот, кисломолочной сыворотки, введением солей кальция, химозина и др. В зависимости от способа получения различают казеинат натрия, казеинат кальция, кислотный, сычужный казеин и копреципитат с разными функциональными свойствами. При производстве новых форм белковой пищи большое значение имеет гелеобразование казеина, его взаимодействие с веществами небелковой природы, образование стойких эмульсий и явление синерезиса.
Белки молока характеризуются высокой биологической ценностью, они содержат в избыточных количествах лизин и триптофан с одновременным недостатком серосодержащих аминокислот. Белки сыворотки содержат незаменимые аминокислоты в значительно больших количествах, чем казеин.