дхм что это такое в химии
Дхм что это такое в химии
Декстрометорфан также использовался для лечения задержки умственного развития, болезни Паркинсона, при лечении легочного и другого рака и для предотвращения отторжения тканей при трансплантации из-за (плохо понятых) эффектов сигма лигандов на опухолевые клетки и иммунную систему.
В России DXM входит в состав сиропов от кашля Гликодин и Туссин Плюс, а так же желатиновые капсулы ТОФФ+
Содержание
Взаимодействие
Ингибиторы МАО (в том числе фуразолидон, прокарбазин, селегилин) при одновременном применении могут вызывать адренергический криз, коллапс, кому, головокружение, возбуждение, повышение АД, гиперпирексию, внутричерепное кровотечение, летаргию, тошноту, спазмы, тремор. В сочетании с трициклическими антидепрессантами (амитриптилин, имован и др) может взывать серотониновый синдром и возможный последующий летальный исход. Амиодарон, флуоксетин, хинидин, ингибируя систему цитохрома P450, могут повышать концентрацию препарата в крови. Табачный дым может привести к повышению секреции желез на фоне ингибирования кашлевого рефлекса.
Побочные действия
Сонливость, тошнота, головокружение. Симптомы: возбуждение, головокружение, снижение АД, тахикардия, гипертонус мышц, атаксия. Лечение: ИВЛ, симптоматические ЛС. При передозировке может проявляться (в зависимости от количества) сонливость, или, наоборот, возбуждение, нарушение координации, психики. Антидот при передозировке — налоксон, может применяться при передозировке в 100 и более раз.
Противопоказания
Гиперчувствительность, бронхиальная астма, бронхит, одновременный прием муколитических ЛС.C осторожностью. Нарушения функции печени, беременность (I триместр).
История DXM
1958 — DXM одобрен Управлением по контролю за пищевыми продуктами и лекарственными средствами (FDA — Food and Drug Administration) для продажи в качестве средства от кашля.
1960-ые — 1970-ые — Таблетки, содержащие DXM, продаются под фирменным знаком «Romilar». «Romilar» был предложен как замена для кодеина, использующегося раннее как средство от кашля, чтобы предотвратить его использование как наркотического средства.
1973 — «Romilar» (таблетки содержащие DXM) сняты с продажи после многократных случаев использования их в качестве наркотического средства.
1977 — «Romilar» в виде таблеток заменен сиропами от кашля содержащими DXM. Это было разработанно специально, чтобы предотвратить использование его в качестве наркотического средства.
1990—2009 — Использование DXM в качестве наркотика продолжается. Множество смертельных случаев было зарегистрировано после использования DXM, хотя большинство их было результатом употребления конкретных сиропов («Coricidin» и «Cold») в большом количестве, так как они сочетают в своем составе DXM вместе с другими химическими веществами, которые становятся опасными при больших дозах. Тем самым DXM нельзя обвинять в этих смертях, так как они наступают не от самого вещества, а от совершенно иных веществ, содержащихся в опасных сиропах(таких веществ, как, например, парацетамол).
Рекреационное использование
Поскольку декстрометорфан в высоких дозах оказывает диссоциативное действие, сходное в некотором роде с действием кетамина и фенциклидина, иногда его используют в рекреационных целях. В некоторых случаях возможна психологическая зависимость. Физической зависимости декстрометорфан не вызывает.
Возможные побочные эффекты при однократном (случайном) употреблении:
— Тошнота и желудочные боли
— Головокружение
— Небольшие аллергические реакции
— Сексуальная дисфункция
— Повышенное потоотделение
— Тахикардия
— Гипертония
— Увеличенная температура
— Крапивница (Хотя все это может быть вызвано скорее дополнительными составляющими сиропов от кашля (Туссин Плюс, Гликодин), нежели самим декстрометорфаном)
Возможные побочные эффекты при многократном употреблении:
— Панические состояния
— Психотические срывы
— Депрессия
— Очень высокая температура
— Очень высокое давление
— Затруднение дыхания
— Аллергические реакции
Возможные побочные эффекты при систематическом употреблении:
— Инсульт
— Различные мании
— Депрессия
— Паранойя
— Ухудшение памяти
— Потеря веса
— Психозы
— Повреждение печени, почек, и поджелудочной железы
— Необратимые поражения мозга. Так называемые Лезии Олни, которые были обнаружены при проведении опытов над крысами, но возможность их появления у человека не доказана
Другие нестандартные использования
Законодательное регулирование
Входит в список III Перечня наркотических средств (список психотропных веществ, оборот которых в Российской Федерации ограничен и в отношении которых допускается исключение некоторых мер контроля в соответствии с законодательством Российской Федерации и международными договорами Российской Федерации).
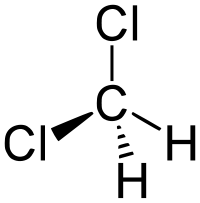
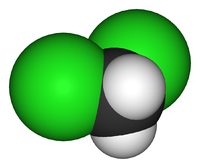
Дихлорметан
| Дихлорметан | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | дихлорметан |
| Сокращения | ДХМ |
| Традиционные названия | дихлорметан, метилен хлористый |
| Химическая формула | CH2Cl2 |
| Эмпирическая формула | CH2Cl2 |
| Физические свойства | |
| Состояние (ст. усл.) | подвижная прозрачная жидкость |
| Примеси | хлорметаны |
| Молярная масса | 84.9 г/моль |
| Плотность | 1.3266 г/см³ |
| Термические свойства | |
| Температура плавления | -96.7 °C |
| Температура кипения | 40 °C |
| Температура вспышки | 14 °C |
| Критическая точка | 245 |
| Энтальпия образования (ст. усл.) | -87.86 кДж/моль |
| Удельная теплота испарения | 336,4 Дж/кг |
| Давление пара | 470 |
| Химические свойства | |
| Растворимость в воде | при 20 °C 1.3 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,4242 |
| Классификация | |
| Рег. номер CAS | 75-09-2 |
| SMILES | C(Cl)Cl |
| RTECS | PA8050000 |
Дихлормета́н (хлористый метилен, ДХМ, CH2Cl2) — прозрачная легкоподвижная и легколетучая жидкость с характерным для галогенпроизводных сладковатым запахом. Впервые был синтезирован в 1840 году выдерживанием смеси хлора с хлористым метилом на свету. В целом наиболее безопасен среди галогеналканов.
Содержание
Получение
Получают прямым хлорированием метана хлором в условиях радикального механизма при 400—500 °C при соотношении равном 5:1
В результате получается смесь всех возможных хлоридов: хлорметан, дихлорметан, хлороформ и четырёххлористый углерод, которые потом разделяются дистилляцией. После чего он имеет чистоту не менее 99,7 % В 1995 году годовое производство оценивалось в 500 миллионов тонн.
Свойства
Растворимость в воде 2% по массе (13 г/л), смешивается с большинством органических растворителей. Легколетуч (40 °C), образует азеотропную смесь с водой (т.кип. 38,1 °C, 98,5 % дихлорметана). Метиленхлорид (дихлорметан) реагирует с хлором с образованием хлороформа и четырёххлористого углерода. С йодом при 200 °C дает СН2l2, с бромом при 25-30 °C в присутствии алюминия — бромхлорметан. При нагревании с водой гидролизуется до СН2О и НСl. При нагревании со спиртовым раствором NH3 до 100—125 °C образует гексаметилентетрамин. Реакция с водным раствором NH3 при 200 °C приводит к метиламину,муравьиной кислоте и НСl. С ароматическими соединениями в присутствии АlСl3 метиленхлорид вступает в реакцию Фриделя — Крафтса, например с бензолом образует дифенилметан. [1]
Применение
Дешевизна, высокая способность растворять многие органические вещества, легкость удаления, относительно малая токсичность привела к широкому применению его как растворителя для проведения реакций, экстракций в том числе и в лабораториях. Используют в смесях для снятия лака, обезжиривания поверхностей. В пищевой промышленности используют для приготовления быстрорастворимого кофе, экстракта хмеля и других пищевых препаратов. Для растворения смол, жиров, битума. Его высокая летучесть используется для вспенивания полиуретанов.
Также используется в хроматографии.
В промышленности в смеси с полимерами используют для создания формы, которая быстро застывает за счёт испарения дихлорметана. Он также используется для склеивания пластмасс: полистирола, поликарбонатов, полиэтилентерефталата, АБС-пластиков, но не для полиэтилена и полипропилена.
Очистка в лаборатории
Специализированные применения
Дихлорметан используется в составах для склеивания пластиков. В смеси с метанолом используют как пропеллент, в качестве хладагента.
Безопасность
Хотя он и является наименее ядовитым среди галогеналканов, но нужно быть осторожным при обращении, так как он очень летуч и может вызвать острое отравление. Работы следует проводить при работающей вытяжной вентиляции.
В организме дихлорметан метаболизируется до монооксида углерода, что может вызвать отравление им. Длительный покровный контакт с дихлорметаном может вызвать его накопление в жировых тканях и привести к ожогу. Также при длительной работе с ним возможно поражение печени и нейропатия.
В Евросоюзе запрещены краски с дихлорметаном как для личного пользования, так и для профессонального применения.
Для регулярной работы с дихлорметаном не подходят перчатки из латекса или нитриловые.
Контакт дихлорметана с щелочными металлами приводит к взрыву.
ПДК в рабочей зоне 50мг/м³, в воде водоёмов не более 7.5 мг/л. КПВ 12-22 %
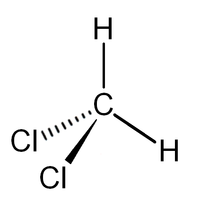
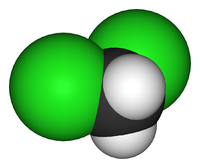
Хлористый метилен
Хлористый метилен
| Дихлорметан | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | дихлорметан |
| Сокращения | ДХМ |
| Традиционные названия | дихлорметан, метилен хлористый |
| Химическая формула | CH2Cl2 |
| Эмпирическая формула | CH2Cl2 |
| Молярная масса | 84.9 г/моль |
| Физические свойства | |
| Плотность вещества | 1.3266 г/см³ |
| Примеси | хлорметаны |
| Состояние (ст. усл.) | подвижная прозрачная жидкость |
| Термические свойства | |
| Температура плавления | -96.7 °C |
| Температура кипения | 40 °C |
| Температура вспышки | 14 °C |
| Критическая точка | 245 |
| Энтальпия (ст. усл.) | -87.86 кДж/моль |
| Удельная теплота парообразования | 336,4 Дж/кг |
| Давление пара | 470 |
| Химические свойства | |
| Растворимость в воде | 20 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,4242 |
| Классификация | |
| номер CAS | 75-09-2 |
| RTECS | PA8050000 |
Дихлорметан (хлористый метилен, ДХМ, CH2Cl2) — прозрачная лекгоподвижная и легколетучая жидкость с характерным для галогенпроизводных сладковатым запахом. Впервые был синтезирован в 1840 году выдерживанием смеси хлора с хлористым метилом на свету. В целом наиболее безопасен среди галогеналканов.
Содержание
Получение
Получают прямым хлорированием метана хлором в условиях радикального механизма при 400—500 °С при соотношении равном 5:1
В результате получается смесь всех возможных хлоридов: хлорметан, дихлорметан, хлороформ и четырёххлористый углерод, которые потом разделяются дистилляцей. После чего он имеет чистоту не менее 99,7% В 1995 году годовое производство оценивалось в 500 миллионов тонн.
Свойства
Применение
Дешевизна, высокая способность растворять многие органические вещества, легкость удаления, относительно малая токсичность привела к широкому применению его как растворитель для проведения реакций, экстракций в том числе и в лабораториях. Используют в смесях для снятия лака, обезжиривания поверхностей. В пищевой промышленности используют для приготовления быстрорастворимого кофе, экстракта хмеля и других пищевых препаратов. Для растворение смол, жиров, битума. Его высокая летучесть используется для вспенивания полиуретанов. Также используется в хроматографии. В промышленности в смеси с полимерами используют для создания формы которая быстро застывает за счёт испарения дихлорметана. Он же используется для склеивания этих пластиков: полистирол, поликарбонат, полиэтилентерефталат, АБС-пластик, но не для полиэтилена и полипропилена.
Очистка в лаборатории
Специализированные применения
Используется в составах для склеивания пластиков. В смеси с метанолом используют как пропеллент, в качестве хладагента.
Безопасность
Хотя он и является наименее ядовитым среди галогеналканов, но нужно быть осторожным при обращении, так как он очень летуч и может вызвать острое отравление. Вытяжная вентиляция необходима. В организме дихлорметан метаболизируется до монооксида углерода, что может вызвать отравление им. Длительный покровный контакт с дихлрометаном может вызвать накопление его в жировых тканях и привести к ожогу. Также при длительной работе с ним возможно поражение печени и нейропатия. На крысах показано, что он может вызывать рак лёгких, печени и поджелудочной железы. В тоже время не было отмечено какого либо влияния на развития эмбрионов у женщин имевших контакт с ДХМ.
Общая безопасность и методы устранения аварий [3]
Примечания
Полезное
Смотреть что такое «Хлористый метилен» в других словарях:
Хлористый метилен — (хим.), дихлорметан СН2Cl2, получен впервые Реньо при действии хлора на X. метил: СН3Cl + Cl2 = CH2Cl2 + HCl; впоследствии он получен Бутлеровым при пропускании струи хлора в йодистый метилен: СН2J2 + Cl2 = CH2Cl2 + J2 и Перкиным при действии… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
хлористый метилен — дихлорметан … Cловарь химических синонимов I
дихлорметан — хлористый метилен … Cловарь химических синонимов I
Болотный газ или метан — (также водородистый метил, формен) предельный углеводород состава СН4, первый член ряда СnН2n+n, одно из простейших соединений углерода, вокруг которого группируются все остальные и от которого могут быть произведены через замещение атомов… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Химическое строение — Настоящая статья имеет задачей изложение истории возникновения теории X. строения органических соединений и ее связи с предыдущими теориями. В значительной мере это уже выяснено в статьях Замещение, Унитарная система, Химических типов теория и… … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Галоидопроизводные — Этим именем в органической химии обозначаются вообще продукты, происходящие из различных органических веществ (углеводородов, спиртов, кислот, альдегидов, кетонов, аминов и пр.) через замещение в них атомов водорода углеводородных групп галоидами … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Термохимия — отдел химии, занимающийся превращениями внутренней энергии тел в тепло при химических процессах. Почти каждая химическая реакция связана с тем или иным тепловым эффектом: химическое превращение сопровождается или выделением, или поглощением тепла … Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона
Отравления — I Отравления (острые) Отравления заболевания, развивающиеся вследствие экзогенного воздействия на организм человека или животного химических соединений в количествах, вызывающих нарушения физиологических функций и создающих опасность для жизни. В … Медицинская энциклопедия
Дихлорметан — Дихлорметан … Википедия
Декстрометорфан
Химическое название
Химические свойства
Декстрометорфан, что это такое? Данное химическое соединение представляет собой противокашлевое средство, оптический левовращающий изомер меторфана. Несмотря на свое сходство с морфином, средство не обладает опиатными эффектами.
Обычно в составе лекарственных средств вещество находится в виде декстрометорфана гидробромида. Это белые кристаллы, горькие на вкус, не обладающие специфическим запахом. Молекулярная масса соединения = 370,3 грамма на моль. Оно хорошо растворяется в хлороформе, хуже – в воде и эфире. Одним из основных способов получения Декстрометорфана является метилирование 3-окси-N-метилморфинана.
Вещество чаще всего используют в комбинации с прочими лекарствами в качестве замены кодеина. Также широко распространено рекреационное употребление препарата в качестве диссоциатива. Также в медицине средство используют для проведения диагностики, лечения припадков, алкоголизма, некоторых нейродегенеративных заболеваний и зависимости от героина. Иногда лекарство применяют для лечения задержки умственного развития у детей, болезни Паркинсона, при раке легких и трансплантации.
В связи с тем, что Декстрометорфан в высоких дозировках может оказывать действие, сходное с диссоциативными и психоделическими веществами (схожее с фенциклидином и кетамином) его применяют в рекреационных целях. Вещество может вызвать психологическую зависимость.
Также ведутся исследования способности лекарства блокировать NMDA-каналы в клетках поджелудочной железы и приводить к блокировке роста базального уровня инсулина. Данное свойство можно использовать, чтобы помочь больным сахарным диабетом 2 типа, которые раньше были вынуждены принимать метформин. Возможно, препарат способен повышать интенсивность выработки инсулина, не приводя к негативным последствиям, а именно – гипогликемии.
На территории РФ данное химическое соединение входит в список 3-го перечня наркотических средств, оборот которых ограничен государством. Чаще всего лекарство можно увидеть в составе сиропов от кашля, капсул для приема внутрь или таблеток.
Фармакологическое действие
Подавляет активность кашлевого центра.
Фармакодинамика и фармакокинетика
Декстрометорфана гидробромид после проникновения в системный кровоток воздействует непосредственно на кашлевой центр, расположенный в продолговатом мозгу, снижая порог чувствительности центра к внешним раздражителям и предотвращая сухой кашель. При использовании вещества в терапевтических дозах, оно не обладает анальгезирующим, снотворным или наркотическим эффектами.
После приема внутрь лекарство начинает действовать в течение 10 минут – получаса. Продолжительность действия составляет от 5 до 9 часов (дети). В головном мозгу вещество также оказывает влияние на процессы обратного захвата серотонина и активизирует сигма рецепторы. Средство способно блокировать N-метил-D-аспартат каналы при использовании дозировок более 150 мг.
Абсолютная биологическая доступность средства составляет 11%. Метаболизм лекарства протекает в тканях печени, с участием системы цитохрома Р450 (в основном CYP2D6, менее выражено CYP3A4 и CYP3A5). Выводятся метаболиты из плазмы крови с помощью почек в течение 1,4 — 4 часов.
Показания к применению
Декстрометорфан назначают для лечения сухого кашля различного происхождения в сочетании с прочими противопростудными и противокашлевыми препаратами.
Противопоказания
Осторожность рекомендуется соблюдать при печеночной недостаточности, беременным женщинам в первые 3 месяца.
Побочные действия
Обычно при использовании терапевтических дозировок лекарства побочные эффекты не проявляются. Тем не менее, в зависимости от индивидуальных особенностей пациента могут проявиться: тошнота, слабость, сонливость и головокружение.
Декстрометорфан, инструкция по применению (Способ и дозировка)
В зависимости от лекарственной формы и тяжести заболевания препарат могут назначить в различной дозировке.
Как правило, для взрослых и детей от 12 лет суточная дозировка = 60 мг. Лекарство распределяют на 4 приема в день. Для детей от 6 лет необходима коррекция дозировки (30 мг в сутки по 7,5 мг за один прием).
Передозировка
В зависимости от принятой дозы могут проявляться различные побочные реакции. Наблюдаются: сонливость или сильное психомоторное возбуждение, атаксия, тахикардия, снижение артериального давления, галлюцинации, непроизвольные движения мышцами, тошнота.
В качестве лечения показано: ИВЛ, симптоматическая терапия, введение налоксона в качестве антидота.
Взаимодействие
При сочетании препарата с ингибиторами МАО (селегилином, фуразолидоном, прокарбазином) может возникнуть коллапс, головокружение, адренергический криз, рост артериального давления, возбуждение, тошнота, кровотечения внутричерепные, тремор и спазмы, вплоть до летаргии и комы.
Одновременный прием средства и трициклических антидепрессантов чреват развитием серотонинового синдрома и летального исхода.
Под действием средств, ингибирующих систему цитохрома Р450 (хинидина, амиодарона, флуоксетина и т.д.) может повыситься концентрация Декстрометорфана в крови, удлиниться время его действия на организм.
Вдыхание табачного дыма приводит к повышению секреции желез, что крайне нежелательно на фоне угнетения кашлевого рефлекса, происходящего под действием препарата.
Условия продажи
Условия хранения
Условия хранения стандартные, обычно зависят от лекарственной формы и производителя.
Детям
Вещество можно назначать детям от 6 лет. В таком возрасте необходимо скорректировать дозировку препарата. Для детей от 12 лет используется взрослая дозировка.
При беременности и лактации
Особую осторожность необходимо соблюдать женщинам в 1 триместре беременности.
