дидрогестерон что делает в организме человека
Главный «антистрессовый» гормон организма
Дегидроэпиандростерон или ДГЭА — является гормоном с андрогенной активностью. ДГЭА отвечает за развитие вторичных половых признаков, поддержание половой функции, а также обладает анаболическим действием. 90% гормона образуется в коре надпочечников, остальные 10% синтезируется у мужчин в семенниках, у женщин в яичниках.
Предшественником ДГЭА является холестерин. В свою очередь, ДГЭА преобразуется в другие стероидные гормоны. В организме мужчин ДГЭА конвертируется в более сильные андрогены: тестостерон и андростендион; у женщин — эстроген и прогестерон. Производство гормона происходит под контролем АКТГ.
Уровни ДГЭА достигают пика в юношеском возрасте, а затем постепенно снижаются. В 70–80 лет значения ДГЭА составляют лишь 10–20% от пикового значения в пубертатном периоде.
ДГЭА во многом работает как синергетический близнец другого гормона стресса — кортизола. Это помогает организму более эффективно адаптироваться к стрессовому воздействию. Стресс может быть любым: физическим, психическим и эмоциональным, но его воздействие всегда происходит длительно. Например, учеба, которая дается человеку с трудом или изнуряющие условия на работе — могут стать источником серьезных проблем для здоровья.
Исследования показали, что снижение уровня ДГЭА связано с аллергией, воспалением, усталостью, аутоиммунными проблемами, сексуальной дисфункцией, инфекциями, бессонницей, снижением когнитивных функций, сердечно-сосудистыми заболеваниями, потерей массы костной ткани, депрессией и раком.
ДГЭА и кардиоваскулярная патология
ДГЭА оказывает защитное действие по отношению к заболеваниям сердечно-сосудистой системы. Результаты исследования, опубликованные в 2014 г в журнале Американского колледжа кардиологов, показали, что низкий уровень ДГЭА в крови связан с риском развития коронарной болезни сердца у пожилых мужчин. Ученые из Гарвардской школы общественного здравоохранения обнаружили связь между низкими уровнями ДГЭА и высоким риском развития инсульта у пожилых женщин.
ДГЭА и остеопороз
ДГЭА улучшает минеральную плотность костной ткани и тормозит остеопороз. Особенно это важно для женщин, которые находится в постменопаузе и страдают от дефицита женских половых гормонов.
ДГЭА и сексуальное поведение
Здоровые уровни ДГЭА поддерживают здоровую сексуальную жизнь. ДГЭА улучшает либидо у мужчин и женщин в равной степени.
ДГЭА и когнитивные функции
Исследования показали, что ДГЭА поддерживает здоровые когнитивные функции и настроение. Гормон поддерживает производство и функционирование нейротрансмиттеров в мозге — химических веществ, которые влияют на память и настроение.
Было обнаружено, что ДГЭА обладает регенеративной активностью по отношению к тканям мозга. Люди, страдающие от болезни Альцгеймера, имеют низкий уровень факторов роста, жизненно необходимых для нервной ткани. ДГЭА может защитить тонкие ткани мозга, сохранив их.
Люди с низким уровнем ДГЭА более восприимчивы к тревоге и депрессии.
ДГЭА и метаболический ответ на инсулин
ДГЭА предотвращает развитие сахарного диабета. Гормон позволяет клеткам более эффективно усваивать глюкозу, тем самым снижая резистентность тканей к инсулину. Как известно, это ведущая причина развития сахарного диабета 2-го типа.
ДГЭА и здоровье иммунной системы
ДГЭА имеет решающее значение для укрепления иммунной системы. При хроническом стрессе уровень кортизола падает, и иммунная система оказывается подавленной. Но здоровые уровни ДГЭА могут уравновесить это состояние.
Некоторыми исследователями было продемонстрировано, что ДГЭА играет определенную роль в борьбе с аутоиммунными состояниями, особенно с красной волчанкой.
Недостаток ДГЭА способствует ряду заболеваний и состояний, поэтому для поддержания оптимального сердечно-сосудистого здоровья и жизнеспособности на протяжении всей жизни важно следить за уровнем ДГЭА. Возможно определение гормона в образцах крови, а также в образцах слюны.
Поскольку для хорошего здоровья имеет значение правильный баланс гормонов, поэтому уровень ДГЭА сопоставляют с уровнем кортизола.
Тестирование уровня ДГЭА и сохранение гормонального баланса между стресс-гормонами является ключом успеха на пути к долголетию. Хороший уровень ДГЭА поможет почувствовать себя моложе, сильнее и увереннее.
Дигидротестостерон – гормональная причина выпадения волос
Гормональный фон воздействует на организм человека комплексно. Если он находится в пределах нормы, то, как правило, проблем не возникает. А вот перекос в сторону выше или ниже естественного продуцирования тех или иных гормонов способен оказать отнюдь не самое позитивное влияние на наше здоровье и нашу внешность. В частности именно гормональные сдвиги являются достаточно частой причиной выпадения волос или так называемой алопеции. В случае, если речь идет о женском организме данное состояние называется андрогенной алопецией.
Распространено мнение, что именно повышенное содержание в организме на постоянной основе главного мужского полового гормона – тестостерона, является причиной облысения не только у представителей сильной половины человечества, но и у женщин, и соответственно поводом обращаться за пересадкой волос к специалистам. Тем не менее, это утверждение будет верным лишь отчасти. С точки зрения медицины и биохимии дело обстоит несколько по-другому.
Что препятствует восстановлению волос? Гормон, который «не виден».
При подозрении на андрогенную алопецию чаще всего главным диагностическим методом является анализ крови на определение уровня общего и свободного тестостерона. Особенно, если речь идет о женской проблеме. В то же время уровень тестостерона может быть вполне нормальным, но человек продолжает терять волосы. И тогда нередко мысль об андрогенной алопеции отвергается и начинается поиск других причин.
На самом же деле виновником является тот же гормон, но в преобразованном виде, поэтому анализ крови его и не определяет. Дигидротестостерон – производный от тестостерона считается основной причиной обращения пациентов в клиники для трансплантации волос. Но едва ли процедура даст желаемый эффект, если не устранить первопричину заболевания.
Дигидротестостерон синтезируется организмом в ответ на выработку избыточного количества тестостерона, чтобы нормализовать уровень «чистого» гормона.
Негативное действие дигидротестостерона на рост волос заключается в следующем: вещество как бы стягивает волосяной фолликул и не дает волосу полноценно расти. И чем более выражено это воздействие, тем сильнее сжатие, и в какой-то момент рост волоса становится просто невозможным.
Процедура HFE способна решить эту проблему, но эффект сохранится лишь в том случае, если препятствие – избыток дигидротестостерона, будет устранен.
Квалификация
Член Международного общества трансплантации и восстановления волос ISHRS, США, член Российского общества трихологов и действительный член Общества врачей Европы, член FUE EUrope. Более чем 17ти летний опыт по трансплантации волос по новейшим методикам в России и зарубежных клиниках.
Выпускница ДонМИ, 1992 год. Интернатура дерматовенерология. С 1998 года работает по пересадке волос в клиниках Греции, Италии, Франции, Португалии, Сербии. В 2004 году осваивает новый полностью безоперационный способ пересадки волос FUE/FUI и начинает сотрудничать с компанией DHI. С 2008 года работает в Ирландии и Англии, используя более совершенный способ безоперационной трансплантации волос Н+. После обучения в России на курсах повышения квалификации, Шнайдер становится членом Российского общества трихологов. С 2009-2010 года внедряет в России усовершенствованную методику безоперационной пересадки волос на основе Н+, которая получает название HFE (в международной аббревиатуре: изъятие способом FUE manually панчем 0,6-0,8мм и постановка способом FUI с имплантером choi 0,6-0,8мм).
Регулярно проводит трансплантацию волос за рубежом.
Дигидротестостерон – гормональная причина выпадения волос
Гормональный фон воздействует на организм человека комплексно. Если он находится в пределах нормы, то, как правило, проблем не возникает. А вот перекос в сторону выше или ниже естественного продуцирования тех или иных гормонов способен оказать отнюдь не самое позитивное влияние на наше здоровье и нашу внешность. В частности именно гормональные сдвиги являются достаточно частой причиной выпадения волос или так называемой алопеции. В случае, если речь идет о женском организме данное состояние называется андрогенной алопецией.
Распространено мнение, что именно повышенное содержание в организме на постоянной основе главного мужского полового гормона – тестостерона, является причиной облысения не только у представителей сильной половины человечества, но и у женщин, и соответственно поводом обращаться за пересадкой волос к специалистам. Тем не менее, это утверждение будет верным лишь отчасти. С точки зрения медицины и биохимии дело обстоит несколько по-другому.
Что препятствует восстановлению волос? Гормон, который «не виден».
При подозрении на андрогенную алопецию чаще всего главным диагностическим методом является анализ крови на определение уровня общего и свободного тестостерона. Особенно, если речь идет о женской проблеме. В то же время уровень тестостерона может быть вполне нормальным, но человек продолжает терять волосы. И тогда нередко мысль об андрогенной алопеции отвергается и начинается поиск других причин.
На самом же деле виновником является тот же гормон, но в преобразованном виде, поэтому анализ крови его и не определяет. Дигидротестостерон – производный от тестостерона считается основной причиной обращения пациентов в клиники для трансплантации волос. Но едва ли процедура даст желаемый эффект, если не устранить первопричину заболевания.
Дигидротестостерон синтезируется организмом в ответ на выработку избыточного количества тестостерона, чтобы нормализовать уровень «чистого» гормона.
Негативное действие дигидротестостерона на рост волос заключается в следующем: вещество как бы стягивает волосяной фолликул и не дает волосу полноценно расти. И чем более выражено это воздействие, тем сильнее сжатие, и в какой-то момент рост волоса становится просто невозможным.
Процедура HFE способна решить эту проблему, но эффект сохранится лишь в том случае, если препятствие – избыток дигидротестостерона, будет устранен.
Менопаузальная гормонотерапия (МГТ)

Почему же процент женщин, принимающих МГТ, остается невысоким?
Крупное американское исследование WHI (Women’s Health Initiative, 2002 г.) вызвало драматический период в судьбе менопаузальной гормонзаместительной терапии, что способствовало резкому сокращению МГТ в большинстве стран мира, появлению страхов и сомнений в отношении пользы и рисков.
Преждевременное завершение части исследования по менопаузальной гормонзаместительной терапии (МГТ) привлекло к себе всеобщее внимание. Как женщины, так и врачи чувствовали себя обманутыми, так как терапия, которая до этого считалась полезной для здоровья в долгосрочной перспективе, теперь оказалась опасной. Отличающийся от фактического изложения пресс-релиз предварительной работы прогремел в СМИ за неделю до того, как сама статья стала доступна для большинства читателей. Сообщалось, что исследование было остановлено в связи с повышенным риском развития рака молочной железы, связанным с заместительной гормональной терапией. На самом деле, в скорректированном анализе связь МГТ и рака молочной железы не была статистически значима!
Последующий углубленный анализ результатов WHI показал, что МГТ характеризуется благоприятным профилем пользы/риска у более молодых женщин, которые начинают терапию в близкие к менопаузе сроки. Эти результаты характеризовались сходным защитным воздействием терапии в отношении ИБС и снижения общей смертности, которые были продемонстрированы ранее в крупномасштабных наблюдательных исследованиях с участием относительно молодых женщин. После WHI широкое распространение получила так называемая временная гипотеза или гипотеза «окна терапевтических возможностей», согласно которой существует различное влияние МГТ на атеросклероз и связанные с ним клинические события в зависимости от возраста женщины и времени начала использования МГТ по отношению к моменту наступления менопаузы.
Основными недостатки данного исследования являлись:
Что же происходит с женским организмом в 45-55 лет?
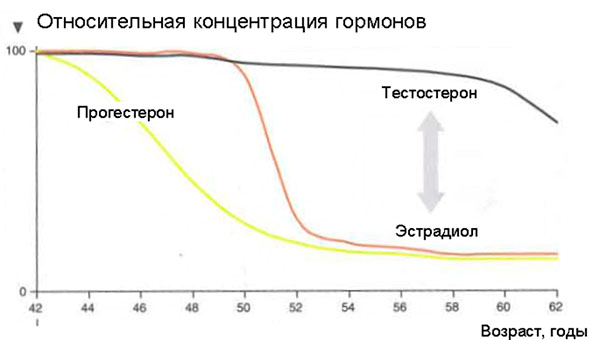
Что будет если МГТ не проводить?
А зачем нужно так «рисковать» и принимать «страшные» гормональные препараты при наступлении менопаузы? Ведь это естественный процесс, может, пусть все идет, как заведено природой? — Но тогда мы неизбежно столкнемся с заболеваниями, которые также предопределены природой.
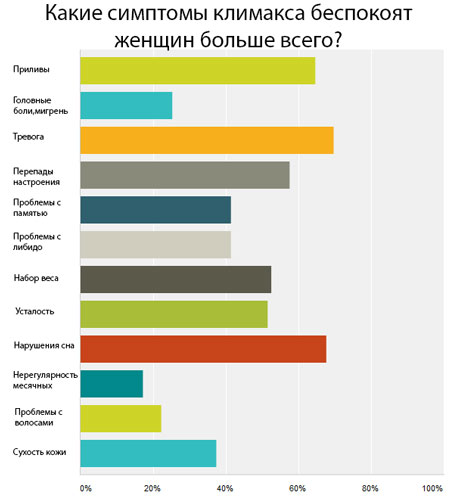
Сначала появляются ранние симптомы:
Через некоторое время появятся и поздние нарушения, связанные с длительным дефицитом половых гормонов:
Какое обследование проводится перед МГТ
Перед назначением менопаузальной гормональной терапии необходимо обследование (впрочем, которое необходимо проводить хотя бы раз в год и без терапии всем сознательным женщинам старше 45 лет).
Дополнительные обследования (при соответствующих данных анамнеза):
Когда пора начинать менопаузальную гормональную терапию?
Но проблема в том, что диапазон нормы ФСГ огромен, и для каждой женщины уровень свой. В идеале нужно сдать анализы крови на гормоны в период максимального расцвета – с 19 до 23 лет. Это и будет вашей индивидуальной идеальной нормой. А начиная с 45 лет ежегодно сверять с ней результаты. Но даже если вы впервые слышите о ФСГ – лучше поздно, чем никогда: в 30, 35, 40 лет имеет смысл выяснить свой гормональный статус, чтобы ближе к критическому возрасту было, на что ориентироваться.
Как самостоятельно понять, что пришло время МГТ?
Уровень эстрогенов снизился, если:
Препаратов огромное количество, какие из них наиболее безопасны?
Действует принцип «минимальности» и «натуральности»!
Для менопаузальной гормональной терапии применяются различные препараты, которые могут быть разделены на несколько групп:
«Натуральные» эстрогены – это препараты эстрогенов, которые по химической структуре идентичны эстрадиолу, синтезируемому в организме женщин. Благодаря современным технологиям создан синтетический эстрадиол, но по своей химической структуре он идентичен натуральному Эстрадиол–17b.
На сегодняшний день таким критериям более всего соответствует препарат Фемостон. Препараты линейки фемостона имеют различные дозировки, что укладывается в один из основных постулатов современной концепции МГТ – использование наименьшей возможной дозировки, которая сохраняет эффективность.
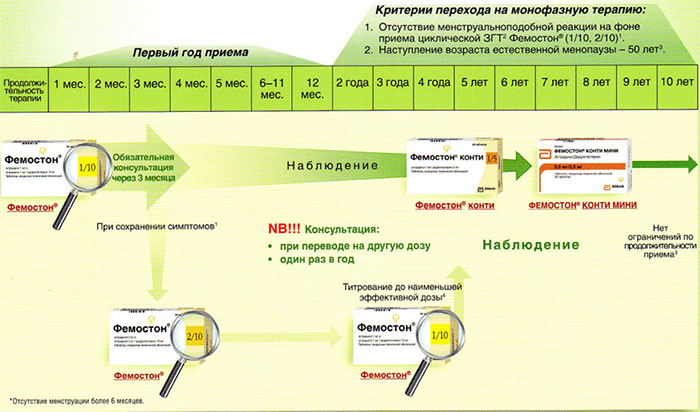
Препараты для двухфазной терапии – когда еще есть месячные
Фемостон 1/10 и Фемостон 2/10
В состав Фемостона 1/10 входят 28 таблеток. 14 белых, содержащих 1 мг Эстрадиола, и 14 серых, содержащих 1 мг Эстрадиола и 10 мг Дидрогестерона.
Состав Фемостона 2/10 отличается только количеством Эстрадиола
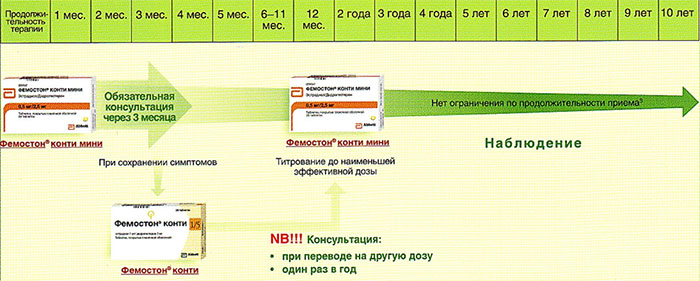
Препараты для монофазной терапии – когда месячные отсутствуют
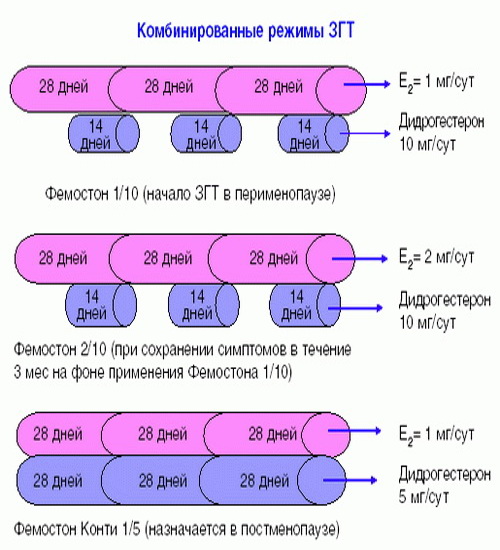
В состав Фемостона конти 1/5 входят 28 таблеток, содержащих 1 мг Эстрадиола и 5 мг Дидрогестерона.
В состав Фемостона мини 0,5/2,5 входят 28 таблеток, содержащих 0,5 мг Эстрадиола и 2,5 мг Дидрогестерона.
Ниже представлена более подробная схема первоначального назначения препаратов фемостон в пременопаузе (то есть до прекращения менструаций, но при наличии характерных климактерических симптомов). Пациенткам, у которых менструации не прекратились, рекомендуют начинать лечение в первый день менструального цикла. Пациенткам с нерегулярным менструальным циклом целесообразно начинать лечение после 10-14 дней монотерапии прогестагеном («химический кюретаж»).
Далее Вашему вниманию представлен алгоритм первоначального назначения препарата фемостон в постменопаузе (то есть когда уже прошел год и более после последней менструации).
Какой способ применения препаратов лучше?
Трансдермальное (накожное) нанесение позволяет избежать первой стадии печеночного метаболизма, благодаря чему колебания концентрации эстрадиола в плазме крови при применении накожных препаратов незначительны. Метаболизм и выведение эстрадиола при трансдермальном введении подобен метаболизму натуральных эстрогенов.
Большинству пациентов желательно использовать оптимальную и наиболее безопасную на сегодняшний день схему: Дивигель накожно + Утрожестан интравагинально.

Схема приема для женщин, у которых сохранена менструальная функция, назначается врачом. Обычно средство прописывают циклом с первого дня после окончания менструации (5 день цикла) в течение 25 дней, после овуляции (c 16 по 25 день цикла) нужно добавлять препараты гестагенов.
Утрожестан – содержит прогестерон микронизированный, существует в двух формах — 100 и 200 мг.
При МГТ в постменопаузе в непрерывном режиме препарат Утрожестан применяется в дозе 100 мг с первого дня приема эстрогенов.
При болях в молочной железе можно добавить прожестожель ежедневно по 1 дозе на каждую молочную железу 2-4 недели.
Противопоказаниями для заместительной гормонотерапии являются:
Нужен ли женщинам тестостерон?
Согласно рекомендациям Международного общества по менопаузе (International Menopause Society (IMS)) основное показание для применения тестостерона – лечение уменьшенного сексуального влечения, которое заставляет данную женщину испытывать значительные страдания. До рассмотрения вопроса о проведении терапии тестостероном необходимо решить вопросы, связанные с другими причинами нарушенного сексуального желания и/или возбуждения. К ним относятся диспареуния, депрессия, побочные эффекты лекарственных препаратов, проблемы взаимоотношений и другие проблемы со здоровьем, влияющие на женщину или ее партнера.
В настоящее время возможно применение трансдермальных препартов. На отечественном фармацевтическом рынке существует только один вариант – Андрогель, но его применение у женщин является «off-label», то есть не разрешено инструкцией. Обычно назначается 1/5 пакета в день (то есть 1 г геля/10 мг тестостерона).
Еще более перспективным может стать интравагинальная форма тестостерона, которая также может оказывать благоприятное действие при лечении вульвовагинальной атрофии.
Ключевые положения по применению препаратов тестостерона
Самые частые заблуждения:
А как же рак молочной железы, ведь это самая главная причина смерти у женщин?
В этом утверждении много заблуждений. На самом деле рак молочной железы – причина смертности в 4% случаев. Ведущая причина преждевременной смерти – сердечно-сосудистые заболевания (50%), которые запускает инсулинорезистентность. А она возникает на фоне гормональных нарушений.
Гормоны вызывают побочные эффекты и от них толстеют?
Новые низкодозированные и высокоселективные препараты направлены четко на мишень. Врачи на протяжении многих лет наблюдали за тысячами женщин, которые получали МГТ? Сегодня уже есть уникальные гестагены, метаболически нейтральные, они не приводят к ожирению и вместе с тем не понижают тестостерон, если у женщины нет его избытка. Выработаны и новые схемы лечения. Иногда при применении таблеток с эстрогенами, где-то в 10% случаев, бывают головные боли и боль в венах. В этом случае они заменяются на трансдермальные формы в виде геля.
Зачем мне принимать гормоны, если у меня нет приливов и отличное самочувствие?
Вместе с падением уровня гормонов возникает риск развития возрастных болезней: повышается артериальное давление, возникает ожирение, увеличивается риск развития сахарного диабета второго типа, подагры, остеопороза и онкологических заболеваний.
Вместо таблеток лучше принимать травы и различные фитоэстрогены?
Эффективность данных препаратов по устранению вазомоторных симптомов составляет 30%, что равно эффективности плацебо. При этом данная группа препаратов никаким образом не оказывает профилактического действия на возрастные заболевания (сердечно-сосудистые, онкологические заболевания, остеопороз, ожирение и сахарный диабет).
Дидрогестерон
Фармакологическое действие
Дидрогестерон — синтетический прогестаген. По своей молекулярной структуре, химическим и фармакологическим свойствам весьма близок к природному прогестерону. В связи с тем, что дидрогестерон не является производным тестостерона, он не обладает побочными эффектами, характерными для большинства синтетических прогестагенов, так называемых «андрогенных» прогестагенов. Дидрогестерон не обладает эстрогенной, андрогенной, анаболической, глюкокортикостероидной и термогенной активностью.
Выступая в роли прогестагенного компонента заместительной гормональной терапии в менопаузе, дидрогестерон способствует сохранению благоприятного действия эстрогенов на липидный профиль крови. Однако, в отличие от эстрогенов, которые обычно отрицательно влияют на систему свёртывания крови, дидрогестерон не оказывает влияния на показатели коагуляции. Не влияет отрицательно на метаболизм углеводов и функцию печени. Дидрогестерон при пероральном применении селективно воздействует на эндометрий, тем самым предотвращая повышенный риск развития гиперплазии эндометрия и/или карциногенеза в условиях избытка эстрогенов. Он показан во всех случаях эндогенной недостаточности прогестерона. Дидрогестерон не имеет контрацептивного действия. При лечении дидрогестероном терапевтический эффект достигается без подавления овуляции или нарушения менструальной функции. Дидрогестерон делает возможным зачатие и сохранение беременности во время лечения.
Фармакокинетика
После приёма внутрь, дидрогестерон быстро всасывается из желудочно-кишечного тракта. Максимальная плазменная концентрация (Cmax) достигается через 2 часа. Связывание с белками плазмы составляет 97 %.
Метаболизм в печени происходит путём гидроксилирования кетоновых групп 20-го углеродного атома. Наряду с этим наблюдалось также гидроксилирование метильных групп 21-го углеродного атома и в весьма незначительном объёме 16-альфа углеродного атома.
С мочой выводится от 56 % до 79 %; через 24 часа выводится примерно 85 %, через 72 часа процесс выведения практически заканчивается. Сведений о задержке или усилении действия дидрогестерона при ограниченной функции почек на сегодняшний день не поступало. Метаболиты обнаруживаются в моче преимущественно в виде конъюгатов глюкуроновой кислоты. Присутствия в моче неизменённого вещества не обнаружено.
Показания
Состояния, характеризующиеся дефицитом прогестерона:
Заместительная гормональная терапия:
Противопоказания
С осторожностью
При указаниях в анамнезе на кожный зуд при предшествующей беременности.
В настоящее время отсутствуют данные об отрицательном действии дидрогестерона при хронической почечной недостаточности.
Беременность и грудное вскармливание
Применение при беременности
Возможно применение дидрогестерона при беременности по показаниям.
Применение в период грудного вскармливания
Дидрогестерон выделяется с грудным молоком. Грудное вскармливание во время приёма препарата не рекомендуется.
Способ применения и дозы
Режим дозирования индивидуальный, в зависимости от показаний, клинической ситуации, схемы терапии и лекарственной формы.
Для приёма внутрь разовая доза составляет 5–10 мг, суточная доза — 10–30 мг, частота приёма 2–3 раза в сутки.
Побочные действия
Со стороны системы кроветворения
В единичных случаях — гемолитическая анемия.
Со стороны иммунной системы
В очень редких случаях — реакции гиперчувствительности.
Со стороны центральной нервной системы
Головная боль, мигрень.
Со стороны гепатобилиарной системы
Редко — незначительные нарушения функции печени, иногда сопровождающиеся слабостью или недомоганием, желтухой или болью в области живота.
Со стороны половой системы
В редких случаях — прорывные маточные кровотечения (которые можно предупредить повышением дозы); повышенная чувствительность молочных желёз.
Со стороны кожи и подкожной клетчатки
Аллергические реакции, такие как кожная сыпь, зуд, крапивница; очень редко — отёк Квинке.
Прочие
Очень редко — периферические отёки.
Передозировка
До настоящего времени о случаях передозировки дидрогестероном не сообщалось.
Лечение
При случайном приёме в дозе, значительно превышающей терапевтическую, рекомендуется промывание желудка. Специфического антидота нет, лечение должно быть симптоматическим.
Взаимодействие
Индукторы микросомальных ферментов печени (в том числе фенобарбитал, рифампицин) могут ускорять биотрансформацию дидрогестерона и ослаблять эффект.
Особые указания
Следует учитывать, что заместительная гормональная терапия не назначается без предварительного общего медицинского обследования, включая гинекологический осмотр.
Рекомендуется регулярное проведение маммографии.
Аномальные кровотечения и патологические изменения, выявленные при гинекологическом осмотре, могут служить показанием к исследованию эндометрия.
Влияние на способность к вождению автотранспорта и управлению механизмами
Не влияет на способность к управлению автомобилем и другими механизмами.