если пгд плохой что делать
ПГД при привычном невынашивании беременности
Нужно ли проводить эмбрионам ПГД, если беременность все-таки наступает? Рассказывает акушер-гинеколог, репродуктолог GMS ЭКО Юлия Кикина
Привычное невынашивание беременности — это потеря двух и более беременностей в паре. Наиболее частая причина этой проблемы — генетические аномалии эмбриона, иммунологические, эндокринные факторы, но не менее 50% всех потерь беременности попадают под понятие «неясного генеза», т. е. когда нет явных причин, которые могли бы вызвать выкидыш или замирание плода. У пациентов с диагнозом «привычное невынашивание неясного генеза» выявляется до 55% хромосомных нарушений у эмбриона.
Давайте попробуем решить для себя этот вопрос с позиций доказательной медицины и обратимся к результатам авторитетных исследований, которые показывают роль преимплантационного генетического скрининга для благополучного течения и завершения беременности вместе с акушер-гинекологом, репродуктологом GMS ЭКО Юлией Кикиной.
Делать или нет?
Группа американских и испанских ученых провела контролируемое исследование эффективности преимплантационного генетического скрининга методом CGH (генетическое исследование эмбриона по 24 хромосомам методом сравнительной геномной гибридизации). Частота имплантации у пациенток, которым была выполнена преимплантационная генетическая диагностика (ПГД), была достоверно выше в сравнении с контрольной группой (52,63 против 19,15%); частота наступления клинически подтвержденной беременности также выше: (69,2 против 43,91%). Частота возникновения развивающейся беременности была практически вдвое выше (61,54 и 32,49% соответственно), частота самопроизвольного выкидыша ниже (11,11 против 26%).
Ответ очевиден — ДА.
Когда следует делать обязательно?
Очень важный фактор для решения вопроса о необходимости проведения преимплантационной генетической диагностики в программе ЭКО у пары с привычным невынашиванием беременности — возраст женщины.
Исследователи выполнили 332 процедуры ПГД методом CGH у пар с привычной потерей беременности в анамнезе. У пациенток менее 38 лет у 62,6% эмбрионов выявлены хромосомные аномалии, в 80% циклов удалось отобрать эмбрионы без патологии для переноса. Частота наступления беременности составила 60%, частота имплантации — 47%, доля самопроизвольных абортов — 11,7%.
У женщин с невынашиванием беременности старше 38 лет число эмбрионов с анеуплоидным набором хромосом (аномальных) значительно выше (83,7%), эмбрионов без патологии у них удалось отобрать только в 56,4% циклов. При этом частота наступления беременности составила 53,2%, частота имплантации 50,3%, доля самопроизвольных абортов — 10%.
Чем старше женщина, тем важнее для нее проведение скрининга.
Таким образом, авторы пришли к выводу, что хромосомная аномалия — основная причина привычного невынашивания беременности неясной этиологии, и проведение преимплантационной генетической диагностики эмбрионов в программе ЭКО с применением современных технологий (CGH, NGS) повышает результативность лечения и уменьшает частоту самопроизвольных абортов.
В нашей клинике проводится лечение методом ЭКО с использованием современных методик преимплантационной генетической диагностики эмбрионов. Если у вас возникают вопросы, связанные с этой темой и не только, мы готовы на них ответить — пишите нам через электронную форму «Задать вопрос».
Использована литература: Гавард Дж. А. Карп «Привычное невынашивание беременности. Причины, версии, контраверсии, лечение». Пер. с англ. под ред. проф. Радзинского В. Е. ГЭОТАР, 2017.
Преимплантационный генетический анализ эмбрионов
Исследование проводится в рамках применения программы вспомогательной репродукции у пар, которые имеют высокий риск передачи генетических патологий или появления хромосомных нарушений у потомства. В результате в полость матки переносятся только эмбрионы, не имеющие аномалий в генетическом статусе.
История преимплантационной генетической диагностики (ПГД)
В норме генетический материал человека закодирован в 44 аутосомных хромосомах. Полный хромосомный набор представлен 22 соматическими парами и одной половой парой (у мальчиков ХУ, а у девочек ХХ). Однако нередки ситуации, когда количество хромосом может уменьшиться или, наоборот, увеличиться в результате сбоя в процессе деления клеток. Это приводит либо к рождению детей с хромосомными синдромами и множественными пороками развития, либо к подсадке нежизнеспособного эмбриона (такая беременность прерывается в первом триместре), либо к отсутствию имплантации. Чтобы снизить подобные неудачи ЭКО до этапа переноса эмбриона в маточную полость, было предложено проводить преимплантационную генетическую диагностику. Чуть позже выяснилось, что с помощью такой технологии можно также избежать передачи моногенного заболевания, носителем которого может оказаться один из родителей. Подсаживаться будут только те эмбрионы, в структуре которых нет этого аллеля.
Интересно отметить, что идея проведения подобного исследования зародилась еще до эры вспомогательных репродуктивных технологий у человека. Произошло это в 1967 году, когда ученые провели забор материала кроличьих эмбрионов, чтобы определить пол еще до подсадки. В репродуктивной медицине человека проведение генетического тестирования стало возможно с 90-х годов XX столетия, и связано с более широким распространением ЭКО и изобретением метода полимеразной цепной реакции.
Сначала в 1989 году перед имплантацией определили пол будущего ребенка. Для родителей это было важно, т.к. Х-хромосома одного из супругов содержала дефектный ген, и риск рождения больного ребенка был высок. В 1990 году уже удалось идентифицировать эмбрионы с моногенными нарушениями, в частности это касалось муковисцидоза. Позже ПГД шагнула еще дальше, предоставив возможность лечить больного брата или сестру с помощью пересадки костного мозга, свободного от мутации и полностью совместимого по системе HLA.
Как передаются по наследству генетические заболевания
Генетические заболевания, в отличие от хромосомных, связаны с изменением структуры генетического кода, когда один или несколько его участков являются патологическими. Подобные нарушения могут затрагивать как соматические хромосомы, так и половые. Стоит отметить, что мутантный аллель может быть доминирующим, то есть его влияние в паре всегда превалирует, или рецессивным, то есть патологический признак не проявится, если будет здоровый доминант. Этим определяются типы наследования генетических заболеваний. Хромосомный набор в норме всегда парный. Поэтому возможны следующие варианты:
Наследственные заболевания связаны со структурными изменениями наследственной информации клеток человека. Вероятность передачи «поломки» зависит от конкретного типа патологии, т.к. разные виды по-разному наследуются.
Типы наследования могут быть следующими:
Отнесение болезни к той или иной группе позволяет генетику предположить, с какой вероятностью она проявится у потомства и составить оптимальный репродуктивный план для пары.
Доминантные заболевания
В случае доминантного наследования патологический признак превалирует над здоровым. Поэтому при его наличии (хоть в одной, хоть в 2 хромосомах) ребенок всегда болен. Здоровые дети не являются носителями мутантного аллеля.
По аутосомно-доминантному типу наследуются болезнь Марфана (поражение соединительной ткани), боковой амиотрофический склероз (поражение структур спинного мозга), нейрофиброматоз (из нервной ткани образуются опухоли), семейная гиперхолестеринемия и др.
Рецессивные заболевания
При рецессивном типе наследования заболевание проявляется только в том случае, если патологический участок присутствует одновременно в 2 хромосомах из пары. Здоровые дети от больных родителей могут быть как носителями патологического гена (одна из хромосом имеет повреждение), так и не иметь его в своем наборе (2 хромосомы в паре абсолютно нормальны).
Рецессивный тип передачи наследственного заболевания часто встречается при близкородственных браках. Основными представителями этой группы являются анемия Фанкони, лизосомные болезни накопления, фенилкетонурия, синдром Жильбера, наследственная тугоухость и другие.
Для генетики справедливо правило – если у двух здоровых родителей ребенок болен, то такой тип наследования считается рецессивным.
Х-сцепленные заболевания
Чаще всего в популяции встречаются Х-сцепленные заболевания, намного реже – У-сцепленные. В последнем случае патологический признак выявляется только у мужчин и передается по мужской линии всем сыновьям.
Х-сцепленное наследование может быть доминантным и рецессивным.
Возможные преимущества генетического анализа
Что значит ПГД эмбриона? Это высокотехнологичное исследование помогает решать сразу несколько важных задач, связанных с улучшением репродуктивных и медико-генетических исходов беременности. Благодаря генетическому анализу, удается достигать следующих целей:
В результате проведения ПГД снижается риск рождения больного ребенка, риск невынашивания и многоплодия, увеличиваются шансы на успешную имплантацию (в среднем на 10%) и на благополучное рождение ребенка (примерно на 15-20%).
Что дает ПГД эмбриона еще? Если брат или сестра от одних родителей имеют заболевание, связанное с мутацией, требующее пересадки костного мозга, и в базе данных подобрать совместимого донора не удается, то на помощь приходит ЭКО с преимплантационным скринингом. Что показывает ПГД в этом случае? Благодаря этому исследованию удается подобрать эмбрион, который не только не содержит мутации, но и полностью совместим по тканевым антигенам. Такое направление в терапии применяется в США и Европе уже более 15 лет, а в России с 2016 года, когда девочке с синдромом Шахванда-Даймонда пересадили здоровые стволовые клетки от ее родного брата, зачатого путем ЭКО.
Показания к преимплантационной генетической диагностике
Метод ПГД в первую очередь предназначен для выявления количественных нарушений в хромосомном наборе эмбриона, которые не являются летальными, но могут приводить к рождению ребенка с пороками развития. Это касается 13,18, 21-й пары аутосом и половых хромосом – Х- и У.
К тому же, некоторые хромосомные аномалии являются летальными, то есть несовместимыми с жизнью. Клинически это проявляется самопроизвольными выкидышами на ранних сроках беременности. Частота их по причине хромосомных аномалий в первом триместре доходит до 60%. Поэтому чтобы вам подсадили наиболее качественный эмбрион (без генетических поломок), и проводится ПГД.
Что показывает ПГД эмбриона еще? Это исследование позволяет также идентифицировать носительство конкретных мутантных аллелей и выбрать для подсадки здоровые эмбрионы, которые лишены патологического гена.
Таким образом, ПГД работает и в отношении выявления хромосомных синдромов, и в отношении генетических заболеваний.
Кому показано ПГД
Европейское общество репродуктологов и эмбриологов рекомендует проводить преимплантационный тест при наличии следующих показаний:
Помимо этого ПГД эмбриона при ЭКО рекомендуется женщинам со сниженным овариальным резервом. Уменьшение численности фолликулов в яичниках практически всегда ассоциировано с плохим качеством яйцеклеток, в которых увеличивается риск спонтанных мутаций. Поэтому чтобы подсадить в полость матки здоровый эмбрион, проводится преимплантационный скрининг. Это же исследование показано также парам, у которых в анамнезе были случаи пузырного заноса, неразвивающейся и биохимической (уровень ХГЧ был повышен, но дальше гестационный процесс прервался на очень раннем сроке) беременности.
Состояния, диагностируемые с помощью ПГД
Анализ ПГД эмбриона – что это? Данное исследование позволяет провести генетическое изучение эмбрионов на нулевые сутки, 3-и или 5-ые. С помощью этого теста выявляют различные хромосомные аномалии еще до подсадки эмбриона в полость матки для того, чтобы предотвратить рождение ребенка с генетическими отклонениями и наследственными заболеваниями.
ПГД эмбриона позволяет объективно диагностировать носительство конкретных генетических патологий. В свою очередь преимплантационный генетический скрининг в медицине репродукции направлен на выявление общих изменений количества хромосом (увеличение или уменьшение).
Условно все нарушения в строении генетического аппарата будущего ребенка можно разделить на 3 категории:
Заболевания, сцепленные с полом
Практически все заболевания, которые сцеплены с полом, наследуются через патологически измененную Х-хромосому. Поэтому женщины могут быть как больными, так и здоровыми носителями. Мужчины всегда проявляют заболевание. Патологии, сцепленные с полом, возникают при наличии мутаций в половых хромосомах родительских организмов и связаны с нарушением генетических процессов.
Наиболее распространенными патологиями этой группы являются:
Одиночные дефекты гена
Одиночные дефекты гена могут приводить к развитию моногенных заболеваний у потомства. Благодаря ПГД удается подсадить эмбрион, который не имеет соответствующей мутации. Так наследуются:
Хромосомные расстройства
Хромосомные заболевания не зависят от генетического аппарата родителей, а возникают при нарушениях расхождения хромосом в процессе мейотического деления.
Наиболее частые хромосомные заболевания, связанные с изменением численности хромосом, это:
Кандидаты для биопсии эмбриона и ПГД
Биопсия эмбриона и преимплантационное генетическое тестирование проводится в тех ситуациях, когда риск хромосомных и генных нарушений достаточно высок. В первую очередь это определяется возрастом родителей. Задуматься о возможных генетических поломках стоит женщинам старше 35 лет и мужчинам старше 40 лет. Помимо этого есть определенные клинические ситуации, когда повышена вероятность генетических нарушений. Последние могут быть причиной привычного невынашивания беременности, многократных неудачных попыток ЭКО. ПГД рекомендуется и в тех случаях, когда имеется мужское бесплодие, связанное с хромосомными аномалиями, или же кто-то из потенциальных родителей имеет доказанное носительство хромосомных перестроек, транслокаций, инверсий и других хромосомных патологий.
Пары с повторными неудачами ЭКО
Повторные неудачи ЭКО нередко связаны с наличием генетических аномалий у эмбриона/плода. Преимплантационная диагностика позволяет отбирать только здоровые эмбрионы. Это в разы повышает результативность цикла ЭКО, снижает вероятность рождения ребенка с хромосомными аномалиями, а также риск спонтанных прерываний беременности.
Используемые методы
Как делают ПГД эмбриона? Состояние будущего плода изучают в самые ранние сроки его развития. Материалом для исследования могут служить полярные тельца, бластомеры и клетки трофэктодермы. Оптимальным вариантом является исследование трофэктодермы, т.к. это самый малотравматичный вариант биопсии, а биопсийный материал, который получают на 5-е сутки, наиболее информативен. Генетику удается получить большее количество эмбриональных клеток, а значит, и большее количество копий ДНК. В рамках тестах изучается последовательность нуклеиновых кислот.
Раньше изучались единичные хромосомы. Как правило, те, в которых чаще всего встречаются проблемы. На сегодня микроматричная сравнительная геномная гибридизация позволяет исследовать все пары хромосом (как соматические, так и половые).
Репродуктивный центр «СМ-Клиника» располагает необходимым оборудованием и квалифицированными специалистами для проведения ПГД в соответствии с рекомендациями международного общества репродуктологов.
ПГД, заблуждения и факты
Врачи говорят одно, друзья и семья другое, а доктор Гугл имеет свое особое мнение. В век переизбытка информации — когда экспертом является каждый — порой бывает трудно отделить факты от вымысла.
Это особенно верно, когда речь заходит о лечении бесплодия.
Женщины, сталкивающиеся с этой проблемой, вынуждены искать доказательства, искать правду среди противоречивых советов и развенчивать неверные представления в попытке найти среди всех возможностей именно то, что им подходит.
Генетический скрининг возглавляет список наиболее широко обсуждаемых и неправильно понимаемых опций при лечении бесплодия.
Преимплантационный генетический скрининг (PGS) и преимплантационная генетическая диагностика (PGD) — этапы процедуры экстракорпорального оплодотворения (ЭКО), направленные на увеличение шансов имплантации «здоровых» эмбрионов. PGS выявляет лишние либо недостающие хромосомы у эмбриона, тогда как с помощью PGD выявляются дефекты генов, которые могут привести к развитию моногенных заболеваний.
Давайте рассмотрим пять наиболее частых заблуждений о PGS и PGD
ЗАБЛУЖДЕНИЕ 1
PGS ПРЕДНАЗНАЧЕН ДЛЯ ЖЕНЩИН СТАРШЕГО РЕПРОДУКТИВНОГО ВОЗРАСТА
Легко понять, почему большинство людей считает, что PGS создан исключительно для женщин старшего репродуктивного возраста. С одной стороны верно, что с повышением возраста повышается риск хромосомных аномалий, однако многие заблуждаются, считая что более молодые женщины вне зоны риска.
Факт: риску хромосомной аномалии эмбрионов подвержены женщины всех возрастов, даже до 30 лет. Для последних такой риск составляет до 30 % для эмбрионов 5-х суток развития.
ЗАБЛУЖДЕНИЕ 2
PGS ТОЛЬКО ДЛЯ ВЫЯВЛЕНИЯ ХРОМОСОМНЫХ АНОМАЛИЙ
Никто не отрицает, что PGS обеспечивает бесплодные пары ценной информацией о генетическом статусе эмбрионов. Проведение поиска хромосомных аномалий позволяет парам подготовится к таким отклонениям, как синдром Дауна.
Пары, подверженные повышенному риску хромосомных аномалий, являются идеальными кандидатами для PGS, так же как и пары с привычным невынашиванием беременности или с множественными неудачными попытками ЭКО в анамнезе, ищущие ответ на вопрос «почему?»
Факт: Преимплантационный генетический скрининг так же может помочь бесплодным парам понять причину их бесплодия. Множество людей до проведения скрининга не знают причины почему их эмбрионы либо совсем не имплантируются, либо прекращают развиваться на определенной стадии. PGS также зачастую помогает определить причину необъяснимого бесплодия. Некоторые полагают, что PGS пользуют для селекции пола, однако большинство клиник ЭКО не сообщают пол перенесенного эмбриона до наступления беременности.
ЗАБЛУЖДЕНИЕ 3
PGD — ЭТО «ИГРА В БОГА»
Преимплантационная генетическая диагностика, по мнению многих, противоречивая процедура. PGD проводится в цикле ЭКО для выявления дефектов единичных генов, которые могут привести к генетическим заболеваниям.
Проводя такую диагностику пары, являющиеся носителями наследственных заболеваний или сами страдающие от таких заболеваний, могут избежать или существенно снизить риск того, что их дети унаследуют данное заболевание — вот почему многие называют PGD «игрой в Бога».
Факт: ничто нельзя подразделять на черное и белое, когда речь идет о вопросах веры и нравственности. Однако следует понимать, что подобным образом можно осуждать и обсуждать многие другие медицинские технологии, вошедшие сегодня в повседневную практику, такие как профилактический прием препаратов, кесарево сечение или искусственная вентиляция легких, которые направлены на снижение смертности или улучшение качества жизни.
ЗАБЛУЖДЕНИЕ 4
PGD РЕКОМЕНДОВАНА ВСЕМ НОСИТЕЛЯМ МОНОГЕННЫХ ЗАБОЛЕВАНИЙ
Для людей, имеющих семейную историю наследственных моногенных заболеваний, таких как муковисцидоз или гемофилия, PGD является очевидным решением. Однако PGD показана далеко не всем.
Факт. Большинство пар находятся вне зоны риска развития моногенных заболеваний. Каждый из нас может являться носителем от 4 до 6 различных аутосомно-рецессивных моногенных заболеваний, но для того, чтобы болезнь проявилась у потомства, оба партнера должны иметь поломки (мутации) в одном и том же гене. Определить статус носительства наиболее частых моногенных заболеваний на сегодняшний день совсем не сложно, для этого достаточно провести молекулярно-генетическое исследование.
ЗАБЛУЖДЕНИЕ 5
ПРИ ПЕРЕНОСЕ ЭМБРИОНОВ НИЗКОГО КАЧЕСТВА БЕРЕМЕННОСТЬ НЕ НАСТУПАЕТ
В клиниках ЭКО принято проводить оценку полученных эмбрионов, исходя из морфологических критериев (внешняя оценка). Очевидно, что когда дело доходит до переноса, первыми кандидатами являются эмбрионы класса «А», но не стоит забывать, что и при переносе эмбрионов более низкого качества так же возможно наступление беременности.
Факт: Внешний вид эмбриона и его хромосомный набор зачастую не коррелируют друг с другом. После проведение PGS зачастую оказывается, что «здоровые» эмбрионы не всегда самые красивые, и если бы диагностика не проводилась, то такой эмбрион вряд ли был выбран для переноса. Именно поэтому одним из показаний к проведению PGS является отсутствие наступления беременности в 2-х и более попытках ЭКО при переносе эмбрионов хорошего качества, при условии, что другие проблемы решены.
ПГТ: как повысить шансы на успех ЭКО?
Генетическая диагностика эмбрионов улучшает результативность ЭКО.
Несмотря на высокую эффективность современных программ ВРТ, многие пары сталкиваются с многочисленными неудачными попытками. Перенос морфологически качественного эмбриона не всегда приводит к имплантации, а наступившая беременность в ряде случаев прекращает развиваться на ранних сроках.
Поэтому перед вступлением в протокол паре рекомендована консультация врача генетика. На консультации генетик может рекомендовать паре сделать преимплантационное генетическое тестирование эмбриона. Что это такое? Какие показания к процедуре, какие болезни выявляет ПГТ и насколько повышаются шансы на успех ЭКО после ПГТ?

К сожалению, многие пациенты, столкнувшиеся с безрезультатными попытками ЭКО, замершими беременностями, отклонениями в кариотипе, воспринимают эти неудачи как приговор и опускают руки. Но в современноймедицине есть эффективные способы, позволяющие обойти сложности при генетических нарушениях.
Преимплантационное генетическое тестирование (ПГТ) позволяет обследовать эмбрионы до имплантации в полость матки и выбрать именно тот, который не имеет генетических нарушений.
Преимплантационное генетическое тестирование дает возможность перенести в матку здоровые эмбрионы, снизить риск выкидыша и замершей беременности. В большинстве случаев использование данной технологии не только сокращает количество переносов, но и значительно приближает долгожданную встречу с малышом.
Будущим родителям важно знать, что ПГТ безопасно для будущего ребенка и никак не отражается на дальнейшем его развитии.
Какие генетические нарушения можно выявить с помощью ПГТ?
ПГТ-А – скрининг анеуплоидий. Позволяет выявить патологии плода, связанные с уменьшением или увеличением числа хромосом, определить эмбрион с хромосомным нарушением, которое в большинстве случаев является причиной замершей беременности. ПГТ-А позволяет исключить возможность беременности жизнеспособным плодом, имплантация и дальнейшее развитие которого может привести к рождению детей с хромосомными болезнями (синдром Дауна, синдром Патау, синдром Эдвардса), а также синдромами, связанными с нарушением количества половых хромосом (синдром Клайнфельтера, синдром Шерешевского-Тернера).
ПГТ- М – скрининг моногенных заболеваний. ПГТ-М выявляет такие генетические патологии, как муковисцидоз, фенилкетонурия, синдром Марфана, миотония Томсена/Беккера, немалиновая миопатия и др. ПГТ-М позволяет выбрать для переноса эмбрион, не отягощенный наследственными заболеваниями.
ПГТ на определение резус-фактора эмбриона выполняется тогда, когда есть высокий риск резус-конфликта и гемолитической болезни плода.
Каковы показания к применению ПГТ?
Какова результативность ПГТ?
Что касается повышения результативности ЭКО, то доля эмбрионов, перенос которых привел к рождению ребенка в циклах ВРТ без ПГ, составляет около40 %, в то время как ПГТ увеличивает этот показатель до 60-70 %.
Анна Владимировна Быстрякова – консультант портала Пробирка. Задать А.В. Быстряковой все интересующие вас вопросы по генетике вы можете в рубрике «Спроси генетика» на форуме Пробирки.
Для получения бесплатной консультации генетика А.В. Быстряковой он-лайн выберите свой город.
Преимплантационный генетический анализ эмбрионов
Каждая из 100 триллионов клеток в организме человека (за исключением красных кровяных клеток) содержит весь человеческий геном. Хромосомы – это струноподобные элементы внутри ядра (в центре) каждой клетки вашего тела. Они содержат генетическую информацию, ДНК. Ген занимает определенное место на хромосоме. В норме, есть 23 идентичных пары хромосом (2 метра ДНК) в каждой клетке, в общей сложности 46 хромосом. Каждый партнер во время оплодотворения обычно предоставляет 23 хромосомы. Если яйцеклетка или сперматозоид имеют аномальную упаковку хромосом, эмбрион, который они создают, также будет иметь хромосомные аномалии. Иногда это связано с перестройкой хромосом, или недостатком части хромосомы. В некоторых случаях есть отсутствующие хромосомы, или дополнительная хромосома (анеуплоидии), ведущие к наследственным заболеваниям. Любой эмбрион, в котором отсутствует хромосома (моносомия) перестанет расти до имплантации (фатальная аномалия). Если анеуплоидии включают хромосомы 13, 18, 21, Х или Y, беременность может дойти до родов. Наиболее распространенной из этих несмертельных аномалий является трисомия 21, или синдром Дауна, при которой присутствует дополнительная 21-я хромосома. Другие включают синдром Тернера у женщин и синдром Клайнфельтера у мужчин.
История преимплантационной генетической диагностики (ПГД)
Первые живорождения после ПГД были зарегистрированы в Лондоне в 1989 году. Две двойни девочек-близнецов родились от пяти пар с риском передачи связанного с Х-хромосомой заболевания. В настоящее время с помощью методов генетического анализа или ПГД могут быть обнаружены около 90% аномальных эмбрионов. Не все хромосомные или генетические заболевания могут быть определены этими процедурами, так как в ходе одной процедуры может быть диагностировано только ограниченное число хромосом. Многочисленные исследования на животных и некоторые исследования на человеке показывают, что микрохирургия эмбриона (биопсия), необходимая для удаления клеток, не влияет на нормальное развитие ребенка. Эта процедура, однако, была выполнена относительно небольшому числу пациентов во всем мире, поэтому точные негативные последствия, если таковые имеются, неизвестны. Несмотря на то, что после генетического анализа для выявления анеуплоидии всем мире на сегодняшний день было рождено уже много детей, эта процедура все еще относительно нова. В исследованиях на животных не было обнаружено никаких очевидных проблем и предварительные данные с эмбрионами человека позволяют предположить справедливость этого вывода. В исследовании, проведенном в Университетском колледже Лондона, исследователи недавно рассмотрели 12 преимплантационных эмбрионов с новой техникой, которая сочетает в себе амплификацию всего генома (WGA) и сравнительную гибридизацию генома (CGH). В результате в 8 из 12 изученных эмбрионов были обнаружены значительные хромосомные аномалии. Это может объяснить, почему люди имеют в лучшем случае 25% шансов на достижение жизнеспособной беременности в месяц при естественном зачатии.
Как передаются по наследству генетические заболевания
В диаграммах ниже, D или d представляет дефектный ген, а N или n представляет нормальный ген. Мутации не всегда приводят к болезни.
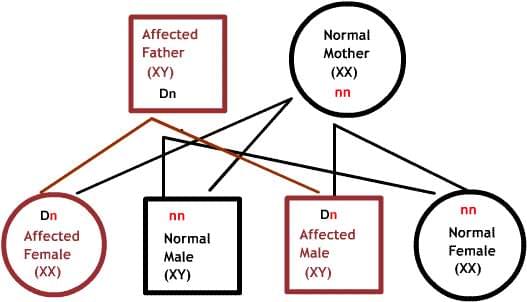
Доминантные заболевания:
Один из родителей имеет один дефектный ген, который доминирует над своей нормальной парой. Так как потомки наследуют половину своего генетического материала от каждого из родителей, есть 50% риск наследования дефектного гена, и, следовательно, заболевания.
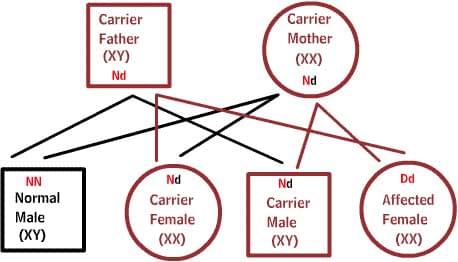
Рецессивные заболевания:
Оба родителя являются носителями одного дефектного гена, но при этом имеют нормальную пару гена. Для наследования заболевания необходимы две дефектных копии гена. Каждый потомок имеет 50% шанс быть носителем, и 25% шанс унаследовать заболевание.
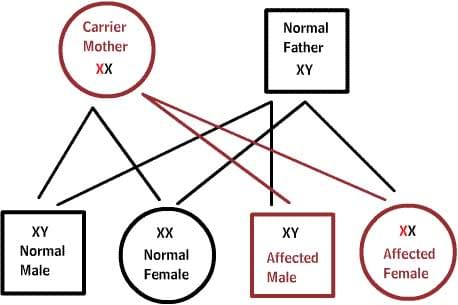
X-сцепленные заболевания:
Нормальные женщины имеют XX хромосомы, а нормальные мужчины XY. Женщины, которые имеют нормальный ген на одной из Х-хромосом, защищены от дефектного гена на их другой Х-хромосоме. Однако, у мужчины отсутствует такая защита в связи с наличием только одной Х-хромосомы. Каждый мужской потомок от матери, которая несет в себе дефект, имеет 50% шанс унаследовать дефектный ген и заболевание. Каждый женский потомок имеет 50% шанс быть носителем, как и ее мать. (на рисунке ниже X представляет нормальный ген а X представляет дефектный ген)
Возможные преимущества генетического анализа
Преимплантационная генетическая диагностика позволяет отобрать и перенести не измененные (хромосомно нормальные) эмбрионы, которые могут привести к большей частоте имплантации на эмбрион, сокращению потерь беременности и рождению большего числа здоровых детей. Генетическая диагностика предлагает парам альтернативу мучительному выбору по поводу того, чтобы прервать пострадавшую беременность после пренатальной диагностики, производимой путем амниоцентеза или биопсии ворсин хориона (CVS) на более поздних стадиях беременности. Почти все генетически связанные заболевания, которые могут быть диагностированы в перинатальном периоде либо амниоцентезом или CVS, могут быть обнаружены и ПГД. Процедура должна уменьшить психологическую травму для пар, которые несут повышенный риск генетических заболеваний для потомства.
Преимущества преимплантационной генетической диагностики (ПГД) могут включать в себя:
Возможные риски генетического анализа
Кандидаты для биопсии эмбриона и ПГД
Кандидаты для биопсии эмбриона и ПГД включают в себя:
Пары с повторными неудачами ЭКО.
Используемые методы
Для анализа на наличие генетических дефектов эмбриона, из него необходимо удалить либо первое полярное тельце из неоплодотворенной яйцеклетки и/или 1 или 2 клетки от каждого эмбриона. Это называется биопсией яйцеклетки или эмбриона и обычно делается перед тем, как происходит оплодотворение, или через 3 дня после оплодотворения. Биопсия на 6-10 клеточной стадии не оказывает отрицательного влияния на преимплантационное развитие. На этом этапе каждая клетка имеет полный набор хромосом. Обычно из эмбриона удаляется только одна клетка, так как ожидается, что будут одинаковыми со всеми другими клетками в эмбрионе. Иногда необходимо удалить вторую клетку из эмбриона, например, если сигнал в первой не обнаружен. Для диагноза предрасположенности с помощью первого и второго полярных телец, как показателей генетического статуса яйцеклетки, используется анализ методом FISH. Недостатком анализа полярных телец заключается в том, что он не принимает во внимание отцовские анеуплоидии.
Анализ биопсированной клетки использует один из двух методов:
Вся информация носит ознакомительный характер. Если у вас возникли проблемы со здоровьем, то необходима консультация специалиста.