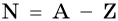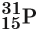Как сделать строение атома химия
Строение атома. Строение электронных оболочек атомов первых 20 элементов Периодической системы Д.И. Менделеева
Атом — электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов. В центре атома находится положительно заряженное ядро. Оно занимает ничтожную часть пространства внутри атома, в нём сосредоточены весь положительный заряд и почти вся масса атома.
Ядро состоит из элементарных частиц — протона и нейтрона; вокруг атомного ядра по замкнутым орбиталям движутся электроны.
Протон (р) — элементарная частица с относительной массой 1,00728 атомной единицы массы и зарядом +1 условную единицу. Число протонов в атомном ядре равно порядковому номеру элемента в Периодической системе Д.И. Менделеева.
Нейтрон (n) — элементарная нейтральная частица с относительной массой 1,00866 атомной единицы массы (а. е. м.).
Число нейтронов в ядре N определяют по формуле:
где А — массовое число, Z — заряд ядра, равный числу протонов (порядковому номеру).
Обычно параметры ядра атома записывают следующим образом: слева внизу от символа элемента ставят заряд ядра, а вверху — массовое число, например:
Эта запись показывает, что заряд ядра (следовательно, и число протонов) для атома фосфора равен 15, массовое число равно 31, а число нейтронов равно 31 – 15 = 16. Так как массы протона и нейтрона очень мало отличаются друг от друга, то массовое число приблизительно равно относительной атомной массе ядра.
Электрон ( е – ) — элементарная частица с массой 0,00055 а. е. м. и условным зарядом –1. Число электронов в атоме равно заряду ядра атома (порядковому номеру элемента в Периодической системе Д.И. Менделеева).
Электроны движутся вокруг ядра по строго определённым орбиталям, образуя так называемое электронное облако.
Область пространства вокруг атомного ядра, где наиболее (90 и более %) вероятно нахождение электрона, определяет форму электронного облака.
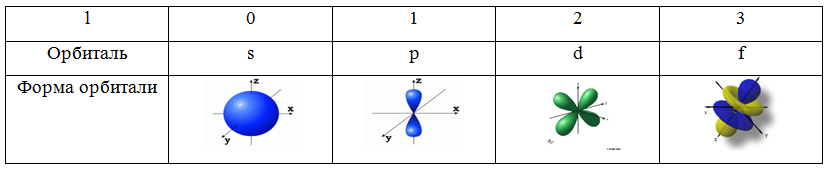
Электронное облако s-электрона имеет сферическую форму; на s-энергетическом подуровне может максимально находиться два электрона.
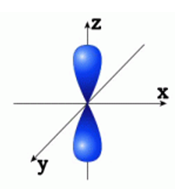
Электронное облако p-электрона имеет гантелеобразную форму; на трёх p-орбиталях максимально может находиться шесть электронов.
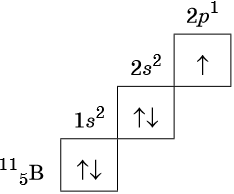
Орбитали изображают в виде квадрата, сверху или снизу которого пишут значения главного и побочного квантовых чисел, описывающих данную орбиталь. Такую запись называют графической электронной формулой, например:
В этой формуле стрелками обозначают электрон, а направление стрелки соответствует направлению спина — собственного магнитного момента электрона. Электроны с противоположными спинами ↑↓ называют спаренными.
Электронные конфигурации атомов элементов можно представить в виде электронных формул, в которых указывают символы подуровня, коэффициент перед символом подуровня показывает его принадлежность к данному уровню, а степень у символа — число электронов данного подуровня.
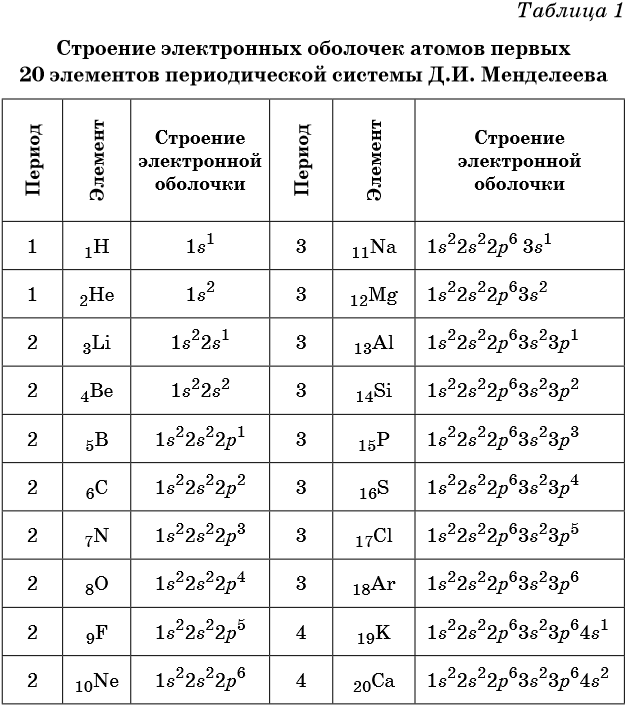
В таблице 1 приведено строение электронных оболочек атомов первых 20 элементов Периодической системы химических элементов Д.И. Менделеева.
Химические элементы, в атомах которых s-подуровень внешнего уровня пополняется одним или двумя электронами, называют s-элементами. Химические элементы, в атомах которых заполняется p-подуровень (от одного до шести электронов), называют p-элементами.
Число электронных слоёв в атоме химического элемента равно номеру периода.
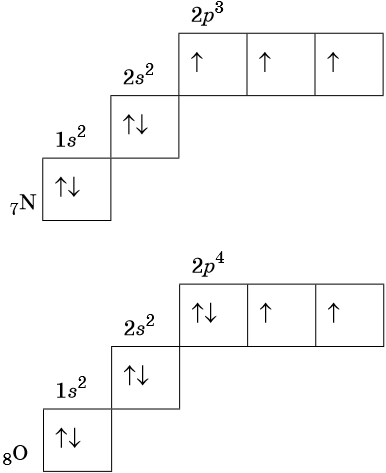
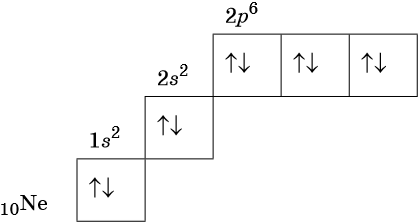
В соответствии с правилом Хунда электроны располагаются на однотипных орбиталях одного энергетического уровня таким образом, чтобы суммарный спин был максимален. Следовательно, при заполнении энергетического подуровня каждый электрон прежде всего занимает отдельную ячейку, а только после этого начинается их спаривание. Например, у атома азота все p-электроны будут находиться в отдельных ячейках, а у кислорода начнётся их спаривание, которое полностью закончится у неона.
Изотопами называют атомы одного и того же элемента, содержащие в своих ядрах одинаковое число протонов, но различное число нейтронов.
Изотопы известны для всех элементов. Поэтому атомные массы элементов в периодической системе являются средним значением из массовых чисел природных смесей изотопов и отличаются от целочисленных значений. Таким образом, атомная масса природной смеси изотопов не может служить главной характеристикой атома, а следовательно, и элемента. Такой характеристикой атома является заряд ядра, определяющий число электронов в электронной оболочке атома и её строение.
Рассмотрим несколько типовых заданий по этому разделу.
На внешнем энергетическом уровне у данного элемента находится один 4s-электрон. Следовательно, этот химический элемент находится в четвёртом периоде первой группе главной подгруппе. Этот элемент — калий.
К этому ответу можно прийти по-другому. Сложив общее количество всех электронов, получим 19. Общее число электронов равно порядковому номеру элемента. Под номером 19 в периодической системе находится калий.
Пример 2. Химическому элементу соответствует высший оксид RO2. Электронной конфигурации внешнего энергетического уровня атома этого элемента соответствует электронная формула:
По формуле высшего оксида (смотрите на формулы высших оксидов в Периодической системе) устанавливаем, что этот химический элемент находится в четвёртой группе главной подгруппы. У этих элементов на внешнем энергетическом уровне находятся четыре электрона — два s и два p. Следовательно, правильный ответ 2.
Тренировочные задания
1. Общее число s-электронов в атоме кальция равно
2. Число спаренных p-электронов в атоме азота равно
3. Число неспаренных s-электронов в атоме азота равно
4. Число электронов на внешнем энергетическом уровне атома аргона равно
5. Число протонов, нейтронов и электронов в атоме 9 4Be равно
1) 9, 4, 5
2) 4, 5, 4
3) 4, 4, 5
4) 9, 5, 9
6. Распределение электронов по электронным слоям 2; 8; 4 — соответствует атому, расположенному в(во)
1) 3-м периоде, IА группе
2) 2-м периоде, IVА группе
3) 3-м периоде, IVА группе
4) 3-м периоде, VА группе
7. Химическому элементу, расположенному в 3-м периоде VA группе соответствует схема электронного строения атома
1) 2, 8, 6
2) 2, 6, 4
3) 2, 8, 5
4) 2, 8, 2
8. Химический элемент с электронной конфигурацией 1s 2 2s 2 2p 4 образует летучее водородное соединение, формула которого
9. Число электронных слоёв в атоме химического элемента равно
1) его порядковому номеру
2) номеру группы
3) числу нейтронов в ядре
4) номеру периода
10. Число внешних электронов в атомах химических элементов главных подгрупп равно
1) порядковому номеру элемента
2) номеру группы
3) числу нейтронов в ядре
4) номеру периода
11. Два электрона находятся во внешнем электронном слое атомов каждого из химических элементов в ряду
1) He, Be, Ba
2) Mg, Si, O
3) C, Mg, Ca
4) Ba, Sr, B
13. Число электронных слоев и число p-электронов в атоме серы равно
1) 2, 6
2) 3, 4
3) 3, 16
4) 3, 10
14. Электронная конфигурация ns 2 np 4 соответствует атому
1) хлора
2) серы
3) магния
4) кремния
15. Валентные электроны атома натрия в основном состоянии находятся на энергетическом подуровне
1) 2s
2) 2p
3) 3s
4) 3p
16. Атомы азота и фосфора имеют
1) одинаковое число нейтронов
2) одинаковое число протонов
3) одинаковую конфигурацию внешнего электронного слоя
4) одинаковое число электронов
17. Одинаковое число валентных электронов имеют атомы кальция и
1) калия
2) алюминия
3) бериллия
4) бора
18. Атомы углерода и фтора имеют
1) одинаковое число нейтронов
2) одинаковое число протонов
3) одинаковое число электронных слоёв
4) одинаковое число электронов
19. У атома углерода в основном состоянии число неспаренных электронов равно
20. В атоме кислорода в основном состоянии число спаренных электронов равно
Химия
Именная карта банка для детей
с крутым дизайном, +200 бонусов
Закажи свою собственную карту банка и получи бонусы
План урока:
Строение атома
Сегодня мы будем путешествовать в микромир – мир атома. Даже если превратить нас в песчинку, то по сравнению с размером ядра атомов химических элементов, мы будем гигантами.
Атом нельзя увидеть, невозможно потрогать, он на столько мал, что существует только в нашем воображении. До XIX века учёные оперировали только одной характеристикой атома – это его масса. Наука не оперировала понятиями, что ядро атома содержит более мелкие частицы. Почему элементы отличаются массой. Атом долгое время считали «неделимым». Но отличия в массе подвигли искать причину в строении.
Как описать строение, то чего невозможно увидеть, а можно только представить. Ведь современные электронные микроскопы появились только в XX веке.
Атом – как мельчайшая частица, известна ещё с древних времён. Древнегреческий философ Демокрит считал, что свойства веществ определяются определённым типом атома. Даже тонкая материя, душа, по его мнению, состоит из атомов. Так тела бывают в разных агрегатных состояниях, поэтому атомы металлов будут с зубцами, жидкости будут обладать гладкими, это будет причиной их текучести.
Долгое время атом считали неделимым. Заглянув в словарь синонимов, можно увидеть пару синонимов для слова атом, неделимый, мельчайшая частица. Теория о неделимости существовала до XIX века, пока экспериментально не подтвердили, что ядро атома состоит из более мелких частиц. Но как они располагаются в атоме, как конфеты драже в кармашке, или по версии Томсона, который сравнивал электроны с изюминками, хаотично разбросанных в кексе. Учёный с Японии Хантаро Нагаока сравнил атом с загадочной планетой Сатурн, которая известна своим кольцом. Саму планету он сравнил с массивным ядром, а роль кольца отдал электронам.
В конце XIX века, начале XX происходит стремительное развитие науки, открываются новые частицы α и β. Позже было установлено, что это ядро атома элемента Не и электроны.
В ходе данных исследований было доказано, что атом представляет совокупность заряженных и нейтральных частичек.
Анализируя размеры, важно запомнить, что радиус ядра атома, будет всегда значительно меньше радиуса всего атома. Этот факт объясняется тем, что частицы составляющие ядро более компактно упакованы, чем электроны.
Ядро атома
Орешки фундука явно вы видели. В середине ореха находится большое ядро, занимающее почти всю массу ореха, оставляя малое пространство между скорлупой.
Ядро атома элемента имеет в составе протоны и нейтроны, которые принято называть нуклонами.
Данные частицы не относятся к элементарным, научно доказано, что они состоят с кварков (в словарь). Нейтроны в ядре атома не несут никакого заряда, они нейтральны. Протоны в ядре атома определяют его заряд.
Сумма протонов и нейтронов составляет массовое число ядра атома (нуклонное).
Вы наверняка замечали, что значение Ar в ПСХЭ имеет вид не целого числа, с чем это связано? Причина кроется в том, что химические элементы существуют в виде изотопов.
Чтобы понять суть этого понятия, давайте вспомним, чем особенный каждый элемент? Заряд ядра атома постоянен, другими словами, неизменимое количество протонов. Значит, это будет разновидность элементов, которые будут отличаться нуклонным числом, и как следствие, количеством нейтронов.
Именно по причине существования изотопов, Ar не имеет целого числового значения. Например, количество изотопов хлора – 2.
Масса изотопов и их процентное содержание составляют относительную массу элемента.
Возможно, вы ранее замечали, что в ПСХЭ есть пара элементов, которые нарушают порядок размещения по увеличению относительной атомной массы. Это пары K – Ar, Co – Ni, Te – I.
Некоторые изотопы отличаются особенной способностью самовольно превращаться в другие элементы – это явление носит название радиоактивность, а сами элементы – радиоактивные. Таким образом, они делятся на стабильные и радиоактивные изотопы.
Изотопы элементов после Висмута в ПСХЭ, начиная с 84, будут относиться к радиоактивным элементам.
Электроны в атоме
Давайте рассмотрим, какое место занимают электроны в атоме. Если ядро составляет 99,86 % от массы, а, как известно, что количество протонов и электронов равно. То на долю электронов приходится всего 0,14% от массы.
На данный момент, электрон считают элементарной частицей.
Модель Резерфорда (планетарная) на очень примитивном уровне даёт представление,как располагаются электроны и протоны в атоме, поскольку атом имеет достаточно сложное строение.
Электрон настолько мал и находится в постоянном движении с достаточно большой скоростью, что зафиксировать его в определённом месте и времени сложно. Именно по этой причине говорят, что электрон в атоме находится не в заданной точке, а может там предположительно находиться, потому что его зафиксировать в определённый момент времени невозможно.
Ядро атома Водорода имеет 1 протон, вокруг которого вращается один электрон. Но как быть, если количество электронов в атоме будет два и более, каким образом они будут размещаться.
Поскольку они двигаются с достаточной большой скоростью, то чтобы указать распределение электронов в атоме используют 4 числа – орбитальные характеристики.
Прежде чем, мы перейдём к орбитальным характеристикам, давайте представим многоэтажный дом, в который необходимо разместить жителей, в нашем случае – это электроны.
Первая орбитальная характеристика
Другими словами, представляем, что наш многоэтажный дом содержит 7 этажей. Цифры 1, 2, 3, 4, 5, 6, 7 обозначают номер этажа или энергетические уровни электрона в атоме.
Вторая орбитальная характеристика
Возвращаемся к нашему, многоэтажному дому, орбитальное число показывает типы орбиталей или в сравнении с домом квартиры s, p, d и f.
Третья орбитальная характеристика
Представить квартиру, в виде ячейки или квадрата, так вот магнитное квантовое число указывает число орбиталей.
Смотрим, на первом этаже размещается только s-квартиры, которые будут однокомнатными. На втором этаже уже имеется две квартиры s и р, т.е. однокомнатная и трёхкомнатная. На третьем этаже s, p, d. Четвёртый, пятый и шестой этажи размещают 4 квартиры s, p, d и f.
Четвёртая орбитальная характеристика
Это означает, что в одной ячейке (квадрате), может поселиться не больше двух электронов.
Вот на таком достаточно примитивном уровне, мы рассмотрели состояние электронов в атоме. Но как они там располагаются? Каждый электрон занимает своё определённое место, согласно энергии.
Рассмотрим распределение электронов по энергетическим уровням в атоме. Наверняка вы заметили, что наш дом семиэтажный. Как думаете, по какой причине? ПСХЭ содержит 7 периодов (7 этажей). Если элемент находится во втором периоде, значит, его электроны будут занимать 1 и 2 этаж и никаким образом не могут попасть на 5 или 6 этажи. В данном примере 2 этаж будут называть внешним, научным языком – внешним энергетическим уровнем (он крайний).
Главные правила образования оболочки электронов в атоме
Давайте дадим волю фантазии, допустим, к нашему семиэтажному дому подошёл Бор, не лес как вы могли подумать, а элемент. Смотрим в шпаргалку, как вы уже догадались, это будет периодическая таблица, и ищем там его расположение. Бор занимает ячейку под номером 5. Эта ячейка находится во втором периоде, третьей группе. Значит, число электронов в атоме 5, они размещаются на I и II этажах. Первый уровень будут занимать 2 электрона. Значит на второй этаж (внешний уровень) переходят оставшиеся 3. Два будут занимать s-подуровень, один будет размещаться на р-подуровне. Строение оболочки атома В (бор).
Составим электронную и графическую схему элемента на примере Si и V с помощью алгоритма.
Обратите внимание, чтобы составить электронную формулу элемента, достаточно знать его расположение в ПСХЭ. Итак, начинаем по порядку.
Существует основное состояние электрона в атоме и возбуждённое, которое возникает, если к атому применить некоторую определённую энергию. Электроны во внешнем электронном слое атома имеют способность перемещаться, занимая место на свободной орбитали, образуя при этом возбуждённое состояние.
Обратите внимание, число неспаренных электронов отвечает валентности элементов: Li (I), Be (II), B (III), C (II и IV).
Периодичность свойств элементов. Электроотрицательность
С развитием учения о строении атома, периодический закон занимает ещё больше значимое место в естествознании. Уже неоднократно говорилось, что ПСХЭ является уникальной подсказкой. Достаточно знать расположение и строение электронных оболочек атомов элементов, и возникает возможность судить о том, какими характеристиками он будет обладать. В настоящее время периодический закон имеет формулировку, данную Менделеевым, с небольшим уточнением.
За то, какими свойствами будет наделён элемент, отвечают электроны, которые размещены на внешнем энергетическом уровне. Их ещё называют валентные электроны атома, именно они отвечают за периодическое изменение свойств элементов.
С увеличением массы атома в пределах периода, количество электронов также возрастает, пока не заполнятся все вакантные ячейки уровня.
В ходе химической реакции происходит «движение» электронов. Т.е. одни элементы будут отдавать их, а вторые принимать.
Рассмотрим на примере, образования вещества NaCl.
Обобщая данный пример, сделаем вывод, элементы, которые содержат малое количество электронов на внешнем уровне (1 – 3) будут только отдавать электроны – и они будут относиться к металлам. Неметаллы характеризуются способностью принимать электроны.
Из определения сделаем вывод, что наибольшую электроотрицательность имеет Фтор (F), нет ни одного элемента, кому бы он смог отдать свой электрон, а будет только забирать. Минимальную ЭО будет иметь Франций (Fr).
Ещё одна важная причина изменения свойств элементов, которая изменяется периодически, это радиус атома. Если ЭО характеризует неметаллы, то по радиусу судят о металлических свойствах. Металлы легко отдают электроны, чем дальше они находятся от ядра, тем легче «отрываются». Радиус атома с увеличением заряда ядра в периоде уменьшается, так как ядро начинает сильнее притягивать электроны.
Строение атома
Многообразие химических соединений обусловлено различным сочетанием атомов химических элементов в молекулы и немолекулярные вещества. Способность же атома вступать в химические соединения, его химические и физические свойства определяются структурой атома. В связи с этим для химии первостепенное значение имеет внутреннее строение атома и в первую очередь структура его электронной оболочки.
Модели строения атома
В начале XIX века Д. Дальтон возродил атомистическую теорию, опираясь на известные к тому времени основополагающие законы химии (постоянства состава, кратных отношений и эквивалентов). Были проведены первые эксперименты по изучению строения вещества. Однако, несмотря на сделанные открытия (атомы одного и того же элементы обладают одними и теми же свойствами, а атомы других элементов – иными свойствами, введено понятие атомной массы), атом считали неделимым.
После получения экспериментальных доказательств (конец XIX начало XX века) сложности строения атома (фотоэффект, катодные и рентгеновские лучи, радиоактивность) было установлено, что атом состоит из отрицательно и положительно заряженных частиц, которые взаимодействуют между собой.
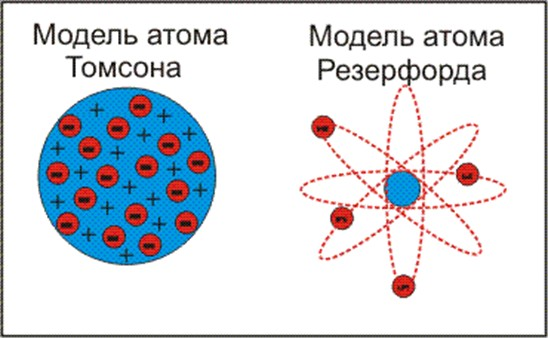
Эти открытия дали толчок к созданию первых моделей строения атома. Одна из перых моделей была предложена Дж. Томсоном (1904) (рис. 1): атом представлялся как «море положительного электричества» с колеблющимися в нем электронами.
Рис. 1 Модели строения атома по Томсону и Резерфорду
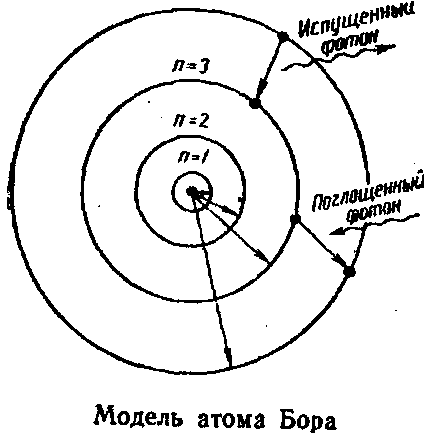
Опыты по изучению атомных спектров показали несовершенство планетарной модели строения атома, поскольку эта модель противоречит линейчатой структуре атомных спектров. На основании модели Резерфорда, учении Энштейна о световых квантах и квантовой теории излучения планка Нильс Бор (1913) сформулировал постулаты, в которых заключается теория строения атома (рис. 2): электрон может вращаться вокруг ядра не по любым, а только по некоторым определенным орбитам (стационарным), двигаясь по такой орбите он не излучает электромагнитной энергии, излучение (поглощение или испускание кванта электромагнитной энергии) происходит при переходе (скачкообразном) электрона с одной орбиты на другую.
Рис. 2. Модель строения атома по Н. Бору
Накопленный экспериментальный материал, характеризующий строение атома, показал, что свойства электронов, а также других микрообъектов не могут быть описаны на основе представлений классической механики. Микрочастицы подчиняются законам квантовой механики, которая стала основой для создания современной модели строения атома.
Главные тезисы квантовой механики:
— энергия испускается и поглощается телами отдельными порциями – квантами, следовательно, энергия частиц изменяется скачкообразно;
— электроны и другие микрочастицы имеют двойственную природу – проявляет свойства и частицы, и волны (корпускулярно-волновой дуализм);
— квантовая механика отрицает наличие определенных орбит у микрочастиц (для движущихся электронов невозможно определить точное положение, т.к. они движутся в пространстве вблизи ядра, можно лишь определить вероятность нахождения электрона в различных частях пространства).
Пространство вблизи ядра, в котором достаточно велика вероятность нахождения электрона (90%), называется орбиталью.
Квантовые числа. Принцип Паули. Правила Клечковского
Состояние электрона в атоме можно описать с помощью четырех квантовых чисел.
n – главное квантовое число. Характеризует общий запас энергии электрона в атоме и номер энергетического уровня. n приобретает целочисленные значения от 1 до ∞. Наименьшей энергией электрон обладает при n=1; с увеличением n – энергия возрастает. Состояние атома, когда его электроны находятся на таких энергетических уровнях, что их суммарная энергия минимальна, называется основным. Состояния с более высокими значениями называются возбужденными. Энергетические уровни обозначаются арабскими цифрами в соответствии со значением n. Электроны можно расположить по семи уровням, поэтому, реально n существует от 1 до 7. Главное квантовое число определяет размеры электронного облака и определяет средний радиус нахождения электрона в атоме.
l – орбитальное квантовое число. Характеризует запас энергии электронов в подуровне и форму орбитали (табл. 1). Принимает целочисленные значения от 0 до n-1. l зависит от n. Если n=1,то l=0, что говорит о том, что на 1-м уровне 1-н подуровень.
Таблица 1. Формы орбиталей
Рис. 3. Одна из возможных ориентаций в пространстве p-орбитали
Состояние электронов в атомах определяется принципом Паули: в атоме не может быть двух электронов с одинаковым набором всех квантовых чисел. Последовательность заполнения орбиталей электронами определяется правилами Клечковского: орбитали заполняются электронами в порядке возрастания суммы (n+l) для этих орбиталей, если сумма (n+l) одинакова, то первой заполняется орбиталь с меньшим значением n.
Однако, в атоме обычно присутствуют не один, а несколько электронов и, чтобы учесть их взаимодействие друг с другом используют понятие эффективного заряда ядра – на электрон внешнего уровня действует заряд, меньший заряда ядра, вследствие чего внутренние электроны экранируют внешние.
Основные характеристики атома: атомный радиус (ковалентный, металлический, ван-дер-ваальсов, ионный), сродство к электрону, потенциал ионизации, магнитный момент.
Электронные формулы атомов
У элементов второго периода электроны заполняют 2-й энергетический уровень, на котором могут находиться не более 8-ми электронов. Вначале электроны заполняют s-подуровень, потом – p-подуровень. Например:
У атомов некоторых элементов, наблюдается явление «проскока» электрона с внешнего энергетического уровня на предпоследний. Проскок электрона происходит у атомов меди, хрома, палладия и некоторых других элементов. Например:
24Cr 1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 4s 1
Связь электронного строения атома с положением элемента в Периодической системе
Электронную формулу элемента определяют по его положению в Периодической системе Д.И. Менделеева. Так, номер периода соответствует У элементов второго периода электроны заполняют 2-й энергетический уровень, на котором могут находиться не более 8-ми электронов. Вначале электроны заполняют У элементов второго периода электроны заполняют 2-й энергетический уровень, на котором могут находиться не более 8-ми электронов. Вначале электроны заполняют s-подуровень, потом – p-подуровень. Например:
У атомов некоторых элементов, наблюдается явление «проскока» электрона с внешнего энергетического уровня на предпоследний. Проскок электрона происходит у атомов меди, хрома, палладия и некоторых других элементов. Например:
24Cr 1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 4s 1
энергетический уровень, на котором могут находиться не более 8-ми электронов. Вначале электроны заполняют s-подуровень, потом – p-подуровень. Например:
Номер группы для элементов главных подгрупп равен числу электронов на внешнем энергетическом уровне, такие электроны называют валентными (они участвуют в образовании химической связи). Валентными электронами у элементов побочных подгрупп могут быть электроны внешнего энергетического уровня и d-подуровня предпоследнего уровня. Номер группы элементов побочных подгрупп III-VII групп, а также у Fe, Ru, Os соответствует общему числу электронов на s-подуровне внешнего энергетического уровня и d-подуровне предпоследнего уровня
Задания:
Изобразите электронные формулы атомов фосфора, рубидия и циркония. Укажите валентные электроны.
Ответ:
15P 1s 2 2s 2 2p 6 3s 2 3p 3 Валентные электроны 3s 2 3p 3
37Rb 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 5s 1 Валентные электроны 5s 1
40Zr 1s 2 2s 2 2p 6 3s 2 3p 6 3d 10 4s 2 4p 6 4d 2 5s 2 Валентные электроны 4d 2 5s 2