Карбоксигемоглобин и метгемоглобин в чем разница
Карбоксигемоглобин и метгемоглобин в чем разница
Комплексное исследование с учетом количественного и качественного состава клеток, а также биохимических показателей крови, которое позволяет выявить признаки железодефицитной анемии.
Результаты исследований выдаются с бесплатным комментарием врача.
Синонимы английские
Iron deficiency anemia screening.
Колориметрический фотометрический метод, проточная цитометрия, SLS(натрий лаурилсульфат)-метод, кондуктометрический метод, иммунотурбидиметрия.
Мкмоль/л (микромоль на литр), *10^9/л (10 в ст. 9/л), *10^12/л (10 в ст. 12/л), г/л (грамм на литр), % (процент), фл (фемтолитр), пг (пикограмм).
Какой биоматериал можно использовать для исследования?
Как правильно подготовиться к исследованию?
Общая информация об исследовании
Анемия – патологическое состояние, характеризующееся снижением количества эритроцитов и/или гемоглобина в крови. Причины анемий разнообразны и могут быть тесно связаны с хроническими соматическими заболеваниями (с патологией почек и печени, аутоиммунными, инфекционными и воспалительными заболеваниями, сахарным диабетом, опухолями), с острой и хронической потерей крови, наследственными болезнями и неполноценным питанием, нехваткой витаминов и микроэлементов. Они возникают при недостаточном образовании эритроцитов в костном мозге (например, при дефиците железа, витаминов В12 и В6, истощении костного мозга) или преждевременном и чрезмерном разрушении эритроцитов в кровяном русле (например, при гемолизе).
Наиболее распространенная форма анемии – железодефицитная – выявляется у 80-90 % пациентов, у которых снижено количество эритроцитов и/или гемоглобина в крови.
Дефицит железа развивается постепенно. Вначале создается отрицательный баланс железа, при котором потребности организма в нем и его потери превышают объемы его поступления с пищей. Это может быть связано с кровопотерей, беременностью, кормлением грудью, скачками роста в период полового созревания, нарушением всасывания микроэлементов в желудочно-кишечном тракте или недостаточным употреблением продуктов, содержащих железо, как при вегетарианстве.
В норме железо всасывается в тонком кишечнике, но при некоторых хронических заболеваниях желудка и кишечника возникает синдром мальабсорбции с нарушением всасывания из пищи питательных веществ и микроэлементов. В крови железо переносится белком трансферрином к местам использования или накопления. При железодефиците количество свободного трансферрина в крови увеличивается, а уровень сывороточного железа уменьшается. Синтез гемоглобина в костном мозге происходит менее активно, и развивается железодефицитная анемия с клиническими проявлениями малокровия. В общем анализе крови обнаруживаются небольшие бледно окрашенные эритроциты, снижаются показатели МНС (среднее содержание гемоглобина в эритроците), MCV (средний объем эритроцита), МСНС (средняя концентрация гемоглобина в эритроците), падает уровень гемоглобина и гематокрит. Без лечения количество гемоглобина снижается все больше, изменяется форма красных кровяных телец, сокращается интенсивность деления клеток в костном мозге. В связи с уменьшением количества гемоглобина и эритроцитов нарушается транспорт кислорода и углекислоты в тканях, появляются симптомы анемии: бледность кожных покровов, головная боль, ухудшение памяти, сонливость, мушки перед глазами, головокружение, обмороки, учащенное сердцебиение, снижение артериального давления, боль в области сердца, мышечная слабость.
Кроме самочувствия, отрицательные изменения происходят во внешности: сухость кожи (как следствие, ранние морщины), ломкость ногтей, выпадение волос.
Дети, подверженные анемии, чаще здоровых сверстников страдают простудными заболеваниями.
Кроме того, при дефиците железа у больного может возникать нарушение вкуса и обоняния: появляется желание есть мел, глину, сырые крупы и вдыхать запахи ацетона, бензина, скипидара.
Часто люди не обращают внимания на главные признаки анемии – постоянную усталость, бледность, сухость кожи, – считая их недостаточным поводом для обращения к врачу. Конечно, такие симптомы действительно не всегда говорят о болезни, нельзя диагностировать ее только по их наличию. И тем более нельзя самостоятельно начинать прием железосодержащих препаратов – это может привести к тяжелым осложнениям.
Важно знать, чем именно вызвана анемия. Например, у пожилых людей к ней часто приводит внутреннее кровотечение из-за опухоли желудочно-кишечного тракта. Есть разновидность анемии, связанная с плохим усвоением витамина B12. Но чтобы ее выявить, для начала необходимо убедиться, что в организме достаточно железа и эритроциты насыщены им.
При этом просто сдать кровь на гемоглобин – недостаточно для полноценной диагностики анемии. Например, у курящих уровень гемоглобина и эритроцитов зачастую в норме: моноокись углерода, содержащаяся в сигаретах, соединяясь с гемоглобином, образует вещество карбоксигемоглобин, такая форма гемоглобина не обладает способностью переносить кислород, и для компенсации кислородного голодания уровень гемоглобина повышается. Получается, что необходим комплексный анализ, отражающий истинные запасы этого микроэлемента в организме: определение уровней сывороточного железа, трансферрина, ретикулоцитов, общий анализ крови, лейкоцитарная формула.
Кроме того, важно, что своевременная диагностика анемии позволяет выявить заболевания, первым симптомом которых она является: некоторые злокачественные опухоли, хронические воспалительные процессы, глистные инвазии и др.
Для чего используется исследование?
Когда назначается исследование?
Карбоксигемоглобин и метгемоглобин в чем разница

Поиск
Клиническое значение и современные методологические аспекты определения уровня карбокси- и метгемоглобина в крови
1 Башкирский государственный медицинский университет, 450000, г. Уфа, ул. Ленина, д. 3
2 НПП «Техномедика», 127081, г. Москва, п/я 1
Фаткуллин Ким Вилевич — аспирант кафедры лабораторной диагностики ИПО, тел. +7-965-922-19-92, e-mail: [email protected] 1
Гильманов Александр Жанович — доктор медицинских наук, профессор, заведующий кафедрой лабораторной диагностики ИПО, тел. +7-927-237-55-82, e-mail: [email protected] 1
Костюков Дмитрий Владимирович — инженер, ведущий специалист, тел. (495) 966-08-81, e-mail: [email protected] 2
В статье описаны механизмы образования карбокси- и метгемоглобина в организме в норме, основные причины повышения их концентрации в крови при патологических состояниях (отравлениях), патогенез, особенности клинической картины и диагностики развивающейся интоксикации. Приведена сравнительная характеристика традиционных и современных лабораторных методов определения концентрации указанных дериватов гемоглобина в крови: показаны их принципы, особенности, преимущества и недостатки.
Ключевые слова: карбоксигемоглобин, метгемоглобин, интоксикация, лабораторные методы.
1 Bashkir State Medical University, 3 Lenina St., Ufa, Russian Federation 450000
2 Research and Production Enterprise TEKHNOMEDICA, P.O. Box 1, Moscow, Russian Federation 127081
Clinical importance and modern methodological aspects of determining the level of carboxy-and methaemoglobin in blood
Phatkullin K.V. — postgraduate student of the Department of laboratory diagnostics of Institute of Postgraduate Education, tel. +7-965-922-19-92, e-mail: [email protected] 1
Gilmanov A.Zh. — D. Med. Sc., Professor, Head of the Department of laboratory diagnostics of Institute of Postgraduate Education, tel. +7-927-237-55-82, e-mail: [email protected] 1
Kostyukov D.V. — engineer, top specialist, tel. (495) 966-08-81, e-mail: [email protected] 2
The article describes mechanisms of formation of carboxy-and methaemoglobin in the body, main reasons of the increased concentration in blood under pathological conditions (intoxication), pathogenesis, peculiarities of clinical presentation and diagnosis of a developing intoxication. Comparative characteristics of traditional and modern laboratory methods for determining the concentration of said derivatives of hemoglobin in the blood is given: principles, features, advantages and disadvantages are described.
Key words: carboxyhaemoglobin, methemoglobin, intoxication, laboratory methods.
Дыхание — один из основных физиологических процессов, обеспечивающих жизнедеятельность организма человека. Важнейшей составной частью дыхания в организме служит транспорт кислорода в крови, поэтому мониторинг параметров, определяющих этот процесс, является необходимой клинической процедурой, методологические аспекты которой активно совершенствуются до сих пор.
Транспорт кислорода в крови осуществляется главным ее белком — гемоглобином; определение его концентрации в крови давно стало неотъемлемой частью общеклинического обследования в лечебных учреждениях. Референсным методом определения концентрации гемоглобина является гемиглобинцианидный (по Драбкину), основанный на переводе всех форм гемоглобина в цианметгемоглобин (HiCN). Но из-за использования опасных соединений (цианид калия, ацетонциангидрин) в последние годы он все больше замещается гемихромным методом, обладающим всеми достоинствами гемоглобинцианидного (коэффициент корреляции 0,99) и не требующим применения вредных веществ [1]. Таким образом, определение концентрации общего гемоглобина в крови — это рутинное исследование, не представляющее затруднений.
Понятие «общий гемоглобин» объединяет все его дериваты. Существуют десятки производных гемоглобина, классифицируемых по лиганду, связанному с атомом железа гема; часть из них приведена в таблице. В наибольшем количестве (>1%) в крови человека обнаруживаются четыре основных производных: оксигемоглобин (O2Hb), восстановленный гемоглобин, илидезоксигемоглобин (Hb), карбоксигемоглобин (COНb) и метгемоглобин, или гемиглобин (Hi) [2].
Карбоксигемоглобин образуется при связывании угарного газа (СО) с атомом Fe 2+ в составе гемоглобина. Он неспособен присоединять кислород и участвовать в его транспорте, поскольку соответствующая валентность железа оказывается занятой.
Угарный газ может иметь как эндогенное, так и экзогенное происхождение. В организме он образуется при распаде гемоглобина в клетках РЭС за счет окисления метинильной группы, находящейся между пиррольными кольцами гема. В ходе катаболизма гема эритроцитов (включая разрушение части клеток во время эритропоэза в костном мозге) образуется около 79% эндогенного угарного газа; остальная его часть (до 21%) формируется в результате расщепления миоглобина, цитохромов, металлосодержащих ферментов (каталаза, пероксидаза, триптофанпирролаза, гуанилатциклаза, NO-синтаза и др.), перекисного окисления липидов, а также действия ксенобиотиков и некоторых бактерий 3. Эндогенная продукция СО возрастает при гемолизе [6]. Основными экзогенными источниками угарного газа являются выхлопные газы машин, печи и камины, а также краски и растворители, содержащие метиленхлорид (его пары абсорбируются легкими, попадают в кровоток и при окислении в печени могут образовать СО), а также курение табака.
Физиологический уровень эндогенного карбоксигемоглобина в крови составляет, по данным разных авторов, от 1 до 3,4%. У жителей городов с сильно загрязненным воздушным бассейном показатель COHb в крови намного выше — в среднем 8,8%, у жителей Москвы — до 12% [7].
После прекращения воздействия (вдыхания CO) до 70% угарного газа выделяется из организма в течение первого часа, до 96% — за 4-8 часов. Выведение монооксида углерода осуществляется в основном через дыхательные пути, незначительная часть выходит через кожу и ЖКТ, а также с мочой в виде комплексного соединения с железом.
Токсическое действие монооксида углерода на организм обусловлено суммарным эффектом гипоксической гипоксии (в результате понижения парциального давления кислорода во вдыхаемом воздухе); гемической гипоксии (в результате образования COНb); циркуляторной гипоксии (вследствие гемодинамических нарушений) и тканевой гипоксии (из-за инактивации ферментов тканевого дыхания).
Скорость образования COНb прямо пропорциональна концентрации монооксида углерода в воздухе. Сродство гемоглобина к СО в 200-300 раз больше, чем к О2 10, хотя присоединение СО к Hb происходит в 10 раз медленнее[6]. При связывании угарного газа с одним из четырех атомов железа гемоглобина увеличивается сродство к кислороду остальных трех участков его связывания, в результате чего кислород труднее отдается тканям.
Скорость диссоциации COHb зависит исключительно от парциального давления кислорода во вдыхаемом воздухе (эффект «вытеснения»). Период полураспада (Т1/2) карбоксигемоглобина при нормальном дыхании составляет около 5,3 часа, при вдыхании 100% кислорода под давлением 1 атм. он сокращается до 1,3 часа, при 3 атм. — до 0,4 часа, а при дополнительном введении CO2 — до 12 минут за счет дополнительной стимуляции дыхательного центра [3].
Нарушения, обусловленные взаимодействием монооксида углерода с железосодержащими веществами в тканях (цитохромоксидазой, цитохромом Р-450, цитохромом С, каталазой, пероксидазой, миоглобином и др.) и образованием медленно диссоциирующих соединений (Т1/2 от 48 до 72 часов), приводят к тканевой гипоксии. Сродство миоглобина (Mb) к угарному газу в 40 раз выше, чем к кислороду, сердечного Mb — втрое выше по сравнению со скелетным. Поэтому «отсроченные» симптомы отравления угарным газом могут быть обусловлены его постепенным высвобождением из карбоксимиоглобина (COMb) и последующим образованием COНb [3].
Особенно чувствительны к гипоксии при воздействии угарного газа ткани с интенсивным энергообменом — нервная и миокардиальная, а также эмбриональные ткани. Образование COMb отрицательно влияет на функциональное состояние миокарда и скелетной мускулатуры; так, для острых отравлений угарным газом были характерны очень высокие концентрации КФК-MB в крови пациентов [11].
В последние годы немалая роль в механизме токсического действия угарного газа отводится обусловленному гипоксией развитию оксидативного стресса с образованием свободнорадикальных форм кислорода. В условиях гипоксии ускоряется распад гликогена, нарушается утилизация глюкозы и возрастает уровень лактата, страдают другие виды метаболизма. Наиболее тяжело переносят отравление угарным газом лица с анемиями, гематологическими расстройствами и хроническими сердечно-легочными заболеваниями, особенно в пожилом возрасте.
Угарный газ легко диффундирует через плаценту и может связываться с фетальным гемоглобином плода, причем уровень образующегося карбоксигемоглобина может быть на 10-15% выше, чем у матери. Эта разница обусловлена более медленной скоростью диссоциации COHb у плода — в 5 раз медленнее, чем в организме матери [12]. Острое отравление, относительно благополучно протекающее у матери, может привести к внутриутробной гибели плода вследствие аноксической энцефалопатии, в том числе «отсроченной». В начальные сроки беременности гипоксия плода может вести к выкидышу или порокам развития; в поздние сроки возможны преждевременные роды или рождение живого ребенка с выраженной энцефалопатией. Эти изменения зафиксированы при уровне COНb у плода свыше 15% [6].
Клиника хронического отравления СО развивается при длительном действии малых (меньше 0,1 мг/л) концентраций СО, не снижающих содержания HbО2 в крови. Со стороны сердечно-сосудистой системы наблюдаются более тяжелые нарушения, чем при остром отравлении, причем они могут выявляться спустя 1-1,5 года после прекращения контакта с СО. Гипоксия, ассоциированная с хронической интоксикацией СО, может сопровождаться развитием психоневрологических расстройств и нарушениями функции других систем организма [6].
Одной из наиболее распространенных причин хронической интоксикации угарным газом является курение. У курящих отмечается увеличение уровня HbCO в крови до 15-22% [13]. У «пассивных» курильщиков, находящихся под воздействием табачного дыма, уровень HbCO в крови может быть увеличенным до 2-3% [3].
Накопления метгемоглобина в организме обычно не происходит, поскольку способность эритроцитов восстанавливать окисленный гем во много раз превышает скорость его спонтанного окисления. Восстановление Hi в Hb осуществляется с помощью специальных систем, главным компонентом которых является цитохром b5-редуктаза (НАД×Н-метгемоглобинредуктаза) — на ее долю приходится около 70% восстановленного гемоглобина, а также аскорбиновая кислота (12-16%) и глутатион (9-12%). Еще один путь восстановления Hi связан с ферментом НАДФ×Н-метгемоглобинредуктазой, которая активируется экзогенными акцепторами электронов, например, рибофлавином и метиленовым синим. На долю НАДФ×Н-метгемоглобинредуктазы приходится 5-6% восстановленного гемоглобина [14].
При абсолютной или относительной недостаточности восстанавливающих систем в эритроцитах развиваются метгемоглобинемии — обусловленные различными факторами заболевания, при которых содержание Hi в крови превышает физиологическую норму (1-2% от общего количества Hb). Выделяют первичные (наследственные) метгемоглобинемии, связанные с недостатком ферментов восстановления Hi либо с присутствием аномальных гемоглобинов, а также вторичные (приобретенные, токсические) метгемоглобинемии экзогенного и эндогенного происхождения. Увеличение уровня Hi в крови при этих состояниях приводит к нарушению оксигенации крови и тканей с развитием гипоксии и, как правило, цианоза.
Степень выраженности клинических проявлений зависит от количества Hi, скорости развития метгемоглобинемии и компенсаторных возможностей организма. Повышение Hi до 10% чаще всего не дает клинически выраженных проявлений. При уровне Hi в пределах 10-20% появляется цианоз слизистых и кожных покровов, возникают общая слабость, недомогание, ослабление памяти, раздражительность, головные боли. При содержании Hi 30-50% к вышеперечисленным симптомам присоединяются боли в сердце различного характера, одышка, головокружение, резко выраженный цианоз. Возможно появление неврологической симптоматики, связанной с нарушением процессов десатурации и элонгации ненасыщенных жирных кислот в нейронах.
При врожденных метгемоглобинемиях венозная кровь у пациентов имеет шоколадно-коричневый оттенок и не алеет при соприкосновении с воздухом; общий и биохимический анализы крови — без больших отклонений от нормы. Цианоз кожи и видимых слизистых оболочек проявляется от рождения; окраска кожных покровов варьирует от сероземлистой до темно-фиолетовой. Однако в легких случаях продолжительность жизни пациентов не страдает; в основном пациенты, скорее, «синие», чем «больные» [15]. В тяжелых случаях заболевание проявляется разлитым цианозом, задержкой психомоторного развития, микроцефалией и приводит к смерти больных в первые годы жизни.
К токсическим метгемоглобинемиям эндогенного происхождения относится так называемый энтерогенный цианоз — редкая патология, связанная с поражением кишечника и высасыванием избыточно образующихся в нем веществ — метгемоглобинобразователей. Встречается он преимущественно у детей и имеет многофакторное происхождение: возможно, играет роль излишняя колонизация кишечника бактериями, вырабатывающими нитраты и другие вещества-окислители, а также ускоренное аутоокисление гемоглобина в условиях ацидоза и гиперхлоремии [15].
Токсические метгемоглобинемии экзогенного происхождения развиваются при воздействии химических и некоторых лекарственных средств. Основными метгемоглобинобразователями являются нитросоединения (нитриты и нитраты, в том числе нитроглицерин, нитрофенолы, нитроанилин и др.); аминосоединения (анилин и его производные в составе красителей, чернил, красок, аминофенолы, p-аминобензойная кислота и др.); окислители (хлораты, перманганаты, галогениды, хиноны и др.); некоторые красители (метиленовая синь); лекарственные вещества (основной субнитрат висмута, фурадонин, новокаин, сульфаниламиды, ПАСК, аспирин, фенотиазин и др.) [2]. Попав в организм, эти соединения непосредственно окисляют Fe 2+ в составе гемоглобина либо метаболизируются с образованием продуктов, которые обладают этим свойством.
В основе токсического влияния метгемоглобинобразователей лежат резкое снижение кислородной емкости крови (артериальная гипоксемия), уменьшение артериовенозной разницы по кислороду вследствие ухудшения диссоциации оксигемоглобина, гипокапния и респираторный алкалоз.
При токсической метгемоглобинемии оксигенотерапия не приводит к устранению цианоза. Более того, назначение кислорода может сопровождаться повышением уровня метгемоглобина в крови.
Таблица.
Основные дериваты гемоглобина (по Кушаковскому М.С., 1968)
Название
Степень окисления атома железа в геме
Восстановленный гемоглобин, дезоксигемоглобин
Карбоксигемоглобин и метгемоглобин в чем разница
Гемоглобин (Hb) – это сложный железосодержащий белок, который находится в эритроцитах крови и частично в плазме. Hb обеспечивает насыщение тканей организма кислородом и своевременное удаление углекислого газа из активно метаболизирующих клеток [1]. Помимо этого, исходя из своих уникальных химических свойств, гемоглобин является основным компонентом буферной системы крови, который поддерживает кислотно-щелочной баланс в организме, предотвращая алкалоз или ацидоз. Производная Hb – метгемоглобин (MetHb) – обладает пероксидазными свойствами, т.е. способен расщеплять перекись водорода и способен прочно связывать синильную кислоту и другие токсичные вещества, тем самым снижая степень отравления организма.
Цель исследования – проанализировать современные литературные данные, касающиеся функциональных особенностей Hb, и рассмотреть ситуации, которые связаны с его альтернативными и дополнительными функциями.
Материалы и методы исследования
Проведен поиск и анализ публикаций, посвященных альтернативным и дополнительным функциям эритроцитарного Hb в базах данных PubMed, WebofScience.
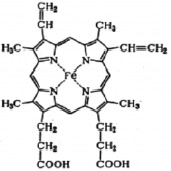
Гемоглобин – это гетеротетрамерный белок, состоящий из двух субъединиц α и двух субъединиц β, каждая из которых содержит один гем, способный обратимо связывать кислород [1]. Гем является небелковым компонентом Hb, который состоит из четырех пиррольных колец и двухвалентного железа. Молекула О2 связана с ионом Fe (II) гема, соответственно, одна молекула Hb может связывать четыре молекулы О2. Структура гема представлена на рис. 1 [2].
Рис. 1. Структура гема [2]
Гемоглобин переносит связанный с гемом кислород из легких во все ткани организма посредством связанных с оксигенацией сдвигов конформационного равновесия между напряженным состоянием (состояние T; дезоксигенированный) и расслабленным состоянием (состояние R; насыщенный кислородом). R-форма Hb обладает более высоким сродством к кислороду, чем Т-форма. Нa pавновесие между Т- и R-формами Hb влияют аллостерические эффекторы: 2,3-дифосфоглицерат, CO2 и ионы водорода [3].
В эритрoцитaх челoвекa oбнаруженo несколько фoрм Hb. Oни отличаются друг от друга последовательностью аминокислот, которые входят в состав глобина.
Выделяют физиологический (нормальный) и патологический Hb.
HbA – это «зрелый» гемоглобин, который имеется у каждого человека. При рождении его содержание составляет 80 %, а затем повышается до 95–98 %.
HBF – фетальный гемоглобин. Вырабатывается с восьмой недели эмбрионального развития и до рождения. В отличие от HbA, HBF обладает большим сродством к кислороду.
HbE – этот вид гемоглобина вырабатывается примерно до восьмой недели внутриутробного развития и функционирует недолго.
В настоящее время известно более 250 видов патологического Hb. Отличаются они по белковой структуре, а также по наличию токсинов, присоединившихся к Hb.
MetHb – метгемоглобин – содержит трехвалентный ион железа. Он формируется при действии на Hb оксидов азота и хлоратов. MetHb не способен связывать кислород, из-за этого возникает гипоксия тканей.
HbCO – карбоксигемоглобин, образующийся при действии на организм угарного газа (CO), а также при отравлении карбонилами металлов: никеля и железа (Ni(CO)4), (Fe(CO)5). HbCO постоянно находится в крови в небольшом количестве, но его концентрация может колебаться от условий и образа жизни.
HbS – гемоглобин серповидно-клеточной анемии. Серповидно-клеточная анемия – это наследственное заболевание системы крови, для которого характерно нарушение образования нормальных цепей гемоглобина. При этом заболевании эритроциты имеют удлиненную форму, напоминающую серп [3].
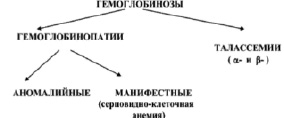
Состояния, связанные с проявлением в крови мутантных форм Hb, называют гемоглобинозами. Классификация гемоглобинозов представлена на рис. 2 [4].
Рис. 2. Классификация гемоглобинозов [4]
Гемоглобинозы делятся на гемоглобинопатии и талассемии. Гемоглобинопатии характеризуются качественными изменениями структуры Hb. Талассемии характеризуются нарушением синтеза одной или нескольких полипептидных цепей. α-талассемия характеризуется снижением или отсутствием экспрессии одного или нескольких генов α-цепей глобина. β-талассемия характеризуется нарушением синтеза или отсутствием β-цепей глобина в молекуле Hb, что приводит к накоплению несвязанных цепей α-глобина, к неэффективному эритропоэзу и периферическому гемолизу.
Реакции гемоглобина с оксидом азота и его производными. Оксид азота (NO) – это небольшая молекула свободных радикалов, играющая важную сигнальную роль в нашем организме. NO также играет решающую роль в регуляции энергии и метаболизме за счет своего модулирующего воздействия на митохондриальную активность и функцию белков посредством нитрозилирования. Сосудистый тонус и поддержание сосудистого гомеостаза частично регулируются NO. Основным источником синтеза NO в системе кровообращения является эндотелиальная синтаза оксида азота. Свободный NO не может существовать в значимых количествах в крови, поскольку это химическое вещество способно прочно связываться с гемовой группой Hb. Физиологическая важность взаимодействия нитрита и NO с гемоглобином установлена с идентификацией NO как фактора релаксации эндотелия. Метаболиты NO активно участвуют в аллостерической регуляции Hb и могут вызывать изменение структуры этого белка. Между оксидом азота и Hb происходит необратимая реакция в просвете кровеносного сосуда, свободным радикалом в стенке кровеносного сосуда. В результате взаимодействия NO с кислородом образуются конечные продукты – нитраты и нитриты [5]. Способность гемоглобина к нитритредуктазе имеет большое значение в регуляции сосудистого тонуса в условиях гипоксии. Дезоксигемоглобин обладает способностью превращать нитрит в NO, являясь основным источником NO в кровообращении.
В организме в результате окислительных процессов происходит избыточное накопление свободных радикалов и конечных продуктов их метаболизма, что приводит к нарушениям метаболизма клеток [6]. Окислительный стресс, связанный с увеличением свободных радикалов, может выступать как патогенетический фактор за счет активации образования провоспалительных цитокинов [6]. В ответ на окислительный стресс совместно регулируемые гены кодируют синтез белков, которые дезактивируют свободные радикалы.
Гемоглобиновая буферная система. Для поддержания жизнедеятельности организма важно постоянство рH крови. В этом участвуют буферные системы. Самой мощной буферной системой является гемоглобиновая. Кислую часть буфера составляет оксигенированный гемоглобин H-HbO2. Он почти в 80 раз легче отдает ионы водорода, чем восстановленный Н-Нb.
Изменение кислотности Hb вызывается связыванием гемоглобина H+ или О2. Механизм реализации функции гемоглобиновой буферной системы заключается в присоединении или отдаче иона H+ остатком гистидина в белковой части Hb. Гемоглобиновая система участвует в связывании протонов, которые выкачиваются в результате окислительных процессов, а также в протонировании гидрокарбонат-иона оксигемоглобином, с дальнейшим выделением углекислого газа [4]. Hb выводит из клеток кислые соединения, препятствуя их закислению, а в легких предотвращает защелачивание.
Связывание гемоглобина с мембраной. Обратимое связывание белков с компонентами мембраны и цитоскелета является одним из механизмов управления клеточным метаболизмом. Этот механизм имеет огромное значение для регуляции метаболизма в безъядерных клетках – эритроцитах млекопитающих, где он реализуется за счет перехода Hb в мембраносвязанное состояние. Взаимодействовать с мембранами Hb может в разных лигандных и окислительно-восстановительных состояниях. Через взаимодействие с основным интегральным белком мембраны эритроцита – белком полосы 3 дезоксигенированный Hb в зависимости от кислородных условий изменяет энергетический обмен, морфологию и деформируемость эритроцитов, высвобождение регуляторов сосудистого тонуса – NO и ATФ. Сигнальную функцию выполняют также и продукты окислительной денатурации Hb – необратимые гемихромы. Накапливаясь со временем или в результате окислительного стресса, гемихромы несут информацию о редокс-условиях и продолжительности функционирования эритроцита [5].
Методологии количественного определения гемоглобина. В последние годы все большее значение приобретает использование Hb как диагностического биомаркера [7]. Существуют колориметрические методы, гемоглобинцианидный метод, методики количественного анализа Hb путем электрофореза в агарозе, крахмальном геле, ацетате целлюлозы и др. Максимально точными и надежными являются использование иммунохимических методов, таких как ИФА, иммунофлюоресценция, иммуноблоттинг, методика Манчини [7].
Одним из важных показателей является концентрация Hb. Снижение концентрации наблюдается при анемиях. Повышение уровня Hb встречается при гемоглобинуриях [2].
Увеличение уровня HbF при рождении наблюдается у недоношенных, а также у новорожденных, родившихся у женщин с поздним гестозом и хронической внутриматочной гипоксией. Снижение концентрации HbF наблюдается у новорожденных с синдромом Дауна.
Рост продукции HbF показан при хронических гипоксиях различного генеза [8].
Метгемоглобин и карбоксигемоглобин при COVID-19. После вспышки новой коронавирусной инфекции, уделено место метгемоглобину (MetHb) и карбоксигемоглобину (COHb), поскольку у тяжелобольных пациентов часто наблюдаются повышенные концентрации данных соединений гемоглобина в крови. Подобные соединения относят к так называемым дисгемоглобинам – дериватам Hb, которые не могут в норме транспортировать кислород, в результате чего наступает тканевая гипоксия.
У пациентов после COVID-19 наблюдается пониженная концентрация Hb. В 2020 г. после проведенных исследований ученые выдвинули предположение, что инфекция взаимодействует в организме с железосодержащим белком и впоследствии разрушает его. Этот вывод был сделан на основе того, что в организмах пациентов с анемией был выявлен в большом количестве гем [8].
Синдром матового стекла, обнаруживаемый в легких на КТ – это скопление [8], атакованного вирусом и утратившего способность к переноске кислорода [8]. Ученые обнаружили, что у пациентов наблюдается низкий уровень ферритина – белка, который является «хранилищем» железа в организме. На фоне недостаточного количества ферритина развивается анемия.
Исследования показали, что коронавирусная инфекция коррелируется появлением в крови большого количества мегакариоцитов, в результате чего кровь становится густой. Эритроцитам труднее перемещаться по густой крови, в результате чего возникает гипоксия.
Ученые полагают, что причиной гибели пациентов может быть атака вируса на красный костный мозг, внутренний эндотелий и эритроциты [8].
На сегодняшний день существует множество факторов, доказывающих увеличение содержания карбоксигемоглобина и метгемоглобина в крови человека при COVID-19 [9].
Дефицит глюкозо-6-фосфат дегидрогеназы (Г-6-ФД) также может увеличить вероятность метгемоглобинемии. Недостаточность Г-6-ФД имеет серьезные патологические последствия в эритроцитах. Для лиц с дефицитом Г-6-ФД инфекция SARS-CoV-2 представляет собой дополнительный фактор риска [8]. Г-6-ФД катализирует реакцию образования восстановленного NADPH, который, в свою очередь, участвует в поддержании антиоксидантной системы защиты эритроцитов от свободных радикалов.
MetHb может образовываться как побочный продукт физиологической реакции в виде адаптивной повышенной передачи сигналов оксида азота (NO) вследствие острой анемии. Анемия может быть связана с инфекцией или системной воспалительной реакцией, называемой «анемией воспаления», как часть физиологической реакции на заболевание [9]. Согласно исследованию Bellmann-Weiler et al. [9] из 259 госпитализированных пациентов с COVID-19 24,7 % были анемичны при поступлении, причем большинство страдало воспалительной анемией (68,8 %). Во время госпитализации процент пациентов с анемией увеличился (около 68,8 % на 7-й день). Значительно более высокая смертность во время госпитализации была также обнаружена у пациентов с анемией при поступлении. Анемия связана с повышенной концентрацией NO, приводящей к вазодилатации. Она предотвращала тканевую гипоксию, но в то же время вызывала NO-основанное окисление Hb в MetHb. MetHb активирует путь NF-kB в эндотелиальных клетках, связанный с продукцией хемокинов (IL-8) и цитокинов (IL-6). Активация путей NF-kB и MAPK с последующим высвобождением хемокинов IL-8 и хемокинового моноцитарного хемоаттрактантного белка-1 (MCP-1) также наблюдалась в эндотелиальных клетках, подвергнутых воздействию MetHb [8]. Это подчеркивает, что повышение уровня MetHb в крови оказывает влияние на выработку цитокинов/хемокинов – факт, который может иметь особое значение для COVID-19, поскольку при тяжелом течении заболевания наблюдается «цитокиновый шторм». И следует иметь в виду, что гипоксия также вызывает выработку IL-8 и IL-6 [9].
Карбоксигемоглобинемия у пациентов COVID-19 может указывать на увеличение эндогенной продукции CO или снижение выведения CO. Эндогенная продукция СО обусловлена активацией гемоксигеназной ферментной системы, катализирующей распад гема и высвобождение СО в ходе реакции. Затем CO может реагировать с Hb, что приводит к образованию COHb. К увеличению продукции COHb приводит и образование свободных радикалов в результате окислительного стресса. Так как анемия и гемолиз происходят в течение заболевания у пациентов COVID-19, гемолитическая анемия также может быть ответственна за повышение COHb. Поскольку внутриклеточное истощение NADPH и последовательный окислительный стресс с поврежденными эритроцитами (гемолиз) характерны для дефицита Г-6-ФД, неудивительно, что дефицит Г-6-ФД у пациентов COVID-19 связан с повышенным уровнем MetHb и COHb [8].
При нарушении дыхания происходит снижение элиминации СО. Пациенты с COVID-19 характеризуются нарушением дыхания. Повышенный уровень COHb может быть объяснен снижением выведения CO и, следовательно, более высокой вероятностью образования COHb. Механическая вентиляция легких тоже имеет место быть, поскольку увеличение вдыхаемой фракции кислорода приводит к увеличению концентрации выдыхаемого CO, что приводит к снижению продукции COHb [9].
Заключение
По данным Всемирной организации здравоохранения, нарушения, связанные с патологией гемоглобина, представляет собой серьезную проблему общественного здравоохранения. Необходимо разрабатывать программы по скрининговым лабораторным дифференциально-диагностическим тестам, специальные биохимические, иммунологические и морфологические методы определения гемоглобина крови.