Кетонал или нимесулид что сильнее обезболивает
Боли в спине
Подбор лекарственных средств для лечения болей в спине
Доктор Перец ® — 100 % натуральное тепло для облегчения мышечных и суставных болей 1
Перцовый пластырь № 1 в России по объемам продаж 2
100 % натуральные экстракты красного перца и красавки 2
Основа, позволяющая коже дышать 3
1 Согласно ТУ Доктор Перец ®. Данное утверждение относится только к активным компонентам пластыря, оказывающим тепловой воздействие.
2 Лидер рынка перцовых пластырей по объему продаж в стоимостном и количественном выражении за период июль 2020‑июль 2021 на основе данных ООО «Айкьювиа Солюшнс»
3 Согласно ТУ Доктор Перец ®
Список лекарств от боли в спине
Форма выпуска
таблетки, покрытые пленочной оболочкой, порошок для приготовления суспензии для приема внутрь
«Дексалгин», «Дексалгин 25»
таблетки, покрытые оболочкой, раствор для внутривенного и внутримышечного введения
«Биоран», «Дикловит», «Флотак», «Раптен рапид», «Раптен Дуо», «Диклофенак ретард Оболенское», «Диклофенак-УБФ», «Табук-Ди», «Наклофен», «Наклофен СР», «Диклофенак-АКОС», «Диклофенак-ФПО», «Диклофенак-Эском»
таблетки пролонгированного действия, покрытые оболочкой, капсулы с модифицированным высвобождением, суппозитории ректальные, раствор для внутримышечного введения
таблетки, покрытые оболочкой
«Ибупрофен», «Бруфен СР», «Солпафлекс», «Ибупром Макс»,
таблетки, покрытые оболочкой, таблетки шипучие, таблетки для рассасывания,
капсулы пролонгированного действия, гранулы для приготовления раствора для приема внутрь, суспензия,
суппозитории ректальные (для детей), суспензия для приема внутрь (для детей)
раствор для внутривенного введения
Ибупрофен + кодеина фосфата гемигидрат
таблетки, покрытые оболочкой
таблетки, покрытые оболочкой
таблетки диспергируемые (для детей)
Ибупрофен + питофенон + фенпивериния бромид
таблетки, покрытые оболочкой
капсулы, таблетки, суппозитории ректальные, для внутримышечного введения
гранулы для приготовления раствора для приема внутрь
таблетки, раствор для внутривенного и внутримышечного введения
«Ксефокам», «Ксефокам рапид»
таблетки, покрытые оболочкой, лиофилизат для приготовления раствора для внутривенного и внутримышечного введения
«Матарен», «Мелоксикам», «Мовасин», «Мовикс», «Мовалис»,
таблетки, раствор для внутримышечного введения + суспензия для приема внутрь (Мовалис), суппозитории ректальные
таблетки, гранулы для приготовления суспензии для приема внутрь, суспензия для приема внутрь
раствор для внутримышечного введения
Миорелаксанты
Мильгамма композитум, Полиневрин®
«Мидокалм-Рихтер», «Толперизон с лидокаином-Ферейн»
раствор для внутривенного и внутримышечного введения
«Сирдалуд», «Тизанил», «Тизанидин-Тева», «Тизалуд»
капсулы с модифицированным высвобождением
таблетки, покрытые пленочной оболочкой, раствор для внутримышечного введения
NB! Ибупрофен в таблетках может быть как рецептурного, так и безрецептурного назначения, в отличие от других НПВП, у которых безрецептурными являются только наружные формы!
Форма выпуска
крем для наружного применения
Глюкозамин (глюкозамина сульфат, глюкозамина сульфата натрия хлорид)
таблетки, таблетки покрытые пленочной оболочкой, раствор для внутримышечного введения, порошок для приготовления раствора для приема внутрь
Хондроксид ® Максимум, «Фармаскин ТГК»
крем для наружного применения
Глюкозамин + ибупрофен + хондроитина сульфат
капсулы, таблетки покрытые пленочной оболочкой
гель для наружного применения
мазь для наружного применения
Глюкозамин + хондроитина сульфат + витамин Е
аэрозоль для наружного применения
крем для наружного применения
мазь для наружного применения
спрей для наружного применения дозированный
«Диклофенак», «Диклонат П», «Наклофен»,
гель для наружного применения
трансдермальная терапевтическая система, пластырь трансдермальный
гель для наружного применения
крем для наружного применения
гель для наружного применения
крем для наружного применения
аэрозоль для наружного применения
раствор для местного применения
гель для наружного применения
гель для наружного применения
трансдермальная терапевтическая система
Хондроксид ® Форте (мелоксикам+хондроитина сульфат&)
крем для наружного применения
мазь для наружного применения
гель для наружного применения
мазь для наружного применения
«Ваньтун Артиплас», «Перцовый пластырь Доктор перец с обезболивающим действием», «Перцовый пластырь» (белладонны листьев экстракт + перца стручкового плодов экстракт)
Витамины группы B
Дополнением к базовой анальгетической терапии может служить применение как «разогревающих», так и локальных «охлаждающих» средств, в частности трансдермальных систем на основе местных анестетиков (лидокаина и т. п.), блокирующих распространение болевых импульсов.
Разумный выбор НПВП при сочетанной патологии: заболеваниях суставов и гипертонической болезни
Нестероидные противовоспалительные препараты (НПВП) являются одной из основных групп лекарственных средств, применяемых при лечении ревматоидного артрита (РА). Противовоспалительный и анальгетический эффект данной группы препаратов связан с подавлением а
Нестероидные противовоспалительные препараты (НПВП) являются одной из основных групп лекарственных средств, применяемых при лечении ревматоидного артрита (РА). Противовоспалительный и анальгетический эффект данной группы препаратов связан с подавлением активности циклооксигеназы-2 (ЦОГ-2) в очаге воспаления — ключевого фермента синтеза простагландинов провоспалительной активности, а подавление изоформы ЦОГ-1 приводит к нарушению физиологических реакций: в частности, к нарушению синтеза простагландинов класса Е в слизистой оболочке желудка и развитию НПВП-гастропатии.
Большинство «стандартных» НПВП способно подавлять активность обеих изоформ ЦОГ, поэтому их применение часто ограничено из-за развития побочных эффектов, в первую очередь — со стороны желудочно-кишечного тракта (ЖКТ). Субъективные симптомы со стороны ЖКТ встречаются примерно у трети больных, а в 5% случаев представляют серьезную угрозу жизни пациентов. Именно поэтому в последние годы особо пристальное внимание привлекает проблема безопасного применения НПВП. Полагают, что препараты более селективные в отношении ЦОГ-2 реже вызывают развитие НПВП-гастропатии. Изучение механизмов действия НПВП послужило толчком к созданию новых препаратов, обладающих всеми положительными свойствами стандартных НПВП, но менее токсичных, — это специфические ингибиторы ЦОГ-2 [3, 4, 13].
В последние годы особую актуальность приобрела проблема взаимодействия НПВП и гипотензивных препаратов, а также связи между применением НПВП и развитием гипертонической болезни (ГБ). Неселективные НПВП могут привести к повышению АД (преимущественно диастолического) не только у больных артериальной гипертензией (АГ), но и у лиц с нормальным АД за счет ингибиции системного и локального, внутрипочечного синтеза простагландинов. Известно, что постоянный прием НПВП вызывает у пациентов увеличение АД в среднем на 5,0 мм рт. ст. Характерным свойством НПВП является также взаимодействие с гипотензивными препаратами, в основе гипотензивного действия которых лежат преимущественно простагландин-зависимые механизмы. Назначение НПВП пациентам, получающим по поводу АГ β-адреноблокаторы, ингибиторы АПФ и диуретики, приводит к снижению гипотензивного эффекта [8, 9].
Нимесулид был разработан еще в 1985 г. и является одним из первых НПВП, при изучении которого продемонстрирована более высокая селективность в отношении ЦОГ-2 и накоплен большой клинический опыт. В многочисленных исследованиях in vitro и in vivo было показано, что нимесулид примерно в 5–20 раз более селективно ингибирует ЦОГ-2, чем ЦОГ-1. Большой интерес представляет и тот факт, что нимесулид обладает широким спектром ЦОГ-независимых эффектов, которые могут определять его противовоспалительную, анальгетическую и хондропротективную активность [1, 2, 5, 7, 11, 12].
Нимесулид хорошо переносится больными и редко вызывает развитие серьезных побочных эффектов, требующих отмены препарата. По результатам ряда исследований, частота побочных эффектов, развивающихся на фоне приема нимесулида, достоверно не отличается от плацебо или ниже, чем при приеме других НПВП. Например, по данным мета-анализа, у больных, получавших нимесулид, общая частота побочных реакций со стороны ЖКТ была значительно ниже (8,7%), чем при назначении других НПВП (16,8%). Низкую частоту поражения ЖКТ на фоне лечения нимесулидом связывают не только с ЦОГ-2-селективностью препарата, но и с антигистаминным действием, приводящим к снижению секреции соляной кислоты в желудке [6, 10, 13].
Таким образом, нимесулид относится к селективным ингибиторам ЦОГ-2, сравним по эффективности с «классическими» НПВП, но отличается более благоприятным профилем токсичности. Фармакоэкономический анализ свидетельствует о преимуществах нимесулида по сравнению с диклофенаком, в первую очередь в связи с более низкой частотой поражения ЖКТ.
Целью нашего исследования явилось изучение эффективности и переносимости найза (нимесулида) у больных РА в сравнении с ортофеном (диклофенаком).
Материалы и методы
Оба НПВП назначались случайным способом 40 больным с момента первого установления диагноза РА, согласно критериям Американской коллегии ревматологов. Найз применялся в виде таблеток по 100 мг дважды в день, ортофен — в виде таблеток по 25 мг в суточной дозе 150 мг. Одновременно всем больным проводилась базисная терапия, преимущественно метотрексатом или сульфасалазином. Эффективность и переносимость НПВП оценивались через 3 нед. от начала лечения, т. е. в те сроки, когда эффект базисных препаратов еще не имел клинической значимости.
В I группе из 20 пациентов, получавших найз, было 14 женщин и 6 мужчин, средний возраст пациентов составил 55,1 года, длительность суставного синдрома к моменту установления диагноза — от 3 до 14 мес., в среднем — 7,25 мес. Во II группе из 20 больных, получавших ортофен, было 18 женщин и 2 мужчин, средний возраст больных — 42,75 года, длительность суставного синдрома — от 2 до 14 мес., в среднем — 5,65 мес. Клиническая характеристика обеих групп представлена в таблице 1.
Результаты лечения оценивались по динамике показателей суставного синдрома (суставной индекс Ричи (СИ), счет болезненных суставов (СБС), счет припухших суставов (СПС), продолжительность утренней скованности (мин), выраженность боли по визуально-аналоговой шкале (ВАШ)) и на основании общей оценки эффективности лечения, по мнению врача и больного. Кроме того, у всех больных оценивалась динамика АД на фоне лечения НПВП.
Результаты
В I группе на фоне лечения найзом в суточной дозе 200 мг за 3 нед. лечения достигнута достоверная динамика показателей суставного синдрома. При этом эффективность терапии оценена 17 пациентами (85%) как хорошая и 3 (15%) — как удовлетворительная. По мнению врача, в 16 случаях (80%) наблюдалась хорошая эффективность препарата, в 4 случаях (20%) — удовлетворительная (рис. 1). Переносимость найза у 85% была хорошей, только у 2 больных (10%) отмечались изжога и гастралгии, у 1 больного (5%) — чувство тяжести в эпигастральной области. Однако при фиброгастроскопии у этих пациентов не выявлено эрозивного повреждения слизистой оболочки желудка. В группе больных, принимавших найз, не потребовалось отмены препарата ни у одного больного.
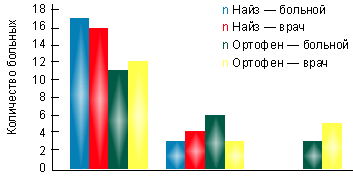 |
| Рисунок. Оценка эффективности препаратов на основании мнения больного и врача |
Во II группе на фоне терапии ортофеном в суточной дозе 150 мг через 3 нед. также отмечена существенная динамика показателей суставного синдрома. Однако оценка эффективности терапии показала, что только 11 пациентов (55%) оценили эффективность препарата как хорошую, 6 (30%) — как удовлетворительную и трое больных (15%) признали ее неудовлетворительной. По мнению лечащего врача, достаточная эффективность ортофена, соответствующая градации «хорошая», отмечалась в 12 случаях (60%), удовлетворительная — в 3 (15%) и неудовлетворительная — в 5 (25%) случаях (рис.).
Переносимость препарата ортофен была хуже, чем у найза: у 9 пациентов (45%) отмечались симптоматические побочные эффекты, причем у 3 больных (15%) потребовалась отмена препарата через 2 нед. от начала лечения в связи с выявленным при ФГДС эрозивным поражением слизистой оболочки антрального отдела желудка. В целом из побочных эффектов чаще отмечались изжога — у 7 (35%) пациентов, гастралгии — у 8 (40%), тошнота — у 4 (20%) и диарея — у 2 (10%) больных.
Особый интерес представляет влияние исследуемых НПВП на уровень АД, так как из 40 больных у 15 имелась сопутствующая ГБ, по поводу которой проводилась гипотензивная терапия. Динамика уровня АД в обеих группах на фоне лечения найзом и ортофеном представлена в таблице 2. Следует отметить, что терапия найзом не требовала усиления проводимой гипотензивной терапии (β-блокаторами, ингибиторами АПФ, диуретиками) и не вызывала повышения АД у ранее нормотензивных пациентов. В то же время лечение ортофеном потребовало коррекции доз гипотензивных препаратов у 4 (66,7%) из 6 больных ГБ и вызвало повышение АД у 5 (25%) женщин в постменопаузе с исходно высоконормальным АД. Данный эффект неселективного НПВП — ортофена — следует считать предсказуемым, особенно с учетом характера проводимой гипотензивной терапии. Все больные ГБ получали в разных комбинациях β-адреноблокаторы, ингибиторы АПФ и диуретики; при этом ни одному пациенту не был назначен дигидропиридиновый антагонист Са — амлодипин, который является препаратом выбора для лечения АГ в условиях терапии НПВП.
Таким образом, результаты открытого клинического исследования показали, что препарат найз у больных РА проявляет выраженную противовоспалительную активность, превосходящую диклофенак. При этом найз характеризуется хорошей переносимостью, малым числом симптоматических побочных эффектов и превосходит с этой точки зрения наиболее широко применяемый в клинической практике ортофен. Дополнительным преимуществом препарата найз можно считать менее выраженное влияние на уровень АД. При назначении найза не требовалось увеличения дозы гипотензивных препаратов. С учетом высокой распространенности эссенциальной гипертензии в популяции, взаимодействие НПВП с наиболее часто используемыми гипотензивными средствами представляется актуальной проблемой. Ревматические заболевания, требующие постоянной терапии НПВП, часто сочетаются с АГ. При этом у большинства больных ГБ коррекция АД может достигаться только благодаря комбинированной антигипертензивной терапии, а монотерапия дигидропиридиновыми антагонистами Са признается недостаточно эффективной. Следовательно, в большинстве случаев при лечении воспалительных ревматических заболеваний у лиц, страдающих ГБ, невозможно полностью нивелировать отрицательное взаимодействие «стандартных» НПВП с основными кардиологическими препаратами — β-адреноблокаторами, ингибиторами АПФ и диуретиками. В такой ситуации представляется рациональным выбор для проведения противовоспалительной терапии специфических ингибиторов ЦОГ-2, представителем которых является найз.
Литература
И. М. Марусенко, кандидат медицинских наук
Н. Н. Везикова, кандидат медицинских наук, доцент
В. К. Игнатьев, доктор медицинских наук, профессор
Петрозаводский университет, кафедра госпитальной терапии
Нестероидные противовоспалительные препараты: список и цены
Нестероидные противовоспалительные препараты используются достаточно широко для подавления воспалительных процессов в организме. НПВП доступны в различных формах выпуска: таблетки, капсулы, мази. Они обладают тремя основными свойствами: жаропонижающими, противовоспалительными и болеутоляющими.
Лучший нестероидный противовоспалительный препарат может подобрать только врач, отталкиваясь от индивидуальных особенностей пациента. Самолечение в данном случае может быть чревато развитие серьезных побочных реакций или же передозировки. Предлагаем ознакомиться со списком препаратов. Рейтинг разработан на основании соотношения цена-качество, отзывов пациентов и мнения специалистов.
Как работают НПВП?
Нестероиды ингибируют агрегацию тромбоцитов. Терапевтические свойства объясняются блокадой фермента циклооксигеназы (ЦОГ-2), а также снижением синтеза простагландина. По мнению специалистов они оказывают влияние на симптомы заболевания, но не устраняют причину его возникновения. Поэтому не следует забывать о средствах, с помощью которых должны быть устранены первичные механизмы развития патологии.
Если у пациента обнаружена непереносимость НПВП, тогда они заменяются лекарствами других категорий. Часто в таких случаях применяют комбинацию противовоспалительного и болеутоляющего средства.
Как показывает практика, нецелесообразно заменять одно лекарство другим той же группы, если при приеме обнаруживается недостаточный терапевтический эффект. Удвоение дозы может привести только к клинически незначительному увеличению воздействия.
Классификация НПВП
Нестероидные противовоспалительные средства классифицируются в зависимости от того, являются ли они селективными для ЦОГ-2 или нет. Таким образом, с одной стороны, есть неселективные НПВП, а с другой – селективные ЦОГ-2.
Сравнительная эффективность и безопасность применения кетопрофена, лорноксикама, нимесулида и целекоксиба у больных остеоартрозом
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
Нестероидные противовоспалительные препараты (НПВП) в настоящее время остаются основными лекарственными препаратами, а в ряде случаев и единственными лекарственными средствами, применяемыми для лечения остеоартроза (ОА). Однако их использование сопряжено с развитием нежелательных явлений со стороны желудочно–кишечного тракта [1–5], печени [6–9]. Описан прогипертензивный эффект НПВП [10–13], неблагоприятное влияние на течение сердечной недостаточности [14–16], ухудшение клубочковой фильтрации. Такие системные побочные реакции связаны с ингибированием циклооксигеназы (ЦОГ), одного из ключевых ферментов в синтезе простагландинов – тканевых гормонов, регулирующих функции различных органов и функциональных систем. В связи с этим целью нашей работы было изучение соотношения клинической эффективности и безопасности различных НПВП, являющихся неспецифическими ингибиторами ЦОГ и специфическими ингибиторами ЦОГ–2 активности.
Материалы и методы: исследование клинической эффективности и безопасности НПВП проводилось в четырех группах больных: 1–я – 24 больных ОА, принимавших лорноксикам по 8 мг 2 раза в сутки; 2–я – 37 больных ОА, принимавших нимесулид по 100 мг 2 раза в сутки; 3–я – 23 больных ОА, принимавших кетопрофен ( Кетонал форте , фармацевтическая компания Лек) по 100 мг 2 раза в сутки; и 4–я группа – 48 больных, принимавших целекоксиб по 200 мг 2 раза в сутки. Диагноз ОА устанавливался по критериям Американского ревматологического колледжа (ACR, 1987), стадия ОА определялась по Kellgren– Lawrence. Клиническая характеристика больных представлена в таблице 1. Все группы больных по своей клинико–демографической характеристике не отличались друг от друга. Средний возраст больных превышал 60 лет (большинство из них – женщины), в равной степени были поражены коленные и тазобедренные суставы, поражения суставов были II и III стадии по Kellegren и Lawrence. Клиническая эффективность лечения ОА оценивалась по динамике индекса WOMAC, противовоспалительный эффект – по уровню С–реактивного белка (СРБ). Безопасность НПВП оценивалась по данным клинического наблюдения за больными, эзофагогастродуоденоскопии, суточного мониторирования АД, данным лабораторного обследования (общий анализ крови, анализ мочи, биохимического исследования крови (билирубин, АСТ, АЛТ, ЩФ, ГГТП, СРБ). Все исследования проводились до начала терапии и по ее окончании.
До начала исследования группы больных достоверно не отличались по интенсивности клинических проявлений ОА по индексу WOMAC (табл. 2). На фоне проводимого лечения у больных уменьшилась боль, увеличилась подвижность в суставах, уменьшились затруднения в повседневной жизни. Произошло достоверное уменьшение всех составляющих индекса WOMAC. Динамика анальгетического эффекта имела определенные особенности в зависимости от проводимой лекарственной терапии (рис. 1). При применении кетопрофена достоверный клинический эффект наступал уже к 3–4 дню лечения, а на фоне лечения нимесулидом, лорноксикамом и целекоксибом – к 7–10 дню лечения. Положительный клинический эффект подтверждается уменьшением активности воспаления; во всех группах больных отмечалось достоверное снижение уровня СРБ (табл. 4).
Одним из основных осложнений в наблюдаемой группе больных была гастропатия, которая развилась у 28 (21%) больных. Клинические варианты гастропатии у больных, принимающих различные НПВП, представлены в таблице 3. Чаще всего гастропатия развивалась на фоне приема лорноксикама (у 66% больных), значительно реже – у больных, принимавших нимесулид (13,5%), кетопрофен (13%) и целекоксиб (8,3%). Наиболее тяжелые варианты гастропатии (язвы желудка и 12–перстной кишки) развились у 4 (16,7%) больных на фоне приема лорноксикама, причем у одного из пациентов диагностировано два язвенных дефекта в 12–перстной кишке. У 10 больных лечение НПВП осложнилось гепатопатией. Поражение печени по данным лабораторных исследований (табл. 4) развилось у 4 (16,7%) больных, принимавших лорноксикам и 6 (16,2%) больных на фоне приема нимесулида. Клинические проявления гепатопатии: тяжесть в правом подреберье, тошнота, увеличение печени (по данным УЗИ) отмечались у 2 (8,3%) больных, принимавших лорноксикам, и у 2 (5,4%) больных на фоне лечения нимесулидом. На фоне приема кетопрофена и целекоксиба достоверной динамики функциональных проб печени не отмечалось. Прогипертензивный эффект НПВП оценивался по изменению показателей суточного мониторирования АД (табл. 5). Применение лорноксикама и нимесулида приводило к повышению среднего систолического и диастолического давления. При применении этих препаратов также достоверно возрастал уровень пульсового давления и нагрузка давления (по данным индекса времени систолического и диастолического артериального давления). Все это свидетельствует, что лорноксикам и нимесулид обладают прогипертензивным эффектом. Их применение у наблюдаемой группы больных привело к достоверному прогипертензивному эффекту – повышению АД более чем на 5%. У 6 (25%) больных на фоне приема лорноксикама и у 7 (19%) больных при приеме нимесулида уровень АД превысил нормальные значения по данным суточного мониторировании АД, что привело к клинически значимой артериальной гипертензии. У больных, принимавших кетопрофен или целекоксиб, достоверных изменений показателей суточного мониторирования не отмечалось. Суммарное число побочных осложнений и количество больных с нежелательными реакциями на фоне приема НПВП представлено в таблице 6. Оценивая безопасность применения НПВП, необходимо учитывать все побочные эффекты, которые могут возникнуть у больных. В большинстве исследований проводится анализ нежелательных явлений только со стороны органов пищеварения или сердечно–сосудистой системы. Однако побочные реакции могут суммироваться как в группе, так и у одного больного. Полученные нами результаты свидетельствуют о том, что при изучении всех возможных побочных реакций процент больных, у которых применение НПВП может вызвать осложнения, гораздо выше. Так, среди больных, принимавших лорноксикам, нежелательные реакции отмечались у 87,5% больных, на фоне применения нимесулида нежелательные реакции отмечались в 29,7% случаев. Наиболее безопасными препаратами являлись кетопрофен и целекоксиб. Появление побочных реакций при приеме НПВП обусловлено ингибированием ЦОГ, одного из ключевых ферментов синтеза простагландинов – тканевых гормонов, регулирующих не только функции отдельных органов и систем, но и отдельной клетки. Появление селективных ингибиторов ЦОГ позволило уменьшить число нежелательных реакций, но индивидуальные особенности препарата влияют как на клиническую эффективность лечения, так и на появление побочных осложнений. В нашем исследовании селективный ингибитор ЦОГ–2 нимесулид показал большее количество побочных реакций, чем неселективный ингибитор ЦОГ кетопрофен. Вероятно, ингибирование фосфодиэстераз, которое отмечается при применении нимесулида, приводит к нарушению внутриклеточного обмена цАМФ и тем самым способствует возникновению побочных реакций со стороны печени и прогипертензивному эффекту нимесулида. В свою очередь, кетопрофен, благодаря своим уникальным свойствам и способности оказывать центральный анальгетический эффект, быстрее всех НПВП приводит к купированию болевого синдрома. Особенности фармакокинетики кетопрофена, короткий период полувыведения, вероятно, не приводят к значительному снижению уровня простагландинов, что и обусловливает небольшое количество побочных реакций при его применении. Применение НПВП при остеоартрозе требует от врача повышенного внимания к больному, так как в основном это больные пожилого возраста, страдающие другими заболеваниями, в том числе артериальной гипертензией, язвенной болезнью, рефлюкс эзофагитом, болезнями печени. Все это увеличивает риск побочных реакций. В связи с этим подбор НПВП необходимо проводить строго индивидуально, с учетом всех возможных нежелательных реакций (даже очень редко встречающихся в общей популяции). По нашим данным, наилучшим сочетанием эффективность/безопасность обладают: среди неселективных НПВП – кетопрофен, а среди селективных ингибиторов ЦОГ–2 – целекоксиб.




