Кеторол или найз что лучше
Как защитить желудок от НПВП — советы эксперта
Что вы делаете, когда болит голова, поднялась высокая температура или беспокоит боль в суставах? 90% опрошенных ответят: «Пью таблетку».
«Волшебные» пилюли
Существует группа препаратов, под общим названием нестероидные противовоспалительные (НПВП), которые мы все хотя бы раз в жизни, а многие регулярно, принимали. Это препараты, обладающие обезболивающим противовоспалительным и / или жаропонижающим действием. В качестве примера можно назвать Аспирин, Нурофен, Найс, Кетанов, Кетопрофен и прочие. Учитывая «волшебные эффекты» от их действия — снятие воспаления, боли и жара, — их назначают практически все, всем и всегда. Назначают травматологи, ревматологи, терапевты, лоры, стоматологи. Плюс, их можно совершенно свободно приобрести в любой аптеке. Но, наряду с «волшебными свойствами» эти лекарства обладают рядом побочных действий, которые можно разделить на 2 группы: кардиориски и гастро риски. Собственно о гастрорисках и пойдёт речь в данной статье.
НПВП-гастропатия
В научной литературе эта проблема называется «НПВП-гастропатия». Впервые термин был предложен в 1986 году для разграничения специфического поражения слизистой оболочки желудка, возникающего при длительном употреблении НПВП, от классической язвенной болезни.
Отличие НПВП-гастропатии от язвенной болезни можно проследить и по зоне поражения. Чаще всего язвы можно увидеть в желудке, а не в кишке. Плюс, изменения встречаются чаще у пожилых, а не у молодых людей.
Немного цифр
Немного статистики. В Великобритании назначается около 24 млн. НПВС в год. 70% лиц старше 70 лет принимают НПВС 1 раз в неделю, а 34% ежедневно. В США продается НПВС на сумму до 6 млрд. в год. Как следствие, риск развития желудочно-кишечных кровотечений (ЖКК) возрастает прободения — в 6 раз, риск смерти от осложнений до 8 раз. До всех случаев острых ЖКК связаны с НПВС.
Проблема эта актуальна и в нашей стране, к примеру по данным Научного Центра сердечно-сосудистой хирургии им. А.Н. Бакулева из 240 больных, ежедневно принимающих аспирин даже в малых дозах, на гастроскопии поражения желудка и 12 п.к выявлены у 30% (из них язвы — у 23,6%, эрозии — у 76,4%). Аналогичная картина у коллег из ВНИИ ревматологии РАМН — у 2126 пациентов, принимающих НПВС без «прикрытия» (защиты) желудка, эрозии и язвы гастродуоденальной зоны найдены в 33,8% случаев. Это очень впечатляющие и драматические цифры осложнений от приема НПВС, учитывая количество употребляющих эти препараты людей в развитых странах.
Как это работает?
Как же действуют эти препараты в наших желудках? Всё очень просто, негативное воздействие реализуется за счёт дисбаланса защитных и агрессивных сил. У нас в желудке существует ряд защитных механизмов, позволяющих противостоять натиску агрессоров. Среди последних:
Защищается желудок за счет мощного слоя слизи и бикарбонатов, которые нейтрализуют кислоту, адекватного кровоснабжения, способности очень быстро регенерировать. Когда мы используем НПВС препараты, баланс сил изменяется в сторону агрессивных механизмов и происходит поражение слизистого и подслизистого слоя желудка и кишки.
Диагностика
Для диагностики подобных изменений используется гастроскопия, являющаяся «золотым стандартом». Интересный факт, дело в том, что порядка 40% больных с эрозивно-язвенными изменениями, принимающих эти препараты длительно (более 6 недель) не ощущают никакого дискомфорта или неприятных, болезненных ощущений. Проблемы с желудком диагностируются лишь при походе к другим врачам, а не к гастроэнтерологу. И, наоборот, у 40% пациентов, на фоне жалоб, которые они предъявляют, ничего не находят.
Что же делать в таком случае?!
Алгоритм действий для пациентов, не имеющих проблем с желудком, и тех, у кого в анамнезе была язвенная болезнь или эрозивные изменения, различен. Для первой группы, при назначении нестероидных противовоспалительных препаратов более, чем на 5 дней, обязательно назначение препаратов из группы ингибиторов протонной помпы (ИПП). Таких как, омепразол, пантопразол, рабепразол и т. д. (на весь курс приема). Для второй группы, любые назначения из группы НПВС, независимо от срока приёма, требуют параллельного назначения ингибиторов протонной помпы. Так же обязателен прием ИПП пациентам, принимающих длительно аспирин.
Мифы, с которыми мы сталкиваемся в ежедневной практике
Миф 1. Использование НПВС препаратов в виде свечей является менее агрессивным для желудка, нежели приём таблеток
Это 100% миф. Патогенное, разрушительное действие лекарства реализуется через кровь, доставляющую его по сосудам в желудок.
Миф 2. В качестве «гастропротекторов» можно использовать лекарства из группы антацидов — Ренни, Маалокс, Фосфалюгель и H2-блокаторы (Ранитидин и Фамотидин)
В данном случае они не эффективны.
Миф 3. Принимать ингибиторы протонной помпы можно нерегулярно
Дело в том, что если пожилому человеку назначили на всю жизнь противовоспалительный препарат, абсолютно бессмысленно назначать гастропротекцию на месяц. В подобных случаях лекарства должны приниматься строго параллельно.
Миф 4. В качестве «гастропротекторов» могут выступать пищевые продукты (кисели и пр.)
Этот миф, как абсолютно фантастический, мы оставим без комментариев.
Как выбрать лекарство
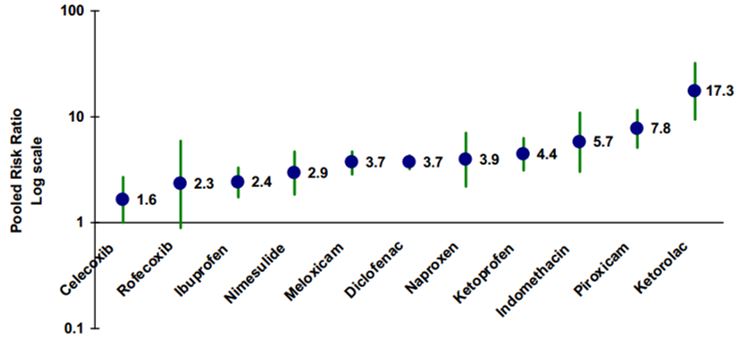
На самом деле, самым важным моментом является то, какие именно лекарства мы принимаем. На рисунке можно увидеть шкалу агрессивности различных препаратов из группы НПВС по отношению к желудку.
Самыми агрессивными препаратами являются Аспирин, Кеторолак, Пироксикам, Индометацин. По возможности рекомендуется использовать селективные препараты, которые обладают минимальными гастро-рисками. Их применение всегда более желательно, к ним относится Целекоксиб и Рофекоксиб. Но несмотря на их относительную безопасность, назначать их должен строго по показаниям лечащий доктор, не забывайте об этом.
Про Helicobacter pylori
Еще одним очень важным компонентом профилактики осложнений, является диагностика инфекции Helicobacter pylori у пациента планирующего длительно принимать НПВС (особенно аcпирин). Наличие бактерии увеличивает риски эрозивно-язвенных поражений ЖКТ и кровотечения в При её выявлении должна в обязательном порядке проводится эрадикация (уничтожение этой бактерии).
Резюме
Итак делаем выводы:
Таблетки для снятия зубной боли
Таблетки для снятия зубной боли
В большинстве случаев первое, что делают люди при возникновении боли, – пьют таблетки. Это самый привычный и доступный способ избавиться от неприятных ощущений. Конечно, идеальным решением было бы обратиться к врачу, но ситуации бывают разные: времени нет, клиники закрыты (зуб заболел ночью), финансовое положение и др. Приводим список наиболее эффективных средств от зубной боли и надеемся, что вы их будете использовать только в крайнем случае.
Обзор обезболивающих средств
Выпускается в форме таблеток, гранул, суспензий. Рекомендуется при зубной боли слабой и средней интенсивности.
Выпускается в различных формах. Подходит для слабой и умеренной боли.
Выпускается в виде таблеток и капсул для инъекций. Поможет снять среднюю и сильную боль. Максимальная доза в сутки – 3 таблетки
Выпускается в форме таблеток. Рекомендуется при слабой и средней выраженности боли.
Обладает противовоспалительным и жаропонижающим действием. Не раздражает слизистую желудка.
Выпускается в виде таблеток, суспензии и геля (для наружного применения).
Выпускается в форме таблеток. Помогает снять умеренную зубную боль.
Выпускается в различных формах.
Максимальная доза в сутки – 4 таблетки.
«Помните, что таблетка – это временный способ избавления от боли. Действие препарата пройдет, и боль может вернуться, потому что сама причина не устранена. Если после первых «звоночков» вы не обратились к стоматологу, то заболевание продолжит прогрессировать. С каждым разом боль будет все сильнее и сильнее»
Ирина Виноградова,
Стоматолог-терапевт, эндодонтист, завотделением терапии и пародонтологии, член медсовета сети клиник «СТОМПРАКТИКА.РФ»
Недостатки таблеток
У обезболивающих есть и обратная сторона: практически все таблетки имеют побочные эффекты.
Большинство анальгетиков запрещено принимать будущим и кормящим мамам, маленьким детям и людям, имеющим системные заболевания, которые входят в список противопоказаний. Поэтому перед применением рекомендуется посоветоваться с врачом.
Болеутоляющие для беременных и кормящих мам
В таких ситуациях выбор любого лекарства должен быть одобрен гинекологом и педиатром. Если зубную боль терпеть невозможно, разрешается однократно принять ½ дозу парацетамола, при условии в скором времени обратиться к врачу.
Сравнительная эффективность нестероидных противовоспалительных препаратов при болях в спине
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
В настоящее время боли в спине (БС) широко распространены, а в развитых странах, по данным экспертов ВОЗ, сравнимы с неинфекционной эпидемией, что в большинстве случаев связано с возрастающими нагрузками на человека [4]. Высокая инвалидизация лиц трудоспособного возраста вследствие поражений опорно-двигательного аппарата возводит проблему лечения БС в ранг актуальной. Популяционные исследования выявили ассоциацию болей в нижней части спины (БНС) с такими факторами, как пол и возраст, осанка, мышечная сила, подвижность позвоночника. В недавно проведенном в Швеции популяционном исследовании спинальных болей среди лиц в возрасте 35-45 лет установлено, что частота возникновения болей за последний год составила 66,3%, причем данный показатель среди женщин был незначительно выше, чем среди мужчин. У 25% респондентов возникли существенные проблемы с трудоспособностью, степенью нарушения функционального статуса. В Великобритании вследствие болей в спине в 1992 г. было потеряно 90 миллионов рабочих дней, что уступало только заболеваниям органов дыхания и кровообращения. При этом 75% больных составили пациенты от 30 до 59 лет, то есть в период максимальной трудоспособности.
Все случаи болей в спине делятся на первичные и вторичные.
Вторичный синдром БС может быть связан с врожденными аномалиями, травматическими поражениями позвоночника, опухолевыми и инфекционными процессами, остеопорозом, заболеваниями внутренних органов.
БС чаще всего развивается в возрасте от 20 до 50 лет (пик заболеваемости в возрасте от 35 до 45 лет). Именно в этой возрастной группе обычно диагностируют первичный (механический) синдром БС, тогда как у больных моложе 20 лет и старше 50 лет преобладает вторичный синдром БС (табл. 1).
Диагностика БС требует участия врачей разных специальностей: терапевта, ревматолога, невропатолога, ортопеда и хирурга, задачей которых, в частности, является исключение вторичного характера болей в нижней части спины.
Провоцирующими факторами острого течения БС могут быть травма, подъем непосильного груза, неподготовленные движения, длительное пребывание в нефизиологической позе, переохлаждения. Хроническая боль может возникать как после регресса острой боли, так и независимо от нее.
Лечение проводится с учетом формы заболевания и варианта его течения с использованием консервативного и хирургического подходов.
В настоящее время показания к хирургическому лечению сужены, поскольку накопились факты о том, что даже при очень хорошей методике хирургической декомпрессии и стабилизации заболевание склонно рецидивировать.
При обострении клинических проявлений БС ранее рекомендовался отдых в течение нескольких недель. Однако во всех исследованиях последних лет подчеркивается, что не постельный режим, а ранняя активизация больных должна быть главным компонентом программы лечения, что способствует улучшению питания межпозвонкового диска, в связи с чем постельный режим при остром течении ограничивается несколькими днями.
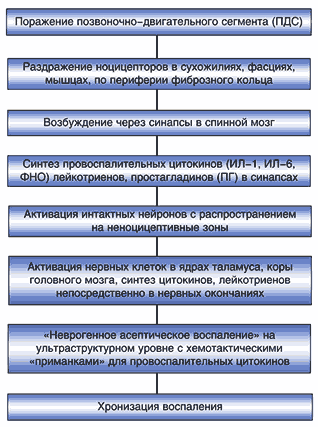
Дегенеративный процесс в межпозвонковом диске активирует ноцицепторы по периферии фиброзного кольца, в сухожилиях, фасциях, мышцах с последующей передачей импульсов в спинной мозг. При этом запускаются иммунные и биохимические реакции, завершающиеся формированием асептического нейрогенного воспаления. В связи с этим целесообразность назначения НПВП обоснована (схема 1) [3].
Схема 1. Механизмы асептического неврогенного воспаления при спондилоартрозе (Borenstein D., 2000).
В настоящее время появилась возможность применения такого НПВП, как кетопрофен (Кетонал) при остеоартрозе, а также при лечении болей в спине. Кетопрофен является производным пропионовой кислоты. Особенностью его противовоспалительного действия является не только ингибирование синтеза простагландинов на уровне циклооксигеназы; он также ингибирует липооксигеназу, обладает антибрадикининовой активностью, стабилизирует лизосомальные мембраны. При приеме внутрь препарат быстро и максимально полно абсорбируется из желудочно-кишечного тракта. Максимальная концентрация в крови достигается через 1-2 часа. Кетонал хорошо проникает в синовиальную жидкость и соединительную ткань. Значимые уровни концентраций достигаются уже через 15 минут после однократного внутримышечного введения 100 мг кетопрофена. Важным преимуществом препарата является то, что он представлен различными лекарственными формами: капсулами, таблетками форте и ретард, раствором для внутримышечных инъекций, кремом и суппозиториями.
Кетонал обладает «сбалансированной» активностью в отношении ингибиции ЦОГ-1 и ЦОГ-2, что позволяет оптимально сочетать высокую эффективность с хорошей переносимостью, сравнимой, по данным ряда авторов, с переносимостью селективных НПВП [3,5]. Исследователи связывают мощный болеутоляющий эффект Кетонала с его доказанным центральным воздействием, которое реализуется на уровне задних рогов спинного мозга, а также за счет непосредственного влияния на таламические центры болевой чувствительности, что, по-видимому, связано с угнетением синтеза простагландинов в ЦНС [4,5].
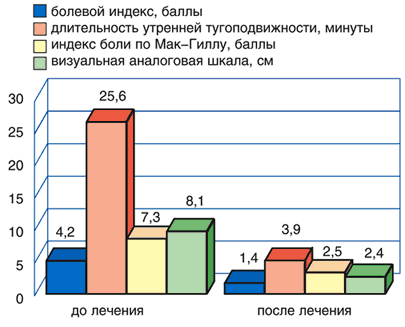
Рис. 1. Динамика клинических показателей у пациентов с болями в спине до и после лечения Кетоналом форте
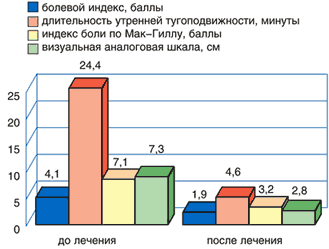
Рис. 2. Динамика клинических показателей у пациентов с болями в спине до и после лечения диклофенаком
Оценки эффективности лечения больным и врачом практически не отличались друг от друга и свидетельствовали о выраженной клинической эффективности препаратов. Высокая эффективность отмечена у 93,3% пациентов, принимавших Кетонал форте, у 73,3% пациентов, принимавших диклофенак.
Переносимость препарата «хорошая» или «очень хорошая» была отмечена у 80% больных, принимавших Кетонал, и у 64% принимавших диклофенак. Основными побочными эффектами при приеме как диклофенака, так и Кетонала были изжога, дискомфорт в эпигастральной области. Прекращение лечения потребовалось лишь в 1 случае, когда у пациента развилась крапивница на фоне приема диклофенака, которая была расценена, как побочный эффект средней степени тяжести.
Таким образом, в настоящее время лечение болей в спине оптимизировано использованием препаратов группы НПВП, в частности, Кетонала, в силу его высокой эффективности, проявляющейся отчетливо выраженной положительной динамикой с регрессом болевых проявлений у пациентов с БС.
1. Клинические рекомендации для практических врачей, основанные на доказательной медицине. Изд. дом «ГЭОТАР-МЕД», 2001, с. 606-611.
2. Насонов Е.Л. Нестероидные противовоспалительные препараты (перспективы применения в медицине). М., 2000, 262.
3. Насонов Е.Л., Чичасова Н.В., Шмидт Е.И. Перспективы применения неселективных нестероидных противовоспалительных препаратов (на примере кетопрофена) и селективных ингибиторов ЦОГ-2 в клинической практике. Русский медицинский журнал, том 10, №22, 2002, с 1014-1017.
4. Ветшев П.С., Ветшева М.С. Принципы аналгезии в раннем послеоперационном периоде. Хирургия, 2002, №12, с. 49-52.
5. Чичасова Н.В., Насонов Е.Л., Имаметдинова Г.Р. Применение кетопрофена (кетонал) в медицинской практике. Фарматека, 2003, №5, с. 30-32.
6. Borenstein D. «Эпидемиология, этиология, диагностическая оценка и лечение поясничной боли». Междун. Медиц. Журнал, 2000, №35, с. 36-42.
7. WHO. Department of noncomunicable disease menagement. Low back pain iniciative. Geneve.1999.
Разумный выбор НПВП при сочетанной патологии: заболеваниях суставов и гипертонической болезни
Нестероидные противовоспалительные препараты (НПВП) являются одной из основных групп лекарственных средств, применяемых при лечении ревматоидного артрита (РА). Противовоспалительный и анальгетический эффект данной группы препаратов связан с подавлением а
Нестероидные противовоспалительные препараты (НПВП) являются одной из основных групп лекарственных средств, применяемых при лечении ревматоидного артрита (РА). Противовоспалительный и анальгетический эффект данной группы препаратов связан с подавлением активности циклооксигеназы-2 (ЦОГ-2) в очаге воспаления — ключевого фермента синтеза простагландинов провоспалительной активности, а подавление изоформы ЦОГ-1 приводит к нарушению физиологических реакций: в частности, к нарушению синтеза простагландинов класса Е в слизистой оболочке желудка и развитию НПВП-гастропатии.
Большинство «стандартных» НПВП способно подавлять активность обеих изоформ ЦОГ, поэтому их применение часто ограничено из-за развития побочных эффектов, в первую очередь — со стороны желудочно-кишечного тракта (ЖКТ). Субъективные симптомы со стороны ЖКТ встречаются примерно у трети больных, а в 5% случаев представляют серьезную угрозу жизни пациентов. Именно поэтому в последние годы особо пристальное внимание привлекает проблема безопасного применения НПВП. Полагают, что препараты более селективные в отношении ЦОГ-2 реже вызывают развитие НПВП-гастропатии. Изучение механизмов действия НПВП послужило толчком к созданию новых препаратов, обладающих всеми положительными свойствами стандартных НПВП, но менее токсичных, — это специфические ингибиторы ЦОГ-2 [3, 4, 13].
В последние годы особую актуальность приобрела проблема взаимодействия НПВП и гипотензивных препаратов, а также связи между применением НПВП и развитием гипертонической болезни (ГБ). Неселективные НПВП могут привести к повышению АД (преимущественно диастолического) не только у больных артериальной гипертензией (АГ), но и у лиц с нормальным АД за счет ингибиции системного и локального, внутрипочечного синтеза простагландинов. Известно, что постоянный прием НПВП вызывает у пациентов увеличение АД в среднем на 5,0 мм рт. ст. Характерным свойством НПВП является также взаимодействие с гипотензивными препаратами, в основе гипотензивного действия которых лежат преимущественно простагландин-зависимые механизмы. Назначение НПВП пациентам, получающим по поводу АГ β-адреноблокаторы, ингибиторы АПФ и диуретики, приводит к снижению гипотензивного эффекта [8, 9].
Нимесулид был разработан еще в 1985 г. и является одним из первых НПВП, при изучении которого продемонстрирована более высокая селективность в отношении ЦОГ-2 и накоплен большой клинический опыт. В многочисленных исследованиях in vitro и in vivo было показано, что нимесулид примерно в 5–20 раз более селективно ингибирует ЦОГ-2, чем ЦОГ-1. Большой интерес представляет и тот факт, что нимесулид обладает широким спектром ЦОГ-независимых эффектов, которые могут определять его противовоспалительную, анальгетическую и хондропротективную активность [1, 2, 5, 7, 11, 12].
Нимесулид хорошо переносится больными и редко вызывает развитие серьезных побочных эффектов, требующих отмены препарата. По результатам ряда исследований, частота побочных эффектов, развивающихся на фоне приема нимесулида, достоверно не отличается от плацебо или ниже, чем при приеме других НПВП. Например, по данным мета-анализа, у больных, получавших нимесулид, общая частота побочных реакций со стороны ЖКТ была значительно ниже (8,7%), чем при назначении других НПВП (16,8%). Низкую частоту поражения ЖКТ на фоне лечения нимесулидом связывают не только с ЦОГ-2-селективностью препарата, но и с антигистаминным действием, приводящим к снижению секреции соляной кислоты в желудке [6, 10, 13].
Таким образом, нимесулид относится к селективным ингибиторам ЦОГ-2, сравним по эффективности с «классическими» НПВП, но отличается более благоприятным профилем токсичности. Фармакоэкономический анализ свидетельствует о преимуществах нимесулида по сравнению с диклофенаком, в первую очередь в связи с более низкой частотой поражения ЖКТ.
Целью нашего исследования явилось изучение эффективности и переносимости найза (нимесулида) у больных РА в сравнении с ортофеном (диклофенаком).
Материалы и методы
Оба НПВП назначались случайным способом 40 больным с момента первого установления диагноза РА, согласно критериям Американской коллегии ревматологов. Найз применялся в виде таблеток по 100 мг дважды в день, ортофен — в виде таблеток по 25 мг в суточной дозе 150 мг. Одновременно всем больным проводилась базисная терапия, преимущественно метотрексатом или сульфасалазином. Эффективность и переносимость НПВП оценивались через 3 нед. от начала лечения, т. е. в те сроки, когда эффект базисных препаратов еще не имел клинической значимости.
В I группе из 20 пациентов, получавших найз, было 14 женщин и 6 мужчин, средний возраст пациентов составил 55,1 года, длительность суставного синдрома к моменту установления диагноза — от 3 до 14 мес., в среднем — 7,25 мес. Во II группе из 20 больных, получавших ортофен, было 18 женщин и 2 мужчин, средний возраст больных — 42,75 года, длительность суставного синдрома — от 2 до 14 мес., в среднем — 5,65 мес. Клиническая характеристика обеих групп представлена в таблице 1.
Результаты лечения оценивались по динамике показателей суставного синдрома (суставной индекс Ричи (СИ), счет болезненных суставов (СБС), счет припухших суставов (СПС), продолжительность утренней скованности (мин), выраженность боли по визуально-аналоговой шкале (ВАШ)) и на основании общей оценки эффективности лечения, по мнению врача и больного. Кроме того, у всех больных оценивалась динамика АД на фоне лечения НПВП.
Результаты
В I группе на фоне лечения найзом в суточной дозе 200 мг за 3 нед. лечения достигнута достоверная динамика показателей суставного синдрома. При этом эффективность терапии оценена 17 пациентами (85%) как хорошая и 3 (15%) — как удовлетворительная. По мнению врача, в 16 случаях (80%) наблюдалась хорошая эффективность препарата, в 4 случаях (20%) — удовлетворительная (рис. 1). Переносимость найза у 85% была хорошей, только у 2 больных (10%) отмечались изжога и гастралгии, у 1 больного (5%) — чувство тяжести в эпигастральной области. Однако при фиброгастроскопии у этих пациентов не выявлено эрозивного повреждения слизистой оболочки желудка. В группе больных, принимавших найз, не потребовалось отмены препарата ни у одного больного.
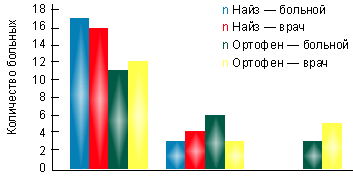 |
| Рисунок. Оценка эффективности препаратов на основании мнения больного и врача |
Во II группе на фоне терапии ортофеном в суточной дозе 150 мг через 3 нед. также отмечена существенная динамика показателей суставного синдрома. Однако оценка эффективности терапии показала, что только 11 пациентов (55%) оценили эффективность препарата как хорошую, 6 (30%) — как удовлетворительную и трое больных (15%) признали ее неудовлетворительной. По мнению лечащего врача, достаточная эффективность ортофена, соответствующая градации «хорошая», отмечалась в 12 случаях (60%), удовлетворительная — в 3 (15%) и неудовлетворительная — в 5 (25%) случаях (рис.).
Переносимость препарата ортофен была хуже, чем у найза: у 9 пациентов (45%) отмечались симптоматические побочные эффекты, причем у 3 больных (15%) потребовалась отмена препарата через 2 нед. от начала лечения в связи с выявленным при ФГДС эрозивным поражением слизистой оболочки антрального отдела желудка. В целом из побочных эффектов чаще отмечались изжога — у 7 (35%) пациентов, гастралгии — у 8 (40%), тошнота — у 4 (20%) и диарея — у 2 (10%) больных.
Особый интерес представляет влияние исследуемых НПВП на уровень АД, так как из 40 больных у 15 имелась сопутствующая ГБ, по поводу которой проводилась гипотензивная терапия. Динамика уровня АД в обеих группах на фоне лечения найзом и ортофеном представлена в таблице 2. Следует отметить, что терапия найзом не требовала усиления проводимой гипотензивной терапии (β-блокаторами, ингибиторами АПФ, диуретиками) и не вызывала повышения АД у ранее нормотензивных пациентов. В то же время лечение ортофеном потребовало коррекции доз гипотензивных препаратов у 4 (66,7%) из 6 больных ГБ и вызвало повышение АД у 5 (25%) женщин в постменопаузе с исходно высоконормальным АД. Данный эффект неселективного НПВП — ортофена — следует считать предсказуемым, особенно с учетом характера проводимой гипотензивной терапии. Все больные ГБ получали в разных комбинациях β-адреноблокаторы, ингибиторы АПФ и диуретики; при этом ни одному пациенту не был назначен дигидропиридиновый антагонист Са — амлодипин, который является препаратом выбора для лечения АГ в условиях терапии НПВП.
Таким образом, результаты открытого клинического исследования показали, что препарат найз у больных РА проявляет выраженную противовоспалительную активность, превосходящую диклофенак. При этом найз характеризуется хорошей переносимостью, малым числом симптоматических побочных эффектов и превосходит с этой точки зрения наиболее широко применяемый в клинической практике ортофен. Дополнительным преимуществом препарата найз можно считать менее выраженное влияние на уровень АД. При назначении найза не требовалось увеличения дозы гипотензивных препаратов. С учетом высокой распространенности эссенциальной гипертензии в популяции, взаимодействие НПВП с наиболее часто используемыми гипотензивными средствами представляется актуальной проблемой. Ревматические заболевания, требующие постоянной терапии НПВП, часто сочетаются с АГ. При этом у большинства больных ГБ коррекция АД может достигаться только благодаря комбинированной антигипертензивной терапии, а монотерапия дигидропиридиновыми антагонистами Са признается недостаточно эффективной. Следовательно, в большинстве случаев при лечении воспалительных ревматических заболеваний у лиц, страдающих ГБ, невозможно полностью нивелировать отрицательное взаимодействие «стандартных» НПВП с основными кардиологическими препаратами — β-адреноблокаторами, ингибиторами АПФ и диуретиками. В такой ситуации представляется рациональным выбор для проведения противовоспалительной терапии специфических ингибиторов ЦОГ-2, представителем которых является найз.
Литература
И. М. Марусенко, кандидат медицинских наук
Н. Н. Везикова, кандидат медицинских наук, доцент
В. К. Игнатьев, доктор медицинских наук, профессор
Петрозаводский университет, кафедра госпитальной терапии