Расширение мвп при беременности что это
Плацентарная недостаточность
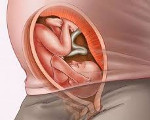
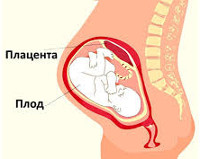
Большинство женщин знают, что плацента связывает маму и малыша во время беременности и при помощи нее к малышу поступают питательные вещества и кислород.
Бывают ли такие ситуации, когда плацента перестает правильно и полноценно выполнять свою функцию? Можно ли как то предотвратить это?
Какую функцию выполняет плацента
Внутри ворсин течет кровь малыша, а снаружи они омываются кровью матери. Между кровотоком мамы и малыша расположен всего один слой клеток, который и играет роль барьера между организмом матери и ребенка. Благодаря этой мембране кровь матери и плода не смешивается.
Однако в последние годы стало известно, что клетки крови плода все-таки проникают через плацентарный барьер в кровоток матери и благодаря этому стало возможным проведение генетических анализов и определение хромосомных аномалий, резуса фактора и пола плода по крови беременной женщины (неинвазивный пренатальный тест).
В плаценте происходит постоянный обмен веществ между мамой и ребенком. Из материнской крови к плоду поступает кислород и питательные вещества, от плода обратно к матери углекислый газ и продукты обмена, подлежащие выведению из организма.
Важной функцией плаценты является выработка гормонов и биологически активных веществ. В первую очередь это гормоны, важные для успешного вынашивания беременности, например хорионический гонадотропин, плацентарный лактоген, эстрогены и др.
К сожалению, не всегда все складывается вполне благополучно. В силу самых различных причин на разных сроках беременности могут происходить отклонения в развитии и функционировании плаценты. Изменения эти никогда не проходят бесследно для мамы и малыша, а зачастую имеют грозные последствия.
Если плацента перестает выполнять свои функции в полной мере, развивается так называемая плацентарная недостаточность. По сути, она заключается в ухудшении кровообращения в системе мать-плацента-плод.
Виды и причины плацентарной недостаточности
Врачи различают острую и хроническую плацентарную недостаточность:
Острая плацентарная недостаточность
Это состояние, требующее экстренного вмешательства врачей. Она характеризуется стремительным ухудшением плацентарного кровотока. Острая плацентарная недостаточность возникает в основном в результате отслойки плаценты или гибели отдельных участков ткани плаценты например при образовании тромбов в сосудах. Причиной отслойки может послужить травма живота, антифосфолипидный синдром.
Фосфолипиды – это сложные жиры, которые входят в состав оболочек всех клеток организма. В ряде случаев иммунная система организма вырабатывает большое количество антител к некоторым собственным фосфолипидам и белкам, связывающим эти липиды. Они называются антифосфолипидные антитела и при взаимодействии с клетками организма вызывают повреждение клеток и активацию свертывающей системы крови, что приводит к тромбообразованию.
Антифосфолипидный синдром является самой частой причиной тромботических осложнений при беременности, в том числе причиной отслойки плаценты и острой плацентаной недостаточности.
Вызвать отслойку плаценты может также тяжелое течение гестоза – грозного осложнения второй половины беременности, проявляющееся отеками, повышением давления и появлением белка в моче.
Острая плацентарная недостаточность развивается при отслойке более 2/3 поверхности плаценты.
В случае развития острой плацентарной недостаточности необходимо максимально быстро провести операцию кесарева сечения для сохранения жизни малыша и мамы.
Хроническая плацентарная недостаточность
Значительно чаще у беременных женщин встречается хроническая плацентарная недостаточность. В этом случае происходит нарушение формирования и созревания плаценты, уменьшается маточно-плацентарный и плодово-плацентарный кровотоки, ограничивается газообмен и обмен веществ в плаценте, снижается синтез плацентарных гормонов. Все эти изменения определяют недостаточное поступление кислорода и питательных веществ малышу, вызывают задержку роста и развития плода.
Причинами плацентарной недостаточности чаще всего являются перенесенные аборты, особенно хирургический аборт при первой беременности, курение, при этом количество и крепость выкуриваемых сигарет значения не имеют, поскольку на формировании неполноценных сосудов плаценты негативное действие оказывает табачный дым, а не никотин.
В группу риска по развитию плацентарной недостаточности входят также женщины с хроническими заболеваниями, такими как артериальная гипертензия, железодефицитная анемия, пиелонефрит, сахарный диабет, заболевания щитовидной железы.
В последние годы наблюдается значительный рост плацентарной недостаточности, вызванной бактериями, вирусами, грибами. Причиной этого может быть как острая инфекция, перенесенная будущей мамой во время беременности, так и активация хронического инфекционного процесса в организме беременной женщины.
Немаловажное значение в формировании хронической плацентарной недостаточности играет патология матки: эндометриоз, пороки развития матки (седловидная, двурогая). Фактором риска врачи считают также миому матки. Безусловно, целый ряд лекарственных средств оказывает неблагоприятное влияние на формирование плаценты и развитие плода. В настоящее время определен список препаратов, не разрешенных к применению во время беременности.
В некоторых случаях плацентарная недостаточность может быть обусловлена наличием хромосомных нарушений у плода, в частности при синдромах Дауна (наличие дополнительной 21 хромосомы у плода) или синдроме Эдвардса (дополнительная 18 хромосома у плода) уже в ранние сроки беременности диагностируется нарушение функции плаценты.
Следует отметить, что среди осложнений беременности, наиболее часто приводящих к развитию хронической плацентарной недостаточности, существенным фактором является преэклампсия (или поздний гестоз) – это осложнения второй половины беременности, проявляющееся отеками, повышением давления и появлением белка в моче.
Независимо от факторов, способствующих развитию плацентарной недостаточности, в основе ее лежат нарушения кровообращения в маточно-плацентарном комплексе, приводящие к нарушению всех функций плаценты. Следовательно, симптомы хронической плацентарной недостаточности будут обусловлены недостатком поступления кислорода и питательных веществ к плоду.
Это прежде всего, задержка внутриутробного развития плода – отставание размеров плода и замедление темпов его роста. Часто имеют место изменение двигательной активности плода. Сначала может быть некоторое усиление движений, а затем уменьшение. Нарушение защитной функции плаценты приводит к внутриутробному инфицированию плода под действием проникающих через плаценту патогенных (болезнетворных) микроорганизмов. Плод, развитие которого происходит в условиях плацентарной недостаточности, в значительно большей степени подвержен риску травматизации в родах, у них отмечается нарушение адаптации к внеутробной жизни, повышенная заболеваемость в первый год жизни.
По времени возникновения врачи разделяют плацентарную недостаточность на раннюю и позднюю.
Ранняя (или первичная) плацентарная недостаточность
Развивается до 16 недель беременности. Она возникает уже на этапе формирования плаценты и связана с заболеваниями беременной женщины, имеющимися до беременности, к примеру с патологией матки, хронической артериальной гипертензией, эндокринологическими заболеваниями. При этом происходит формированием неполноценных сосудов в плаценте.
Поздняя (или вторичная) плацентарная недостаточность
Возникает после 16 недель беременности и чаще всего связана с заболеваниями, возникшими уже во время беременности. Чаще всего это железодефицитная анемия (то есть снижение концентрации гемоглобина и железа в крови), гестационный сахарный диабет (то есть нарушение усвоения организмом глюкозы, возникшее на фоне беременности), перенесенные вирусные и бактериальные инфекции.
Важным является подразделение плацентарной недостаточности на компенсированную и декомпенсированные формы.
Компенсированная плацентарная недостаточность
Развивается, к примеру, при угрозе прерывания беременности и нетяжелых формах позднего гестоза, в случае, если эти осложнения успешно поддаются медикаментозной коррекции.
Декомпенсированная плацентарная недостаточность
Вызывает развитие задержки развития плода, хронической внутриутробной гипоксии, вплоть до гибели плода.
Диагностика плацентарной недостаточности
Лечить уже развившуюся плацентарную недостаточность практически невозможно, поэтому врачи активно стремятся выявлять беременных женщин, угрожаемых в отношении формирования нарушений функции плаценты. Если плацентарная недостаточность выявляется в 3 триместре беременности, эффективного лечения, к сожалению, не существует. Поэтому очень активно в настоящее время применяются все способы выявления в ранние сроки беременности тех женщин, в формировании плаценты которых произошли нарушения.
В первую очередь, при постановке на учет по беременности выявляют максимально значимые факторы риска – курение, перенесенные аборты, отягощенную наследственность (низкий вес при рождении, склонность к тромбозам), наличие хронических заболеваний сердца, сосудов, сахарного диабета.
Профилактические мероприятия против развития плацентарной недостаточности особенно актуальны и необходимы до 16-17 недель беременности, когда происходит формирование структур плаценты.
Значимую помощь в оценке риска развития плацентарной недостаточности оказывает пренатальный скрининг, который проводится в 11-14 недель беременности. Он проводится для выявления синдромов Дауна, Эдвардса и др. хромосомных болезней у плода. В настоящее время самым актуальным является проведение комплексного ранний скрининг беременной на прогнозирование риска развития плацентарной недостаточности, преэклампсии и внутриутробной задержки развития плода. Поскольку данный вид диагностики относится к самым современным и передовым, к сожалению, он пока не включен в перечень услуг, предоставляемых в женской консультации в рамках ОМС, но доступен всем желающим в центрах пренатальной диагностики.
Определение белков, вырабатываемых плацентой
В первую очередь проводят определение белка РАРР-А, он является также маркером хромосомных аномалий плода. Снижение концентрации РАРР-А в крови в 11-14 недель беременности встречается у беременных женщин, имеющих высокий риск плацентарной недостаточности и задержки развития плода.
Второй гормон плаценты, который помогает в оценке рисков плацентарной недостаточности – PIGF (плацентарный фактор роста). Его концентрация в крови снижается задолго до первых проявлений плацентарной недостаточности. Его определение применяют не настолько широко, как PAPP-A, но тем не менее многие лаборатории уже включили данный белок в пренатальный скрининг 1 триместра. Крайне важное значение при проведении скрининга 1 триместра имеет измерение кровотоков в сосудах матки. Однозначно доказано, что сужение сосудов матки, определяемое при исследовании, свидетельствует о неполноценности формирования плаценты, которое будет ухудшаться с увеличением срока беременности и приведет к снижению питания малыша и снабжения его кислородов, то есть к развитию плацентарной недостаточности и задержки развития плода. При нормальных размерах маточных сосудов в 11-14 недель беременности риск тяжелой плацентарной недостаточности ничтожно мал.
Следующее обязательное скрининговое ультразвуковое исследование проводится в 20-21 неделю беременности. При этом обязательно проводят измерения плода, чтобы оценить, нет ли отставания в росте. Ведь при кислородном голодании замедляются темпы роста плода и размеры его начинают отставать от нормы для каждого срока беременности. Кроме того врач обязательно оценивает состояние и зрелость плаценты. Во время УЗИ проводится также допплерометрия сосудов матки для выявления ранних изменений, предшествующих клиническим проявлениям плацентарной недостаточности.
У пациенток, относящихся к группе высокого риска кроме УЗИ и допплерометрии проводят также суточное мониторирование колебаний артериального давления, определение количества белка в анализе мочи, собранном за сутки, оценивают показатели системы свертывания крови.
Третье УЗИ проводится всем будущим мамам в 30–34 недели беременности. Врач измеряет окружность головы и живота крохи, длину костей его ручек и ножек, и вычисляет предполагаемый вес плода. Эти измерения позволяют доктору убедиться в том, что малыш развивается нормально. Также имеет значение строение плаценты, наличие в ней признаков старения, вследствие чего она обычно перестает полноценно снабжать малыша кровью, а, значит, ему перестает хватать кислорода и питательных веществ и развитие ребенка нарушается. Во время УЗИ оценивается количество и вид околоплодных вод, которые также могут изменяться при внутриутробном страдании плода.
Допплерометрия
Допплерометрия сосудов плаценты и пуповины (метод исследования скоростей кровотоков в этих сосудах) так же позволяет оценить самочувствие малыша. Доктор исследует кровоток в артериях матки, пуповины, сердца и мозга ребенка. Это исследование позволяет определить, хорошо ли работает плацента, нет ли признаков нехватки кислорода у малыша, или развития гестоза у мамы. При снижении скорости кровотока в каком-либо сосуде можно говорить о нарушениях питания плода различной степени тяжести.
Вовремя проведенное обследование позволяет выявить начальные стадии дефицита кровоснабжения. В таких случаях лечение сможет предотвратить грозные осложнения, такие как гипоксия и внутриутробная задержка развития малыша. Допперометрию проводят в 20–21 неделю и в 30-32 недели беременности, при наличии изменений, контроль осуществляют минимум каждые две недели.
Кардиотокография
Это важный метод оценки состояния плода. Проводится КТГ при сроке беременности 33 недели и более, поскольку только на этом этапе внутриутробного развития малыша устанавливается полноценная регуляция деятельности сердечно-сосудистой системы плода центрами спинного и головного мозга. Запись сердцебиений плода проводят в течение 20–40 минут, а при необходимости исследование может быть продлено до 1,5 часов.
Аппарат регистрирует и записывает частоту сердцебиений малыша. Врач акушер-гинеколог оценивает кривую записи сердцебиений, эпизоды урежения и резкого учащения частоты сердечных сокращений плода и на основании этих данных делает заключение о том, насколько комфортно малыш чувствует себя в животе у мамы. К примеру, при снижении концентрации кислорода в крови плода, уменьшается и его поступление к клеткам нервной системы, что в свою очередь отражается на частоте сердечных сокращений. При нормальном течении беременности КТГ проводят после 33 недели 1 раз в 10–14 дней, иногда чаще. В некоторых клиниках в настоящее время предлагается услуга постоянного КТГ-мониторирования, что приобретает актуальность при наличии признаков плацентарной недостаточности. Беременной женщине выдается мониторчик, который регистрирует изменения сердечной деятельности малыша и эти данные по интернету передаются лечащему врачу.
Лечение плацентарной недостаточности
Специфических способов лечения плацентарной недостаточности в настоящее время не существует, поскольку нет лекарственных препаратов, которые избирательно улучшают маточно-плацентарный кровоток. Именно поэтому все меры борьбы с плацентарной недостаточностью направлены на профилактику. Если пациентка относится к группе высокого риска по развитию плацентарной недостаточности, с раннего срока беременности ей назначают лекарственные препараты, эффективность которых хорошо доказана и которые предупреждают раннее развитие выраженных нарушений функции плаценты.
Если во время проведения дополнительных методов оценки состояния плода выявляются начальные нарушения поступления кислорода к малышу, проводится медикаментозное лечение, направленное на увеличение притока крови и кислорода через плаценту и обязательные контрольные обследования на фоне проводимой терапии. Если изменения серьезные и малыш испытывает выраженный дефицит кислорода и питательных веществ, состояние его страдает, то в таких случаях проводится экстренное родоразрешение.
Расширение межворсинчатых пространств плаценты как маркер осложнений беременности при тромбофилии
ГБУЗ МО «Московский областной НИИ акушерства и гинекологии» Министерства здравоохранения Московской области, Москва, Россия
Цель. Проследить течение и исходы беременности у пациенток с массивными структурными изменениями плаценты в виде расширения межворсинчатых пространств (МВП) в зависимости от коррекции гиперкоагуляции.
Материалы и методы. В исследование включены 139 беременных с впервые выявленными при УЗИ структурными изменениями плаценты в виде массивного расширения МВП и подтвержденной тромбофилией. В течение беременности проведен анализ толщины и структуры плаценты и исходов беременности в зависимости от лечения. 1-я группа (n=64) не получала или нерегулярно применяла антикоагулянтную или антиагрегантную терапию. 2-я группа (n=75) в течение всей беременности получала лечение под контролем лабораторных данных.
Результаты. Проведен сравнительный анализ течения беременности у пациенток с тромбофилией и характерными структурными изменениями в плаценте. Показано, что у пациенток, получавших постоянную антикоагулянтную терапию под лабораторным контролем с достижением параметров нормокоагуляции, наступают уменьшение толщины и нормализация эхоструктуры плаценты. Улучшение перинатальных исходов выражается в снижении количества неразвивающихся беременностей в 4 раза, отслоек плаценты – в 3,5 раза, задержек внутриутробного роста плода – в 1,5 раза, увеличении срочных родов – в 4 раза.
Заключение. Эхоструктура плаценты может служить дополнительным диагностическим маркером тромбофилии и гиперкоагуляции, а также дополнительным критерием эффективности проводимого лечения.
Определенную роль в формировании осложнений беременности, приводящих к увеличению количества преждевременных родов, перинатальных осложнений и перинатальных потерь, играют гиперкоагуляционные состояния, в том числе связанные с тромбофилией.
Наследственная тромбофилия – это нарушение свертывания крови, при котором доказано увеличение риска венозной тромбоэмболии (ВТЭ). Наследственные тромбофилии связаны и с неблагоприятными исходами во время беременности. Тем не менее существует ограниченное количество данных, позволяющих проводить скрининг и лечение этих состояний во время беременности. Различные виды тромбофилий обусловливают неоднозначный риск тромбоза у матери и неблагоприятные исходы беременности, поэтому также неоднозначны показания к скринингу для выявления этих состояний [1, 2].
Неблагоприятные исходы при беременности включают как ранние (привычное невынашивание), так и поздние опосредованные сосудистые проблемы плаценты (антенатальная гибель плода, преэклампсия, отслойка плаценты и задержка внутриутробного роста). Simcox L.E. et al. говорят: «Существует мало убедительных доказательств связи неблагоприятных исходов беременности с тромбофилией во время беременности» [3].
В течение последних десятилетий многократно обсуждается вопрос, необходимо ли обследование беременных на наследственные тромбофилии в виде повсеместного скрининга, что привело бы к значительным материальным затратам, или тестирование отдельных групп населения с высоким предполагаемым риском осложнений беременности на основании анамнестических данных.
Тестирование на тромбофилию однозначно рекомендовано у пациенток с венозным тромбозом или эпизодами тромбоза у близких родственников в анамнезе [4]. По мнению Dłuski D. et al., тесты на тромбофилию следует проводить у женщин с неблагоприятными исходами беременности в анамнезе, которые планируют беременность, чтобы начать антикоагулянтную профилактику [5].
Однако необходимость применения антикоагулянтной терапии у беременных с тромбофилией с целью улучшения исходов и профилактики осложнений беременности также относится к вопросам неоднозначным и нерешенным [6].
Метаанализ рандомизированных контролируемых исследований от 2016 г., сравнивающих применение низкомолекулярного гепарина (НМГ) у женщин с наследственной тромбофилией и предшествующим невынашиванием беременности, утверждает, что не было значительных различий в показателях числа живорождений в зависимости от наличия или отсутствия терапии НМГ (относительный риск (ОР) 0,81; 95% доверительный интервал (ДИ) 0,55–1,19; Р=0,28) [7].
В обзоре 2019 г. исследуются доказательства влияния наследственной тромбофилии на привычное невынашивание и другие осложнения беременности; обсуждается вопрос, может ли антитромботическое лечение изменить исход беременности. Основной вывод – обследование на наследственную тромбофилию не требуется при привычном невынашивании беременности или осложнениях на поздних сроках беременности [8].
Ранняя диагностика и своевременная коррекция гиперкоагуляционных изменений, вероятно, могли бы оказать определенное влияние на предупреждение развития грозных осложнений, в том числе приводящих к неблагоприятным перинатальным исходам. В настоящее время клинические рекомендации по тромбофилии предусматривают диагностические мероприятия в ряде конкретных ситуаций: пациентки с эпизодом ВТЭ в анамнезе, ассоциированной с наследственной или приобретенной тромбофилией высокого риска, относятся к группе очень высокого риска последующих ВТЭ [9, 10].
В других клинических ситуациях обследование показателей свертывающей системы крови не предусмотрено. Для проведения дорогостоящих исследований нужны отдельные показания, которые могут не проявляться при даже тщательном клиническом наблюдении беременной в рамках существующего протокола. В ранее проведенном ретроспективном исследовании нами была показана корреляция структурных изменений плаценты с частотой выявления наследственной тромбофилии и гиперкоагуляции, а также с частотой неблагоприятных перинатальных исходов в анамнезе. Было предложено считать массивные структурные изменения плаценты в виде расширения межворсинчатых пространств (МВП) маркером гиперкоагуляции при данной беременности [11]. Вторая часть исследования представляет собой проспективный анализ клинических наблюдений пациенток, у которых в течение настоящей беременности при ультразвуковом исследовании (УЗИ) выявлены массивные расширения МВП плаценты.
Цель исследования: проследить течение и исходы беременности у пациенток с массивными структурными изме.
Гиперплазия плаценты
Гиперплазия плаценты — увеличение толщины и объема плацентарной ткани, связанное с действием компенсаторных и патологических факторов. Специфические клинические симптомы отсутствуют. На поздних этапах при наличии плацентарной недостаточности патология проявляется изменением активности плода — усилением или замедлением его шевелений. Для постановки диагноза используют УЗИ матки, КТГ, допплерографию плацентарного кровотока, инвазивные пренатальные методы исследований, лабораторные анализы. Лечение направлено на улучшение кровотока в маточно-плацентарной системе, устранение причины расстройства и коррекцию сопутствующих нарушений.
Общие сведения
В современном акушерстве утолщение плаценты рассматривается не как отдельная нозологическая единица, а как важный диагностический признак, свидетельствующий о наличии другой патологии. В норме по мере развития беременности плацентарная ткань постепенно утолщается, достигая максимальных размеров к 34-36 неделе. После этого ее рост останавливается, а объем остается таким же или даже несколько уменьшается. При гиперплазии плаценты ее масса достигает 750 г и более вместо средних 400-600 г, а плодово-плацентарный коэффициент, отражающий соотношение веса ребенка и плацентарной ткани, к концу беременности составляет не более 2-3 вместо нормальных 6-7.
Причины гиперплазии плаценты
Утолщение плацентарной ткани обычно является следствием компенсаторных реакций и защитных механизмов, призванных обеспечить оптимальные условия развития и безопасность плода. В ряде случаев увеличение массы плаценты вызвано патологическими изменениями в ее тканях. По мнению специалистов в сфере акушерства и гинекологии, основными причинами гиперплазии органа являются:
Патогенез
Механизм гиперплазии плаценты напрямую зависит от причин, спровоцировавших утолщение детского места. При истинном разрастании плацентарной ткани в основе патогенеза лежит компенсаторный ангиоматоз, возникший в ответ на кислородное голодание плода. Для улучшения фетоплацентарного кровоснабжения количество сосудов в ворсине хориона увеличивается с 4-6 до 25-50 и более, из-за чего плацента становится толще. При ложной гиперплазии размер и толщина детского места изменяются вследствие патофизиологических процессов, характерных для основного заболевания. Обычно в этих случаях объем органа увеличивается за счет отека интерстиция, реже — фиброзных и деструктивных изменений. При некоторых состояниях включаются оба механизма — компенсаторный и патологический.
Симптомы гиперплазии плаценты
На ранних этапах заболевания какие-либо клинические проявления отсутствуют, утолщение органа часто становится случайной находкой при проведении планового УЗИ после 20-й недели беременности. По мере прогрессирования гиперплазии могут возникнуть признаки, характерные для плацентарной недостаточности, — плод становится более активным, что проявляется усилением и учащением его шевелений. Прогностически неблагоприятным симптомом, при появлении которого требуется срочная консультация акушера-гинеколога, является затихание движений ребенка. Значительное увеличение живота отмечается только при сочетании гиперплазии с многоводием.
Осложнения
Последствия для плода и матери, возникающие при наличии гиперплазии плаценты, связаны с возможным нарушением ее основных функций — питательной, гормональной и защитной. При наличии патологических процессов и деструкции плацентарной ткани развивается фетоплацентарная недостаточность, влекущая за собой задержку внутриутробного развития, гипотрофию, гипоксию и в крайних случаях гибель ребенка. У беременных с увеличенной плацентой повышается риск преждевременных родов и необходимости кесарева сечения. Нарушение секреции гормонов (эстрогенов, прогестерона, хорионического гонадотропина, плацентарного лактогенного гормона, релаксина) чревато слабостью родовой деятельности, повышенным родовым травматизмом, гипотоническими кровотечениями в послеродовом периоде, гипогалактией.
Диагностика
Задачами диагностического этапа являются оценка степени гиперплазии плаценты, выявление структурных изменений и признаков функциональной недостаточности, уточнение причин, приведших к увеличению органа. Комплексное обследование включает инструментальные и лабораторные методы, позволяющие получить точные данные о состоянии плацентарной ткани, плода и беременной женщины. Для целей диагностики наиболее ценными являются:
Для оценки функционального состояния организма женщины и выявления экстрагенитальной патологии назначают общие анализы крови и мочи, биохимическое исследование крови, определяют уровень глюкозы. В качестве вспомогательных методов обследования плода рекомендованы его фетометрия и эхокардиография. Дифференциальная диагностика проводится между заболеваниями и патологическими состояниями, провоцирующими утолщение плаценты. При необходимости пациентку консультируют эндокринолог, дерматовенеролог, инфекционист, уролог, врач-генетик.
Лечение гиперплазии плаценты
Основными целями терапии являются устранение заболевания, вызвавшего гиперпластические нарушения в плаценте, и нормализация маточно-плацентарного кровоснабжения. Кроме применения медикаментов женщине рекомендуют изменить образ жизни: увеличить время отдыха и ночного сна, полноценно питаться, избегать переохлаждений, значительных физических и эмоциональных нагрузок, дозированно выполнять специальные упражнения для беременных. При утолщенной плаценте пациентке назначают:
Дополнительно в схему лечения гиперплазии включают витаминно-минеральные комплексы, иммунокорректоры и эссенциальные фосфолипиды. Прерывание беременности выполняется только в тяжелых случаях конфликта по резус- или AB0-факторам либо при обнаружении другой патологии, представляющей непосредственную угрозу здоровью и жизни беременной или плода.
Прогноз и профилактика
Прогноз зависит от причины, вызвавшей гиперплазию плаценты, и в большинстве случаев при адекватном комплексном лечении является благоприятным. Профилактика направлена на раннюю диагностику генитальной и экстрагенитальной патологии, возможных пороков развития ребенка. Рекомендованы планирование беременности, своевременная постановка на учет в женской консультации, регулярное прохождение УЗИ-скрининга, санация очагов хронической инфекции, ограничение пребывания в местах скопления людей при эпидемиологически неблагоприятной ситуации, прием препаратов железа для предупреждения анемии.