Раствор мела в воде можно разделить чем
Способы разделения смесей
Как мы уже знаете, каждое вещество в составе смеси сохраняет свои свойства. Это позволяет разделять смеси на отдельные вещества. Чтобы ознакомиться со способами разделения смесей, выполним опыты.
Разделение смеси методом отстаивания
Приготовим смесь мела и воды. Для этого на дно прозрачной сосуды поместим 1 столовую ложку порошка мела, по стеклянной палочке добавим полстакана воды и перемешаем. Образуется смесь белого цвета, которая, постояв несколько минут, разделится на два слоя. Слой мела осядет на дно, а слой воды будет находиться над ним. Такое происходит потому что мел в воде не растворяется и он тяжелее воды. Осторожно слив воду, мы разделим эту смесь. Такой способ разделения смесей получил название отстаивания.
Разделение смеси мела и воды фильтрованием
Однако полностью разделить смесь мела и воды с помощью отстаивания не удается. Как достичь полного разделения смеси этих веществ? Выполним еще один опыт.
Смесь мела и воды пропустим через фильтр — плотный материал из специальной бумаги или ткани. Мы увидим, что вода проникает через фильтр в посуду-приемник, а мел остается на фильтре. Этот способ разделения смесей получил название фильтрования.
Фильтры изготавливаются из специальной бумаги, который так и называется — фильтровальная, или из тканей различной плотности. Фильтром может быть слой чистого песка или ваты. Кстати, в городских водоочистных станциях применяют песчаные фильтры. Толщина слоя песка в них достигает 1 м.
Как видим, отстаиванием и фильтрованием можно разделить смесь воды и нерастворимого в ней вещества.
Разделение смеси поваренной соли и воды выпариванием
Как вы знаете, поваренная соль хорошо растворяется в воде. Такую смесь веществ отстаиванием разделить нельзя. А удастся это сделать фильтрацией? Выполним опыт. Пропустим смесь воды и поваренной соли через бумажный фильтр. Мы увидим, что соли на фильтре не осталось.
Итак, если вещество хорошо растворяется в воде, то отстаивание и фильтрование не подходят для разделения такой смеси. Для этого существует другой способ — выпаривания.
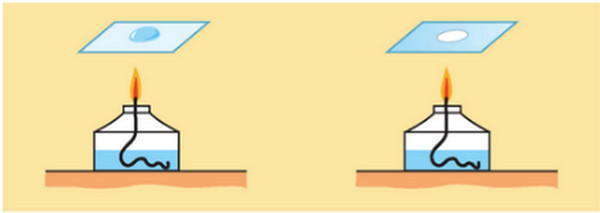
Капните небольшое количество смеси воды и поваренной соли на стекло и начнем нагревать его до тех пор, пока вся вода не испарится. После того как вода испарится, на стекле останется пятно белого цвета. Это и есть поваренная соль. С помощью выпаривания мы разделили смесь воды и поваренной соли.
Разделение смеси газов
Вы уже знаете способы выделения составных частей из смеси твердых и жидких веществ. А как разделить смесь газообразных веществ? Рассмотрим это на примере воздуха.
Заключение
Разделение смеси — это выделение из нее чистых веществ.
Чтобы разделить смесь, необходимо знать свойства веществ, которые входят в ее состав.
Теперь вы знаете, что существуют различные способы разделения смесей: отстаивание, фильтрование, выпаривание.
Инструменты пользователя
Инструменты сайта
Боковая панель
Справочная информация
Ингредиенты
Технология
Кулинария, блюда к пиву и из пива
Остальное
Содержание
Водоподготовка с применением растворенного мела
Для приготовления воды с временной жесткостью (щелочность и кальциевая жесткость) нужен мел ( CaCO3 ). Однако, мел не слишком хорошо растворяется в воде и большая часть добавляемого мела ложится на дно в виде осадка или плавает в нерстворенном виде. Эта статья расскажет, как можно растворить нужное количество мела.
О меле и карбонатной системе
Если вам лень разбираться с химическими принципами растворения мела, можете спокойно пропустить теоретическую часть.
Мел или по-научному карбонат кальция ( CaCO3 ) представляет собой соль угольной кислоты и состоит из ионов кальция ( Ca2+ ) и карбоната ( CO3|2- ). Если мы что-то и знаем о меле, так то, что он очень плохо растворяется в воде. Это потому, что продукт растворимости между кальцием и карбонатом очень невелик. Химики описывают это так:
Но как же тогда растворить мел в воде? Это можно сделать, удалив карбонат, который добавляется в воду с мелом. Чтобы разобраться с этим, давайте взглянем на угольную кислоту и карбонатную систему. Угольная кислота образуется при двуокиси углерода в воде. Не вся двуокись углерода ( CO2 ) образует угольную кислоту, но только часть, согласно этому химическому уравнению:
Этот процесс обратим. То есть, если ион бикарбонат принимает протон, он превращается в угольную кислоту.
Когда ион бикарбонат теряет еще один протон, он становится карбонатом.
Но как все это связано с растворением мела? Что ж, выше мы увидели, что необходимо удалить карбонаты, которые переходят в воду при растворении мела, чтобы позволить мелу растворяться дальше. Это делается превращением карбонатов в бикарбонаты. Этот процесс поглащает протоны. Те самые протоны, которые так нам нужны, чтобы помочь растворить мела больше, чем вода способна без посторонней помощи.
Чтобы получить эти протоны, нам нужно добавить кислоты. В конце-концов, именно это кислота и делает: добавляет протоны и в результате снижает pH раствора. Что касается кислоты, обычно мы можем выбирать только одно из двух: угольную кислоту или любую другую кислоту. Давайте посмотрим, что будет, если добавим какую-нибудь отличную от угольной кислоту. Например соляную кислоту, которую можно разделить в воде на протон ( H+ ) и ион хлора ( Cl- ):
2H+ + 2Cl- + CaCO3 → H2O + CO2 + 2Cl- + Ca2+
В результате реакции между соляной кислотой и мелом мы получим воду, CO2 (который улетучится), хлор ( Cl- ) и кальций ( Ca2+ ). Посмотрев на результат наших манипуляций, мы увидим, что гораздо проще было сделать аналогичную водоподготовку просто добавив хлористый кальций в виде соли. Одна из причин того, почему мы хотим растворить мел в воде — это желание желание получить более щелочную воду, которая получается благодаря повышению концентрации ионов карбоната и бикарбоната. Если содержание карбонатов и бикарбонатов в воде не меняется, щелочность воды так же остается неизменной.
Все кислоты, кроме угольной, не годятся. Так, а что же угольная кислота? Когда угольная кислота становится бикарбонатами, она теряет протоны, которые могут превратить ионы карбонаты, добавленные с мелом, в бикарбонаты. Вот, как это выглядит:
HCO3- + H+ + CaCO3 → Ca2+ + 2HCO3-
Молекула мела распадается на ион кальция и ион бикарбоната. Другой ион бикарбоната поступает из угольной кислоты, которая теряет протон. Благодаря тому, что этот протон был потрачен на растворение мела, мы можем сказать, что эта самая молекула мела отвечает и за создание этого иона бикарбоната. В итоге получается, что одна молекула мела, при растворении в угольной кислоте дает один ион кальция и два иона бикарбоната.
Зачем растворять мел
Теперь, когда мы знаем, как растворять мел, пришла пора спросить себя, зачем все эти сложности. Тем более, что затор и так дает кислую среду, которая должна растворить любой мел, недорастворившийся в воде. При pH затора (
5.5) меньше, чем 0.00005 % карбонатной системы — карбонаты.
Однако, эксперименты с pH затора, проводившиеся с растворенным и взвешенным мелом показали, что способность взвешенного, т.е. не растворенного, мела повышать pH затора ограничена. Как видно на рисунке 4, не растворенный мел не способен повышать pH затора больше, чем на 0,2 единицы. Причем зависимости от кислотности солода не наблюдается: для солода Пилснер и для мюнхенского солода кривые аналогичны. Растворенный же мел, с другой стороны, демонстрирует замечательно линейное влияние концентрации мела на pH.
Я провел эксперимент с двумя аналогичными заторниками, когда варил Schwarzbier. В одном из заторников использовалась вода с растворенным мелом, в другом со взвешенным. Основываясь на исследованиях pH затора, я знал, что, при использовании растворенного мела, должен брать его вдвое меньше для получения тех же значений pH. Что и было подтверждено экспериментом.
Если вы хотите варить пиво следуя Reinheitsgebot — немецкому закону о чистоте пива, вам придется растворять мел. Согласно этому закону, добавление солей или воды, которая не соответствует питьевым стандартам, недопустимо.
Водоподготовку с растворением мела смело можно считать продвинутой техникой для умелого пивовара. Я сварил немало прекрасного пива, добавляя прямо в затор или в воду, не растворенный мел, и только недавно стал растворять его заранее. Как и в случае с другими техниками, пивовар сам должен решать, стоит ли эта техника дополнительно потраченных на нее усилий.
Как растворить мел при помощи газированной воды
Чтобы сварить Kaiser Alt, мне нужно скопировать водный профиль Дюссельдорфа, города где варится большинство немецких Альтов. Одина из наиболее известных своими альтами пивоварен Zum Uereige, однако, не пользуется городской водой. Согласно этому интернет отчету, воду для варки пива они берут из собственного артезианского колодца. С другой стороны, водопроводная вода Дюссельдорфа – тщательно очищенная и обработанная вода из реки Рейн.
Процесс шаг за шагом
Рассчет добавочных солей
Шаг 1
Во вкладке «advanced» введите начальный водяной профиль. Я пользуюсь фильтром обратного осмоса, что дает очень мягкую воду, анализ которой для меня проводили в лаборатории. Если вы так же пользуетесь фильтром обратного осмоса, но анализов своей воды не делали, просто оставьте везде 0. Концентрация ионов в воде настолько мала по сравнению с той, которая будет после водоподготовки, что отклонения будут слишком малы, чтобы иметь значения.
Шаг 2
Поглядывая на таблицу «resulting water profile» 4) (находится ниже или правее) введите концентрацию пивоваренных солей. Указывать конечный вес добавляемых солей с учетом количества воды, предполагаемой для варки, было бы не удобно, вместо этого вводите значения в ppm 5) (или мг/л, что то же самое). Это позволяет рассчитывать «рецепт воды» не зависимо объема необходимой воды. Как только определитесь с нужным вам объемом воды, введите его в таблице «Water use» и калькулятор сам рассчитает веса добавляемых солей относительно объема и покажет их чуть ниже.
Шаг 3
Шаг 4
Шаг 5
Необходимое количество солей рассчитывается исходя из объема воды, определенного раньше. Так как я не имею возможности подготовить сразу всю необходимую мне воду сразу, я вынужден готовить заторную и промывную воду раздельно. Но для тех, кто может себе позволить сделать всю воду разом, калькулятор подсчитывает соли так же и для всего объема.
По-возможности, я предпочитаю растворять мел в 2 л. бутылках их под газированной воды, что и проделал в данном случае. Я использовал 1,9 л. для растворения мела под заторную воду и 1,6 л. для промывной воды и мне потребовалось давление всего в 1,55 бар (23psi) и 1.38 bar (20 psi) соответственно. Это абсолютные значения, что означает, что атмосферное давление так же входит в эти цифры, иными словами, когда я подаю углекислый газ в бутылки, мой манометр должен показывать >0.55 бар (> 8 psi) и >0.38 бар (> 6 psi), так как он измеряет давление, которое превышает атмосферное.
Приготовление пивоваренной воды
Тестовые задания к параграфу 4
1. Выберите схемы, изображающие состав чистых веществ:
На рисунке под номером 2 мы видим разнородные молекулы, поэтому ответ: 1 и 3.
2. Фильтрованием можно разделить смесь:
1. воды и сахара;
2. воды и поваренной соли
3. воды и угольной пыли
4. воды и столового уксуса.
Что такое фильтрование? Отделение твердых, нерастворимых частиц от раствора. Какое вещество, из списка выше, нерастворимо в воде? Уголь.
Ответ: 3. воды и угольной выли.
3. Смесь порошков железа и серы является:
1) гомогенной;
2) гетерогенной.
Смесь чего? Смесь порошков. Казалось бы она должна быть гомогенной, ведь вещества находятся в одинаковом агрегатном состоянии. НО! По определению, гомогенной, называется смесь, в которой частицы вещества невозможно отличить даже под микроскопом. В данном случае, разницу между железом (темно-серое) и серой (светло-желтая) видно даже невооруженным глазом.
Ответ: 2) гетерогенной.
4. Очистить воду от подсолнечного масла можно:
1) выпариванием;
2) фильтрованием;
3) перегонкой;
4) отстаиванием.
5. Установите соответствие между смесью и способом ее разделения:
| 1) раствор поваренной соли в воде | А. действие магнитом |
| 2) раствор мела в воде | Б. с помощью делительной воронки |
| 3) смесь железа и серы | В. выпаривание |
| 4) смесь воды и бензина | Г. фильтрование |
Мел в воде нерастворим. Остальные указанные смеси, и способы их разделения, были описаны в параграфе, так что в подробности вдаваться не буду.
Ответы: 1) В; 2) Г; 3) А; 4) Б.
С пособы разделения смесей (и гетерогенных, и гомогенных) основаны на том факте, что вещества, входящие в состав смеси, сохраняют свои индивидуальные свойства. Гетерогенные смеси могут различаться по составу и фазовому состоянию, например: газ+жидкость; твердое вещество+жидкость; две несмешивающиеся жидкости и др. Основные способы разделения смесей представлены на схеме ниже. Рассмотрим каждый способ отдельно.
Разделение гетерогенных смесей
ФИЛЬТРОВАНИЕ
метод основанный на различной растворимости веществ и разных размерах частиц компонентов смеси. Фильтрование позволяет отделить твердое вещество от жидкости или газа.
Размер пор в фильтровальной бумаге таков, что позволяет молекулам воды и молекулам растворенного вещества беспрепятственно просачиваться. Частицы размером больше 0,01мм задерживаются на фильтре и не проходят сквозь него, таким образом формируется слой осадка.
Запомни! С помощью фильтрования нельзя разделить истинные растворы веществ, то есть растворы, в которых растворение произошло на уровне молекул или ионов.
Кроме фильтровальной бумаги в химических лабораториях используют специальные фильтры с
разным размером пор.
Фильтрование газовых смесей принципиально не отличается от фильтрования жидкостей. Разница заключается только в том, что при фильтровании газов от твердых взвешенных частиц (ТВЧ) используются фильтры специальных конструкций (бумажный, угольный) и насосы для принудительного прокачивания газовой смеси через фильтр, например фильтрация воздуха в салоне автомобиля или вытяжка над плитой.
Фильтрованием можно разделить:
ОТСТАИВАНИЕ
Данным методом можно разделять и несмешивающиеся жидкости. Для этого используют делительную воронку.
Отстаиванием можно разделить смеси:
МАГНИТНАЯ СЕПАРАЦИЯ
Метод основан на разных магнитных свойствах твердых компонентов смеси. Данный метод используют при наличии в смеси веществ-ферромагнетиков, то есть веществ, обладающих магнитными свойствами, например железа.
Все вещества, по отношению к магнитному полю, условно можно разделить на три большие группы:
Магнитной сепарацией можно разделить:
Разделение гомогенных смесей
Для разделения жидких гомогенных смесей (истинных растворов) используют следующие методы:
ВЫПАРИВАНИЕ. КРИСТАЛЛИЗАЦИЯ.
Метод основан на различных температурах кипения растворителя и растворенного вещества. Используется для выделения растворимых твердых веществ из растворов. Выпаривание обычно проводят следующим образом: раствор наливают в фарфоровую чашку и нагревают ее, постоянно перемешивая раствор. Вода постепенно испаряется и на дне чашки остается твердое вещество.
При этом испаренное вещество (воду или растворитель) можно собрать методом конденсирования на более холодной поверхности. Например, если поместить холодное предметное стекло над выпаривательной чашкой, то на его поверхности образуются капли воды. На этом же принципе основан метод дистилляции.
ДИСТИЛЛЯЦИЯ. ПЕРЕГОНКА.
В природе вода в чистом виде (без солей) не встречается. Океаническая, морская, речная, колодезная и родниковая вода – это разновидности растворов солей в воде. Однако часто людям необходима чистая вода, не содержащая солей (используется в двигателях автомобилей; в химическом производстве для получения различных растворов и веществ; при изготовлении фотографий). Такую воду называют дистиллированной, именно ее применяют в лаборатории для проведения химических опытов.
Перегонкой можно разделить:
ХРОМАТОГРАФИЯ
Можно самостоятельно получить хроматограмму и увидеть сущность метода на практике. Нужно смешать несколько чернил и каплю полученной смеси нанести на фильтровальную бумагу. Затем точно в середину цветного пятнышка начнем по каплям приливать чистую воду. Каждую каплю нужно вносить только после того, как впитается предыдущая. Вода играет роль элюэнта, переносящего исследуемое вещество по сорбенту — пористой бумаге. Вещества, входящие в состав смеси, задерживаются бумагой по-разному: одни хорошо удерживаются ею, а другие впитываются медленнее и продолжают некоторое время растекаться вместе с водой. Вскоре по листу бумаги начнет расползаться настоящая красочная хроматограмма: пятно одного цвета в центре, окруженное разноцветными концентрическими кольцами.
Особенно большое распространение получила тонкослойная хроматография, в органическом анализе. Достоинства тонкослойной хроматографии в том, что можно использовать простейший и очень чувствительный метод детектирования – визуальный контроль. Проявлять невидимые глазу пятна можно различными реактивами, а также используя ультрафиолетовый свет или авторадиографию.
В анализе органических и неорганических веществ применяют хроматографию на бумаге. Разработаны многочисленные методы разделения сложных смесей ионов, например смесей редкоземельных элементов, продуктов деления урана, элементов группы платины
СПОСОБЫ РАЗДЕЛЕНИЯ СМЕСЕЙ, ИСПОЛЬЗУЕМЫЕ В ПРОМЫШЛЕННОСТИ.
Способы разделения смесей, используемые в промышленности немногим отличаются от лабораторных способов, описанных выше.
Для разделения нефти чаще всего используют ректификацию (перегонку). Более подробно этот процесс описан в теме «Переработка нефти».
Самыми распространенными методами очистки и разделения веществ в промышленности являются отстаивание, фильтрация, сорбция и экстракция. Методы фильтрации и отстаивания проводятся аналогично лабораторным метода, с той разницей, что используются отстойники и фильтры больших объемов. Чаще всего, эти методы используются для очистки сточных вод. Поэтому рассмотрим подробнее методы экстракции и сорбции.
Термин «экстракция» приложим к различным фазовым равновесиям (жидкость – жидкость, газ – жидкость, жидкость – твердое тело и т.д.), но чаще его применяют к системам жидкость – жидкость, поэтому чаще всего можно встретить такое определение:
Одним из несмешивающихся растворителей обычно является вода, вторым – органический растворитель, однако это не обязательно. Экстракционный метод отличается универсальностью, он пригоден для выделения почти всех элементов в различных концентрациях. Экстракция позволяет разделять сложные многокомпонентные смеси зачастую эффективнее и быстрее, чем другие методы. Выполнение экстракционного отделения или разделения не требует сложного и дорогостоящего оборудования. Процесс может быть автоматизирован, при необходимости им можно управлять на расстоянии.
Чаще всего в промышленности методы абсорбции используют для очистки газовоздушных выбросов от частиц пыли или дыма, а также токсичных газообразных веществ. В случае поглощения газообразных веществ, между сорбентом и растворенным веществом может протекать химическая реакция. Например, при поглощении газообразного аммиака NH3 раствором азотной кислоты HNO3 образуется нитрат аммония NH4NO3 (аммиачная селитра), который можно использовать в качестве высокоэффективного азотного удобрения.
Процесс, при котором происходит абсорбция растворенного вещества за счет протекания химической реакции называется хемосорбцией.
Адсорбцию также используют для очистки воды от химических растворимых примесей. Например, фильтры для питьевой воды работают на принципе адсорбции слоем активированного угля с ионами серебра. Помимо поглощения всем объемом жидкого сорбента (абсорбции), и поверхностным слоем сорбента (адсорбции), выделяют также сорбцию твердого тела или расплава (окклюзию). При сорбции паров твердыми веществами часто происходит капиллярная конденсация.
Способы разделения смесей
Для получения чистых веществ используют различные способы разделения смесей.
| Способы разделения смесей | |
|---|---|
| неоднородных (гетерогенных) | однородных (гомогенных) |
| — Отстаивание — Фильтрование — Действие магнитом — Центрифугирование | — Выпаривание. Кристаллизация. — Дистилляция (перегонка) |
Процессы разделения смесей основаны на различных физических свойствах компонентов, образующих смесь.
Отстаивание
Отстаивание — это разделение неоднородной жидкой смеси на компоненты, путём её расслоения с течением времени под действием силы тяжести.
Отстаиванием можно разделить смесь нерастворимых в воде веществ, имеющих разную плотность.
Пример. Смесь из железных и древесных опилок можно разделить, если высыпать её в сосуд с водой (1), взболтать и дать отстояться. Железные опилки опустятся на дно сосуда, а древесные будут плавать на поверхности воды (2), и их вместе с водой можно будет слить в другой сосуд (3):
На этом же принципе основано разделение смесей малорастворимых друг в друге жидкостей.
Пример. Смеси бензина с водой, нефти с водой, растительного масла с водой быстро расслаиваются, поэтому их можно разделить с помощью делительной воронки:
Отстаиванием также можно разделить вещества, которые осаждаются в воде с различной скоростью.
Пример. Смесь из глины и песка можно разделить, если высыпать её в сосуд с водой (1), взболтать и дать отстояться. Песок оседает на дно значительно быстрее глины (2):
Этот способ используется для отделения песка от глины в керамическом производстве (производство глиняной посуды, красных кирпичей и др.).
Центрифугирование
Центрифугирование — это разделение неоднородных жидких смесей путём вращения.
Пример. Если компоненты неоднородной жидкой смеси очень малы, такие смеси разделяют центрифугированием. Такие смеси помещают в пробирки и вращают с большой скоростью в специальных аппаратах — центрифугах.
Перед центрифугированием частицы смеси распределены по объёму пробирки равномерно. После центрифугирования более лёгкие частицы всплывают наверх, а тяжёлые оседают на дно пробирки.
С помощью центрифугирования, к примеру, отделяют сливки от молока.
Фильтрование
Фильтрование — это разделение жидкой неоднородной смеси на компоненты, путём пропускания смеси через пористую поверхность. В роли пористой поверхности может выступать бумажная воронка, марля, сложенная в несколько слоёв, или любой другой пористый материал, способный задержать один или несколько компонентов смеси.
Фильтрованием можно разделить неоднородную смесь, состоящую из растворимых и нерастворимых в воде веществ.
Пример. Чтобы разделить смесь, состоящую из поваренной соли и песка, её можно высыпать в сосуд с водой, взболтать и затем эту смесь пропустить через фильтровальную бумагу. Песок остаётся на фильтровальной бумаге, а прозрачный раствор поваренной соли проходит через фильтр:
При необходимости, растворённую поваренную соль из воды можно выделить выпариванием.
Действие магнитом
С помощью магнита из неоднородной смеси выделяют вещества, способные к намагничиванию.
Пример. C помощью магнита можно разделить смесь, состоящую из порошков железа и серы:
Выпаривание. Кристаллизация
Выпаривание — это способ разделения жидких смесей путём испарения одного из компонентов. Скорость испарения можно регулировать с помощью температуры, давления и площади поверхности испарения.
Пример. Чтобы растворённую в воде поваренную соль выделить из раствора, последний выпаривают:
Вода испаряется, а в фарфоровой чашке остаётся поваренная соль. Иногда применяют упаривание, т. е. частичное испарение воды. В результате образуется более концентрированный раствор, при охлаждении которого растворённое вещество выделяется в виде кристаллов. Этот процесс получил название кристаллизации.
Дистилляция (перегонка)
Дистилляция (перегонка) — это способ разделения жидких однородных смесей путём испарения жидкости с последующим охлаждением и конденсацией её паров. Данный способ основан на различии в температурах кипения компонентов смеси.
Пример. При нагревании жидкой однородной смеси сначала закипает вещество с наиболее низкой температурой кипения. Образующиеся пары конденсируются при охлаждении в другом сосуде. Когда этого вещества уже не останется в смеси, температура начнёт повышаться, и со временем закипает другой жидкий компонент:
Таким способом получают, к примеру, дистиллированную воду.