Реактивный мезотелий что это
Реактивный мезотелий что это
Считается, что наиболее канцерогенным является минерал крокидолит. При мезотелиомах часто обнаруживается вирус SV 40 (полиомавирус). Однако его роль в возникновении и развитии опухоли остается невыясненной.
Патогенез мезотелиомы
Мезотелиома представляет собой опухоль саркоматозного типа, причем фиброзные и эпителиоидные элементы в ней могут быть настолько анапластичны, что часто новообразование невозможно отличить от плохо дифференцированной карциномы. Выраженность анапластических изменений не совпадает с клинической симптоматикой, наблюдающейся при развитии опухоли. При дифференциальной диагностике очень трудно отличить мезотелиому от аденокарциномы. Для мезотелиом характерен локальный рост, и обычно опухоли поражают ребра и грудную стенку. Раннее распространение опухоли в межреберные связки является причиной развития тяжелых характерных болей.
Опухоль также прорастает диафрагму, инвазирует регионарные лимфатические узлы и обычно метастазирует гематогенным путем. В настоящее время установлено, что важнейшими аутокринными факторами роста опухоли являются ростовой фактор эндотелия сосудов (VEGF), а также тромбоцитарный ростовой фактор (PDGF); отмечена гиперэкспрессия эпидермального ростового фактоpa. Поэтому химиотерапевтические препараты, контролирующие выработку этих факторов, например талидомид, беваку-зимаб (авастин) и гефитиниб, проявляют лечебный эффект.
Разработана система определения стадии развития мезотелиомы, которая позволяет прогнозировать течение заболевания и планировать лечебные мероприятия.
Клиническая картина мезотелиомы
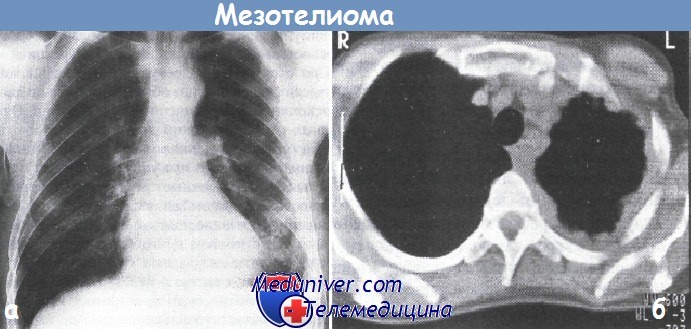
Больные жалуются на усиливающиеся боли в груди, иногда очень мучительные, и на наступление одышки при физической нагрузке. Одышка принимает непрерывный прогрессирующий характер, и часто больные начинают задыхаться, даже находясь в состоянии покоя. При обследовании у них обнаруживаются признаки снижения подвижности грудной клетки и плевральная эффузия. Типичная картина поражения асбестовой пылью на рентгенограмме выглядит как множественные высыпания на плевре, обычно связанные с плевральной эффузией. Для мезотелиомы характерна инвазия плевры и распространение опухоли в средостение. При этом наблюдается «стиснутость» ребер, происходящая за счет сдавления их растущей опухолью.
Диагностика мезотелиомы
Первоначальный диагноз обычно подтверждается после проведения биопсии плевры. В случаях обширного распространения опухоли и невозможности резекции следует избегать диагностической торактомии.
Обычно при этом опухоль распространяется на операционный шов, что причиняет больному дополнительную боль. Для оценки распространения опухоли необходимо провести КТ, особенно близлежащей области плевры и перикарда.
Лечение мезотелиомы
Мезотелиома с трудом поддается лечению. Хирургическое вмешательство возможно лишь в небольшом числе случаев локализованной опухоли, хотя при этом достигается лечебный эффект. Поскольку часто возникают рецидивы, большинство хирургов предпочитают проводить, по возможности, обширную резекцию, с удалением части грудной стенки, диафрагмы, перикарда и, при необходимости, примыкающей доли легкого.
Лучевая терапия, в общем, малоэффективна, хотя в отдельных случаях после облучения рост опухоли замедляется. Облучение всей поверхности плевры затруднительно из-за близости легких, однако появление новых методов тангенциального облучения позволяет надеяться на дальнейшую разработку техники лучевой терапии. Для лечения больных с мезотелиомой использовали разнообразные препараты, однако до недавних пор достигался лишь кратковременный эффект. К числу наиболее эффективных препаратов относятся (в скобках указана примерная эффективность): метотрексат (30%), винорелбин (20%), митомицин (20%), цисплатин (15%), доксорубицин (15%), доцетаксел (10%), гемцитабин (10%).
Гораздо более высокую эффективность (40-50%), хотя на небольших группах больных, проявили новые аналоги фолиевой кислоты — пеметрексед и ралтитрексед. Эти препараты можно считать наиболее эффективными в лечении мезотелиом. Пеметрексед представляет собой аналог фолиевой кислоты, который ингибирует, по крайней мере, три фермента, принимающих участие в синтезе нуклеиновых кислот. На третьей фазе клинических испытаний препарат показал более чем 40%-ю эффективность, и недавно он был разрешен для клинического применения в сочетании с цисплатином при лечении злокачественной мезотелиомы плевры. Это выдающийся результат, полученный при лечении такой трудной опухоли, как мезотелиома, и новый препарат является самым эффективным из известных на сегодняшний день.
В настоящее время больным с мезотелиомой можно назначать сочетание пеметрекседа с цисплатином. Сочетание гемцитабина с цисплатином оказалось эффективным примерно у 35% больных, однако по результатам рандомизированных исследований оно не превышало цисплатин по эффективности. Имеются сообщения об эффективности а-интерферона. Примерно у 20% больных был получен эффект при сочетанном применении интерферона с цисплатином, и у некоторых больных он проявлялся в течение многих месяцев.
Для оценки эффективности других комбинаций химиотерапевтических препаратов, требуются дополнительные исследования. Тем не менее в настоящее время химиотерапия завоевывает место среди средств лечения такой сложной опухоли, как мезотелиома. В ряде случаев, для контроля над распространением опухоли, пытались использовать интраплевральную химиотерапию, однако результаты оказались разочаровывающими. Медиана общей выживаемости больных составляет немногим больше 1 года; к числу неблагоприятных прогностических факторов относятся: наличие опухоли саркоматозного типа, плохое общее состояние больного и лимфоцитоз. Для мужчин характерен менее благоприятный прогноз.
Менее 15% больных живут в течение пяти лет. Медиана выживаемости для неоперабельных больных, получающих поддерживающую терапию, составляет около 6 месяцев. Такие печальные результаты свидетельствуют о необходимости введения жесткого контроля над использованием изделий, содержащих асбест. Больные с опухолью, в прошлом работавшие в асбестовой промышленности, обычно рассматриваются как наиболее вероятные кандидаты на получение соответствующей компенсации в судебном порядке. Недавно в британском законодательстве в данном направлении были приняты новые правовые нормы. Благодаря этому, удовлетворяются иски больных, у которых поражение плевры развилось в результате постоянной стирки рабочей одежды, загрязненной асбестом, или даже вследствие однократного контакта с асбестом на рабочем месте.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Мезотелиома брюшины
Мезотелиома брюшины – злокачественная опухоль, исходящая из клеток мезотелия серозного покрова брюшной полости. Клинически мезотелиома брюшины проявляется абдоминальными болями, тошнотой, рвотой, похуданием, асцитом. Диагностика мезотелиомы основывается на данных УЗИ и МСКТ брюшной полости; решающим диагностическим критерием служит обнаружение атипичных клеток в асцитической жидкости или биоптате, полученном в ходе диагностической лапароскопии. Лечение мезотелиомы брюшины может проводиться хирургическим способом, с помощью лучевой терапии или химиотерапии. Прогноз при мезотелиоме неблагоприятный.
МКБ-10
Общие сведения
Мезотелиома (эндотелиома, карциносаркома) является первичной опухолью, растущей из мезотелиальных клеток, присутствующих в серозных оболочках, выстилающих полости тела. В зависимости от локализации различают мезотелиому брюшины, мезотелиому плевры, реже – мезотелиому перикарда. Среди опухолей данного типа мезотелиома брюшины составляет 10-20% случаев. Развивается мезотелиома брюшины преимущественно у мужчин старше 40 лет.
Причины и формы мезотелиомы брюшины
Считается, что развитие мезотелиомы брюшины и других локализаций напрямую связано с длительным и интенсивным контактированием человека с асбестом. Асбест – тонковолокнистый минерал класса силикатов, часто использующийся в строительной отрасли, металло-, стекло-, автопромышленности и других отраслях производства. Асбестовая пыль очень опасна; ее вдыхание может послужить причиной развития рака легких, асбестоза, мезотелиомы и других заболеваний. При этом от момента контакта с асбестосодержащими материалами до начала болезни могут пройти десятки лет. Среди других факторов не исключается влияние ионизирующего излучения, вирусной инфекции, контакта с силикатами, парафинами.
В зависимости от типа роста мезотелиома брюшины может носить локализованную (узловую) или диффузную форму. В первом случае мезотелиома имеет вид ограниченного узла, исходящего из париетального или висцерального листка брюшины. При диффузной форме мезотелиома имеет инфильтративный рост без четких границ и распространяется по всей поверхности брюшины. Диффузные мезотелиомы брюшины составляют около 75% всех наблюдений и характеризуются более злокачественным течением.
Прогрессирование мезотелиомы брюшины обычно сопровождается накоплением серозного или геморрагического экссудата в брюшной полости и развитием асцита. При мезотелиоме плевры выявляется плеврит, мезотелиоме перикарда – перикардит.
По гистологическому строению выделяют эпителиоидную (50-70%), саркоматоидную (7-20%) и смешанную (20-35%) форму мезотелиомы брюшины. К редким типам мезотелиомы относится мультикистозная форма, которая встречается у женщин и поражает тазовую брюшину, главным образом в области дугласова пространства. С учетом локализации мезотелиомы ее лечение может проводиться специалистами-онкологами в области пульмонологии (торакальной хирургии), кардиологии, гастроэнтерологии, гинекологии.
Симптомы мезотелиомы брюшины
В начальных стадиях проявления мезотелиомы брюшины малоспецифичные. Могут отмечаться дискомфорт и боли в брюшной полости, не имеющие четкой локализации, слабость, похудание. Появляются диспепсические нарушения: тошнота, потеря аппетита, рвота, перемежающиеся поносы и запоры. В дальнейшем, по мере накопления экссудата в брюшной полости, наблюдается увеличение размеров живота, одышка, отеки. При узловой мезотелиоме брюшины во время пальпации может определяться подвижное опухолевое образование. В некоторых случаях имеют место признаки частичной кишечной непроходимости.
Для мезотелиомы брюшины и других локализаций характерен постоянный субфебрилитет, артралгии – боли в мелких суставах летучего характера. Мезотелиома брюшины быстро диссеминирует лимфогенным, контактным, имплантационным путем. Метастазы мезотелиомы брюшины могут обнаруживаться в регионарных лимфоузлах, сердце, легких, печени, кишечнике, головном мозге, костном мозге.
Диагностика мезотелиомы брюшины
Для постановки диагноза необходимо комплексное инструментальное обследование и лабораторное подтверждение мезотелиомы брюшины. Гастроэнтеролога или онколога всегда должен настораживать анамнез жизни пациента, указывающий на имевшийся контакт с асбестом (работа на стройке, проживание в районе асбестоцементных заводов, наличие в доме материалов из асбеста и т. д.).
При подозрении на мезотелиому брюшины выполняется УЗИ брюшной полости, МСКТ, позволяющие выявить наличие асцита и признаки опухолевого процесса. Для точного подтверждения диагноза необходимо проведение лапароцентеза с целью забора и исследования асцитический жидкости. Если злокачественные клетки в экссудате не обнаруживаются, прибегают к диагностической лапароскопии (лапаротомии) и забору биоптата с его последующим морфологическим исследованием. Определение гистологического типа мезотелиомы брюшины имеет важное значение для прогноза и подбора противоопухолевого лечения.
Лечение мезотелиомы брюшины
Оптимальным методом лечения узловых форм мезотелиомы брюшины является радикальное хирургическое удаление опухоли. С целью эвакуации асцитической жидкости проводятся процедуры лечебного парацентеза.
При диффузных процессах показана лучевая терапия, химиотерапия или их сочетание. Химиотерапевтические препараты в различных сочетаниях (доксорубицин, метотрексат, цисплатин, винорелбин и др.) вводятся как внутривенно, так и непосредственно в брюшную полость – внутриперитонеально. Лучевая терапия может проводиться в качестве самостоятельного лечения, паллиативной помощи, вспомогательного лечения после операции для подавления роста опухолевых клеток.
Профилактика и прогноз при мезотелиоме брюшины
Для предотвращения развития мезотелиомы брюшины рекомендуется избегать контакта с асбестом на производстве и дома.
Прогноз при выявлении мезотелиомы брюшины неблагоприятный ввиду быстрой диссеминации опухоли. Обычно после установления диагноза пациенты живут не более 1-2 лет. Наилучший прогноз наблюдается при эпителиоидном типе мезотелиомы брюшины; худший – при саркоматозном и смешанном.
Мезотелиомы брюшины
Мезотелиомы представляют собой редкие опухоли, растущие из мезотелия брюшины.
Современные исследования показывают, что основным фактором риска возникновения подобных опухолей являются токсические воздействия асбеста, пыли стекловолокна или отравления дымом сигарет и другими вредными веществами. Отмечены единичные случаи развития заболевания после лучевой терапии неходжкинской лимфомы и других видов рака.
Типы и формы мезотелиом
Согласно данным макроскопических исследований различают два основных типа злокачественных мезотелиом брюшины:
Особыми формами мезотелиом являются:
Симптомы мезолелиом брюшины
Клинические проявления злокачественных мезотелиом брюшины не специфические. Во многих случаях у пациентов наблюдается асцит. Частыми являются жалобы на боль в области живота, чувство давления, изменения активности кишечника, потерю веса. Реже наблюдается повышение температуры тела. В качестве паранеопластических симптомов отмечались лейкоцитозы, тромбоцитозы и гипогликемия.
Диагностика мезотелиом брюшины
Очень важным при постановке диагноза является дифференциация мезотелиом от метастазов брюшины, которые могут образовываться при следующих видах онкологии:
На основании только клинических и радиологических заключений постановка окончательного диагноза «Мезотелиома» невозможно. Однозначный диагноз возможен лишь после проведения биопсии и гистологического исследования.
Лечение мезотелиом брюшины
В настоящее время наиболее эффективным лечением в Германии мезотелиом брюшины считается химиотерапия. Сегодня медики применяют противоопухолевый препарат Пеметрексед, который ингибирует тимидилат-синтетазу, дигидрофолат-редуктазу, глицинамид-рибонуклеотид-формилтрансферазу. Исследования показывают, что действенной является и комбинация Пеметрексед и Цисплатин. Добавление к терапии препаратов фолиновой кислоты существенно снижает токсичность лечения.
В качестве медикаментозной альтернативы возможно использование Гемцитабина в комбинации с Цисплатином или Карбоплатином.
Сегодня проходит исследование применение гуманизированного моноклонального антитела MORAd-009, направленного против мезотелина, глюкопротеина на поверхности мезотелиомных клеток.
Видео
ВЫПОТНЫЕ ЖИДКОСТИ. ТРАНССУДАТЫ И ЭКССУДАТЫ. ЦИТОЛОГИЧЕСКОЕ ИССЛЕДОВАНИЕ
Еще фото
Автор (ы): О.Ю. КАМЫШНИКОВ ветеринарный врач-патоморфолог, «Ветеринарный центр патоморфологии и лабораторной диагностики доктора Митрохиной Н.В.»
Журнал: №6-2017
Ключевые слова: транссудат, экссудат, выпот, асцит, плеврит
Key words: transudate, exudate, effusion, ascites, pleurisy
Исследование выпотных жидкостей в настоящее время имеет высокую значимость в диагностике патологических состояний. Полученные данные этого исследования позволяют врачу-клиницисту получить информацию о патогенезе образования выпота и корректно организовать лечебные мероприятия. Однако на пути диагностики всегда возникают определенные сложности, способные привести в диагностическую ловушку. Необходимость в данной работе появилась в связи с растущей потребностью в освоении и применении метода исследования выпотных жидкостей в клинике врачами клинической лабораторной диагностики и врачами-цитологами. Поэтому внимание будет уделено как главным задачам врачей-лаборантов – дифференцировать выпот на транссудат и экссудат, так и важнейшей задаче врачей-цитологов – верифицировать клеточный компонент жидкости и сформулировать цитологическое заключение.
Сокращения: ЭС – экссудат, ТС – транссудат, Ц – цитология, МК – мезотелиальные клетки.
Хотелось бы осветить немного исторических данных, сформировавших современный образ лабораторной диагностики выпотных жидкостей. Исследование жидкостей из серозных полостей применялось уже XIX в. В 1875 г. H.J. Quincke и в 1878 г. E. Bocgehold указывали на такие характерные признаки опухолевых клеток, как жировая дегенерация и большие размеры по сравнению с мезотелиальными клетками (МК). Успех подобных исследований был относительно небольшим, так как метода исследования фиксированных и окрашенных препаратов еще не существовало. Пауль Эрлих в 1882 г. и М.Н. Никифоров в 1888 г. описали специфические методы фиксации и окрашивания биологических жидкостей, таких как мазки крови, выпотные жидкости, отделяемое и т.д. J.C. Dock (1897) указал, что признаками раковых клеток служат значительное увеличение размера ядер, изменение их формы и расположения. Он отметил также атипию мезотелия при воспалении. Румынский патологоанатом и микробиолог A. Babes создал основу современного цитологического метода с использованием азуровых красителей. Дальнейшее развитие метода происходило совместно с вхождением в практическую медицину лабораторной диагностики, которая в нашей стране включила в ряды своих специалистов врачей-цитологов. Клиническая цитология в СССР как метод клинического обследования больных начала применяться в 1938 г. Н.Н. Шиллер-Волковой. Развитие клинической лабораторной диагностики в ветеринарной медицине происходило с значительным отставанием, так, первый фундаментальный труд отечественных врачей и ученых этой области знания увидел свет лишь в 1953–1954 гг. Это был трехтомник «Ветеринарные методы исследования в ветеринарии» под редакцией проф. С.И. Афонского, д.в.н. М.М. Иванова, проф. Я.Р. Коваленко, где впервые методы лабораторной диагностики, несомненно экстраполированные из сферы медицины человека, были доступно изложены. С тех давних пор по настоящее время метод исследования выпотных жидкостей постоянно совершенствовался, опираясь на фундамент приобретенных ранее знаний, и сейчас занимает неотъемлемую часть любого клинико-диагностического лабораторного исследования.
В данной работе предпринята попытка осветить основы и суть лабораторного исследования выпотных жидкостей.
Выпотными жидкостями называются компоненты плазмы крови, лимфы, тканевой жидкости, которые накапливаются в серозных полостях. По общепринятому убеждению, выпот – это жидкость в полостях тела, а в тканях по тому же принципу скапливается отечная жидкость. Серозные полости тела – это узкий промежуток между двумя листками серозной оболочки. Серозные оболочки – это пленки, происходящие из мезодермы, представленные двумя листками: париетальным (пристеночным) и висцеральным (органным). Микроструктура париетального и висцерального листка представлена шестью слоями:
2. пограничная мембрана;
3. поверхностный волокнистый коллагеновый слой;
4. поверхностная неориентированная сеть эластических волокон;
5. глубокая продольная эластическая сеть;
6. глубокий решетчатый слой коллагеновых волокон.
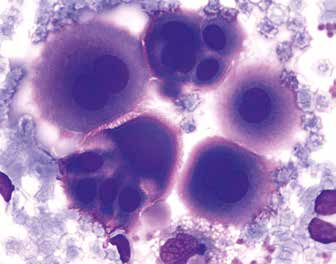
Мезотелий – однослойный плоский эпителий, состоящий из плотно прилегающих друг к другу полигональных клеток. Несмотря на свою эпителиальную форму, мезотелий имеет мезодермальное происхождение. Клетки весьма разнообразны по своим морфологическим свойствам. Можно наблюдать двуядерные и трехъядерные клетки. Мезотелий постоянно секретирует жидкость, выполняющую скользяще-амортизационную функцию, способен к крайне интенсивной пролиферации, проявляет характеристики соединительной ткани. На поверхности МК находится множество микроворсинок, увеличивающих поверхность всей оболочки серозной полости приблизительно в 40 раз. Волокнистый слой соединительной ткани листков серозных оболочек определяет их подвижность. Кровоснабжение серозной оболочки висцерального листка осуществляется за счет сосудов того органа, который она покрывает. А для париетального листка основой системы кровообращения является широкопетлистая сеть артерио-артериолярных анастомозов. Капилляры располагаются сразу под мезотелием. Лимфоотток от серозных оболочек хорошо развит. Лимфатические сосуды сообщаются с серозными пространствами благодаря особым отверстиям – стоматам. По причине этого даже незначительная закупорка дренажной системы может привести к накоплению жидкости в серозной полости. А анатомические свойства кровоснабжения располагают к быстрому возникновению кровотечения при раздражении и повреждении мезотелия.
Клиническая лабораторная диагностика выпотных жидкостей
При лабораторном исследовании решается вопрос принадлежности выпота к транссудату или экссудату, оцениваются общие свойства (макроскопический вид жидкости): цвет, прозрачность, консистенция.
Жидкость, скапливающаяся в серозных полостях без воспалительной реакции, называется транссудатом. Если жидкость собирается в тканях, то имеем дело с отеком (edema). Транссудат может накапливаться в перикарде (hydropericardium), брюшной полости (ascites), плевральной полости (hydrothorax), между оболочками яичка (hydrocele).Транссудат обычно бывает прозрачным, почти бесцветным или с желтоватым оттенком, реже слегка мутноватым из-за примеси слущенного эпителия, лимфоцитов, жира и др. Удельный вес не превышает 1,015 г/мл.
Образование транссудата может быть вызвано следующими факторами.
Одной фразой охарактеризовать образование транссудата можно так: транссудат возникает, когда гидростатическое или коллоидно-осмотическое давление изменяется в той мере, что жидкость, фильтрующаяся в серозную полость, превышает объем реабсорбции.
Экссудатами называются жидкости, которые накапливаются в полостях тела в результате воспалительного процесса. Образование экссудата вызывается микрофлорой (бактерии, грибы), вирусами, паразитами, попаданием в полость желчи, секрета желудка, поджелудочной железы, содержимого желудочно-кишечного тракта, диссеминацией клеток опухоли по серозным полостям.
Макроскопические характеристики экссудатов позволяют отнести их к следующим видам.
1. Серозный экссудат может быть прозрачным или мутным, желтоватым или бесцветным (что определяется присутствием билирубина), разной степени мутности (рис. 1).
2. Серозно-гнойный и гнойный экссудат – мутная, желтовато-зеленая жидкость с обильным рыхлым осадком. Гнойный экссудат встречается при эмпиеме плевры, перитоните и др. (рис. 2).
3. Гнилостный экссудат – мутная жидкость серо-зеленого цвета с резким гнилостным запахом. Гнилостный экссудат характерен для гангрены легкого и других процессов, сопровождающихся распадом ткани.
4. Геморрагический экссудат – прозрачная или мутная жидкость, красновато- или буровато-коричневого цвета. Количество эритроцитов может быть различным: от небольшой примеси, когда жидкость имеет слабо-розовую окраску, до обильной, когда она сходна с цельной кровью. Наиболее частой причиной геморрагического выпота является новообразование, однако геморрагический характер жидкости большого диагностического значения не имеет, поскольку наблюдается и при ряде неопухолевых заболеваний (травма, инфаркт легкого, плеврит, геморрагический диатез). В то же время при злокачественных процессах с обширной диссеминацией опухоли по серозной оболочке может быть серозный, прозрачный выпот (рис. 3).
5. Хилезный экссудат – мутная жидкость молочного цвета, содержащая во взвешенном состоянии мельчайшие жировые капли. При добавлении эфира жидкость просветляется. Такой выпот обусловлен попаданием в серозную полость лимфы из разрушенных крупных лимфатических сосудов, абсцессом, инфильтрацией сосудов опухолью, филяриозом, лимфомой и др. (рис. 4).
6. Хилусоподобный экссудат – молочно-мутная жидкость, появляющаяся в результате обильного распада клеток с жировым перерождением. Так как кроме жира данный экссудат содержит большое число жироперерожденных клеток, добавление эфира оставляет жидкость мутной или просветляет ее незначительно. Хилусоподобный экссудат характерен для выпотных жидкостей, появление которых связано с атрофическим циррозом печени, злокачественными новообразованиями и др.
7. Холестериновый экссудат – густая желтоватого или буроватого цвета с перламутровым оттенком жидкость с блестящими хлопьями, состоящими из скоплений кристаллов холестерина. Примесь разрушенных эритроцитов может придавать выпоту шоколадный оттенок. На стенках пробирки, смоченной выпотом, видны слепки кристаллов холестерина в виде мельчайших блесток. Такой характер имеет осумковавшийся выпот, который длительно существует (иногда несколько лет) в серозной полости. При определенных условиях – обратном всасывании из серозной полости воды и некоторых минеральных компонентов экссудата, а также при отсутствии притока жидкости в замкнутую полость – экссудат любой этиологии может приобрести характер холестеринового.
8. Слизистый экссудат – содержит значительное количество муцина и псевдомуцина, может встречаться при мезотелиоме, слизеобразующих опухолях, псевдомиксоме.
9. Фибринозный экссудате– содержит значительное количество фибрина.
Встречаются также смешанные формы экссудата (серозно-геморрагический, слизисто-геморрагический, серозно-фибринозный).
В нативной выпотной жидкости необходимо провести исследование цитоза. Для этого сразу после пункции жидкость забирают в пробирку с ЭДТА, чтобы предотвратить ее сворачивание. Цитоз, или клеточность (в данном методе определяется только количество ядросодержащих клеток) проводят по стандартной методике в камере Горяева или на гематологическом анализаторе в режиме подсчета цельной крови. За количество ядерных клеток принимают значение WBC (white blood cell, или лейкоцитов) в тысячах клеток на миллилитр жидкости.
После определения цитоза жидкость можно центрифугировать с получением осадка для микроскопического исследования. Надосадочная жидкость, или супернатант, также может исследоваться на содержание белка, глюкозы и т.д. Однако не все биохимические параметры могут быть определены из жидкости с ЭДТА, поэтому рекомендовано также вместе с взятием выпота в пробирку с антикоагулянтом одновременно брать жидкость и в чистую сухую пробирку (например, центрифужную или для биохимического исследования). Отсюда следует, что для исследования выпотной жидкости в лаборатории необходимо получить материал как минимум в двух емкостях: пробирке с ЭДТА и в чистой сухой пробирке, а жидкость должна помещаться туда непосредственно сразу после эвакуации ее из полости тела.
Исследование осадка производится в лаборатории врачом-лаборантом или врачом-цитологом. Чтобы осадить выпотную жидкость, необходимо ее центрифугировать при 1500 об/мин в течение 15–25 минут. В зависимости от вида выпота образуется различный осадок по количеству и качеству (может быть сероватым, желтоватым, кровянистым, однослойным или двухслойным, изредка трехслойным). В серозном прозрачном выпоте осадка может быть крайне мало, его характер мелкозернистый, цвет серовато-белый. В мутном гнойном или хилезном выпоте с большим количеством клеток осадок образуется обильный, крупнозернистый. В геморрагическом выпоте с большой примесью эритроцитов образуется двухслойный осадок: верхний слой в виде белесоватой пленки и нижний в виде плотного скопления эритроцитов. А при разделении осадка на 3 слоя верхний чаще представлен компонентом разрушенных клеток и детрита. При приготовлении мазков на предметных стеклах материал из осадка берется из каждого слоя и приготавливается не менее 2-х мазков. При однослойном осадке рекомендовано изготавливать не менее 4-х стекол. При скудном количестве осадка готовится 1 мазок с максимальным количеством материала в нем.
Высушенные на воздухе при комнатной температуре мазки фиксируются и окрашиваются азур-эозином по стандартному методу (Романовского-Гимзы, Паппенгейма-Крюкова, Лейшмана, Нохта, Райта и т.д.).
Дифференциальная диагностика транссудатов и экссудатов
Чтобы дифференцировать транссудат от экссудата, можно пользоваться несколькими методами, в основе которых лежит определение физических и биохимических параметров жидкости. Различие основано на содержании белка, типе клеток, цвете жидкости и ее удельном весе.
Транссудат, в отличие от экссудата, — выпот невоспалительного происхождения, причем это жидкость, которая накапливается в полостях тела в результате влияния системных факторов регуляции гомеостаза на образование и резорбцию жидкости. Удельный вес транссудата ниже, чем у экссудатов, и составляет менее 1,015 г/мл против 1,015 и более у экссудатов. Содержание общего белка у транссудатов составляет менее 30 г/л против значения, превышающего 30 г/л у экссудатов. Существует качественная проба, позволяющая верифицировать транссудат от экссудата. Это широко известная проба Ривальта. Она вошла в лабораторную практику более 60 лет назад и занимала важное место в диагностике выпотных жидкостей вплоть до развития биохимических методов и их упрощения и доступности, что сделало возможным перейти от качественного метода пробы Ривальта к количественным характеристикам содержания белка. Однако сейчас многими исследователями предлагается использовать пробу Ривальта для быстрого и достаточно точного получения данных о выпоте. Поэтому необходимо немного описать эту пробу.
В узкий цилиндр со слабым раствором уксусной кислоты (100 мл дистиллированной воды + 1 капля ледяной уксусной кислоты) добавляют по каплям исследуемую выпотную жидкость. Если эта капля, падая вниз, дает тянущуюся за ней полоску помутнения, то жидкость является экссудатом. Транссудаты положительную пробу не дают или дают слабо положительную кратковременную реакцию помутнения.
«Цитологический атлас собак и кошек» (2001) Р. Раскин и Д. Мейер предлагают выделять следующие типы серозных жидкостей: транссудаты, модифицированные транссудаты и экссудаты.
Модифицированный транссудат является переходной формой от транссудата к экссудату, содержит «промежуточные значения» концентрации белка (между 25 г/л и 30 г/л) и удельного веса (1,015–1,018). В современной отечественной литературе термин «модифицированный транссудат» не приводится. Однако допускаются формулировки «больше данных за транссудат» или «больше данных за экссудат» на основании результатов параметров дифференциальных характеристик.
В табл. 1 приведены параметры, определение которых позволяет верифицировать транссудат от экссудата.
Табл. 1. Дифференциальные характеристики транссудатов и экссудатов