задержка роста плода до 37 недель на первом скрининге что это значит по крови
Перинатальные и отдаленные исходы у детей с синдромом задержки роста плода
В. Е. Радзинский, А. А. Оразмурадов, Е. А. Девятова
Кафедра акушерства и гинекологии с курсом перинатологии Российского Университета Дружбы Народов
ул. Миклухо – Маклая, 8, Медицинский факультет, 117198, Москва, Россия
Т. В. Златовратская, Н. М. Старцева
ГБУЗ «Городская клиническая больница № 29 им. Н.Э. Баумана» ДЗМ
Госпитальная площадь, д. 2, 111020 Москва, Россия
Актуальность: в статье представлен широкий обзор литературы по проблеме хронической плацентарной недостаточности (ПН), и освещены взгляды, сложившихся на рубеже XX–XXI веков. ПН остается одной из наиболее актуальных проблем современного акушерства и перинатологии, так как перинатальная заболеваемость и смертность в большой мере определяются степенью тяжести ПН, а малый вес при рождении – фактор риска повышенной заболеваемости на протяжении всей последующей жизни ребенка и формирует перинатальную заболеваемость и смертность.
Перинатальные поражения центральной нервной системы приводят к возникновению неврологических осложнений различной степени тяжести, что существенно ухудшает качество жизни таких детей.
При изучении отдаленных исходов у детей с синдромом задержки роста плода (ЗРП) в анамнезе обращает на себя внимание не только большой удельный вес неврологических осложнений, но и высокая частота болезней органов дыхания и болезней крови.
Хроническая ПН остаётся ключевой проблемой акушерства, неонатологии, патологии анте- и перинатального периодов, поскольку функциональная недостаточность плаценты приводит к угрозе прерывания беременности, гипоксии, отставанию роста и развития плода, либо к его гибели ( Савельева Г. М., 1991; Бунин А. Т., 1993; Башмакова Н. В. и др., 1996; Макаров И. О., 1998; Радзинский В. Е., Милованов А. П. и др., 2004). Плацентарная недостаточность – это клинический синдром, отражающий патологическое состояние материнской (маточно – плацентарной) и плодной (плацентарно – плодной) частей плаценты, приводящее к замедлению развития и роста плода (Савельева Г. М. и др., 1991). Милованов А. П., (1999) предложил определение ПН: это клинико – морфологический симптомокомплекс, возникающий как результат сочетанной реакции плода и плаценты на различные нарушения состояния материнского организма. Клинически обоснована терминология и классификация ПН предложенная Радзинским В. Е. (1983, 2001): это поликаузальный синдром, возникающий как результат сочетанной реакции плода и плаценты на различные изменения в материнском организме, характеризующийся нарушением молекулярных, клеточных, тканевых и органных адаптационно – гомеостатических реакций фетоплацентарной системы и реализующийся в компенсированной, субкомпенсированной и декомпенсированной формах. Частота плацентарной недостаточности составляет 17 – 26%, не имеет тенденции к снижению и обусловливает до 47% перинатальных потерь (Колгушкина Т. Н., 2004). По данным Барашнева Ю. И. и др. (1997), частота ее колеблется от 3 – 4 % до 45 %, перинатальная заболеваемость достигает 700 %о, а смертность 24,2 – 177,4%о. По данным других исследователей, ПН составляет более 20% в структуре причин перинатальной смертности (Мурашко Л.Е., Бадоева Ф.С., Асымбекова Г.У., Павлович С.В., 1997).
К основным звеньям многогранного патогенеза ПН относят нарушения маточно – плацентарного и плодово – плацентарного кровотока, метаболизма, синтетической функции и состояния клеточных мембран плаценты, изменения иммунного статуса плода. Патология маточно – плацентарного кровообращения в свою очередь характеризуется тремя важнейшими моментами: нарушением притока крови в межворсинчатое пространство, затруднением оттока из него и локальными изменениями реологических и коагуляционных свойств крови.
Функциональная недостаточность плаценты оказывает прямое отрицательное воздействие на развитие плода и новорожденного, что проявляется характерной клинической симптоматикой, в частности синдромом ЗРП, который занимает важное место в структуре перинатальной смертности и оказывает отрицательное влияние на последующее развитие ребенка. (Борзова Н. Ю., Гагаева Ю. В. и др., 2004). Синдром ЗРП – одно из наиболее часто встречающихся состояний новорожденного (Афанасьева Н. В., Игнатко И. В., 2003). В акушерской практике, по данным Медведева Н. В., Юдиной Е. В. (1998), данная патология встречается в 5 – 31 % случаев.
Учитывая важность своевременной профилактики и диагностики ПН, необходима адекватная оценка степени риска ее развития. По данным Сидельниковой В. М. (2002), хроническая ПН наблюдается у каждой третьей женщины из группы высокого перинатального риска. Легко оцениваемым фактором риска является возраст матери до 18 и старше 35 лет. По данным Стрижакова А. Н. (2003), у 26 – 30 % беременных в возрасте до 20 лет выявляются признаки ПН, что создает угрозу развития ЗРП у данной группы беременных. При наличии экстрагенитальной патологии риск развития ПН составляет 24 – 45%. Важная роль в формировании ПН отведена заболеваниям сердечно – сосудистой и эндокринной систем, а болезни почек составляют до 9,5% среди факторов риска ее развития. Среди эндокринных заболеваний особого внимания заслуживает сахарный диабет. Популяционная частота сахарного диабета у беременных составляет 0,2 – 3,0%, однако среди беременных с ПН он встречается в 2 – 3 раза чаще. При этом частота гипотрофии плода составляет 35,5%, а отставание в росте плода, по данным ряда исследователей, отмечается уже в начале II триместра гестации.
В последние годы все больше внимания уделяется изучению внутриутробного инфицирования как этиологического фактора развития ПН. Так, при хронических неспецифических заболеваниях легких отмечается увеличение процента рождения детей с низкими весо – ростовыми показателями. При этом у 30,8% детей выявляются признаки внутриутробной инфекции. У беременных с ПН на фоне генитальных инфекций в 1,6 раза чаще наблюдается ЗРП, при этом в 2 раза чаще возникает ее симметричная форма.
Среди осложнений беременности, наиболее часто приводящих к развитию ПН, первое место занимает гестоз. При наличии ПН на фоне гестоза, частота ЗРП составляет 22,7 – 44%. Частота клинических проявлений ПН прямо пропорциональна тяжести гестоза и составляет при легкой, среднетяжелой и тяжелой степени 16, 22 и 62% для ЗРП соответственно (Федорова М. В. и др., 1997).
Существенную роль в патогенезе плацентарной недостаточности играет неполноценное питание беременных, прежде всего недостаток белков, жиров, витаминов. При отсутствии рациональной диеты частота ЗРП может достигать 16,2%.
Из данных акушерского анамнеза статистически достоверную связь с развитием плацентарной недостаточности имеют перенесенные ранее самопроизвольные аборты, антенатальная гибель плода и рождение детей с низкой массой тела.
Ранняя диагностика ПН и профилактическое лечение беременных групп высокого риска по развитию синдрома ЗРП позволяет предупредить декомпенсированные формы маточно – плацентарной дисфункции и прогнозировать благополучный исход беременности с высокой степенью вероятности (Афанасьева Н. В., Стрижаков А. П., 2004).
Выявление синдрома ЗРП и определение его формы является основной задачей эхографии при диагностике хронической ПН. ЗРП диагностируется при выявлении параметров фетометрии ниже 10 – го перцентиля или более чем на 2 стандартных отклонения ниже среднего значения для данного гестационного возраста. Некоторые исследователи допускают прогнозирование развития ЗРП по отклонению фетометрических показателей ниже 25 – го перцентиля (Федорова и др., 2001). Однако в этом случае вероятность подтверждения прогноза составляет только 70%.
При ультразвуковой (УЗИ) диагностике ЗРП, говоря о I степени тяжести, наблюдается отставание фетометрических параметров до 2 недель (34,2%), при II степени – в пределах 2 – 4 недель (56,6%), при III степени – более 4 недель (9,2%) от должных значений для данного гестационного срока. Клинически принято выделять симметричную, ассиметричную и смешанную формы данного синдрома. Ассиметричная форма встречается чаще симметричной, но развивается обычно позднее (в 30 – 34 недели гестации). Смешанная форма синдрома ЗРП характеризуется непропорциональным отставанием всех фетометрических показателей при наиболее выраженном отставании размеров живота и считается наиболее неблагоприятной. При обнаружении несоответствия одного или нескольких показателей показано произведение расширенной фетометрии. В то же время отставание фетометрических параметров не всегда позволяет уверенно диагностировать ЗРП. До настоящего времени остаются недостаточно разработанными вопросы тактики ведения беременных с симметричным отставанием размеров плода от срока гестации при отсутствии остальных проявлений ПН, поскольку имеются данные о том, что в этих случаях (генетически детерминированная малая масса, плод «small for date») перинатальные исходы не отличаются от таковых в популяции.
Экстрагенитальные заболевания матери в сочетании с акушерской патологией, реализуясь посредством различных патогенетических механизмов, приводят к единому результату – прогрессирующей ЗРП (Радзинский В. Е., Милованов А. П. и др.,2004). Многолетние наблюдения за развитием детей, родившихся у пациенток с диагностированной ПН, позволили сделать вывод, что акушерская патология обусловливает значительное увеличение перинатальной заболеваемости и является субстратом для возникновения многочисленных патологических изменений в организме ребенка, которые в течение первых лет жизни становятся основной причиной нарушения его физического, умственного развития и повышенной заболеваемости.
По данным Л. О. Бадаляна и др. (1983), более 60% всех заболеваний центральной нервной системы детского возраста связано с перинатальной гипоксией плода. Многие авторы (Paneth N., Stark R., 1983; Seidman D.S., Paz G., 1991 и др.) отмечают, что более половины энцефалопатий обусловлено не острой гипоксией при родах, а длительной, хронической гипоксией плода и новорожденного, нередко связанной с внутриутробной инфекцией. Дети, перенесшие острую гипоксию в родах, чаще имеют совершенно нормальное развитие в дальнейшем (Самсыгина Г.А. и др., 1995).
По данным А. Н. Стрижова и др. (1995), при декомпенсированной форме ПН перинатальная смертность достигает 50%, а заболеваемость новорожденных 100%. ЗРП формирует перинатальную заболеваемость и смертность, а также является фактором риска повышения заболеваемости на протяжении предстоящей жизни. Кроме того, у детей, родившихся маловесными, сокращается средняя продолжительность предстоящей жизни, в сравнении с детьми, не имевшими дефицита веса при рождении (Lithell., 1999). Частота ЗРП по данным многих авторов колеблется от 3% до 22% у доношенных, от 18 до 24% у недоношенных, и не имеет тенденции к снижению (Белоусова В. Б., 1988, Ахмадеева Н. Э. и др., 1989; Радзинский В. Е. и др., 1990).
В структуре перинатальной смертности 23% – 25% занимает ЗРП и связанные с этой патологией осложнения. У 32,5% детей, родившихся с гипотрофией, в возрасте одного года сохраняются отклонения в физическом развитии.
Перинатальные поражения центральной нервной системы занимают одно из важнейших мест в структуре перинатальной заболеваемости по частоте и значимости и составляют 60 – 80% всех заболеваний нервной системы детского возраста ( Студеникин М. Я., Халлман Н., 1984; Яцык Г. В., 1989; Бадалян Л. О., 1989, Барашнев Ю. И., 1993). Перинатальные повреждения головного мозга характеризуются многофакторным генезом, но гипоксия является центральным патогенетическим фактором, приводящим к различным структурным и функциональным повреждениям и порокам развития центральной нервной системы. Характер церебральных изменений зависит от гестационного возраста в период развития патологии, времени действия гипоксии и её интенсивности (Студеникин М.Я. и др., 1993).
Серьёзные неврологические осложнения: такие как детский церебральный паралич, ретинопатиия недоношенных, глухота, грубая задержка темпов психомоторного развития, приводят к неполноценному развитию и снижению качества жизни у таких детей. Неврологические осложнения наиболее распространены у недоношенных детей. Частота неврологических нарушений легкой степени у этих детей составляет 10% – 45 %, тяжелой степени 7% – 9 % (Савельева Г. М., Федорова М. В., Клименко П. А., Сичинава Л. Г., 1991).
Снижение уровня смертности в последние годы сопровождается повышением процента инвалидизации (Cano A., Fons F., Brines J., 2001). Ведущее место среди причин детской инвалидности занимают болезни нервной системы, врождённая и наследственная патология, состояния перинатального периода (Емельянова А. С. 1999).
При снижении летальности новорожденных с массой тела при рождении 1500 г и менее до 49—57%, число выживших детей достигает 43—51%. Однако из выживших детей здоровыми оказываются не более 10—25%. Причем количество детей с тяжелыми психоневрологическими расстройствами может достигать 12—19% (Michelsson K., Lindahl E., Parre M.,1984; Lloyd B. W., 1984; Vohr B.R., Coll C., 1985).
Риск развития психоневрологических расстройств разной степени тяжести у новорожденных с очень низкой массой тела при рождении в 3 раза выше, чем у детей с нормальной массой тела при рождении. Для новорожденных с экстремально низкой массой тела (ЭНМТ) при рождении 1000 г и менее перинатальная смертность может достигать 64—85%, а число выживших детей — не более 15—36%. У выживших детей тяжелые инвалидизирующие расстройства могут превышать 28%, а менее грубые психоневрологические нарушения до 44%. Причем, из выживших детей здоровые составляют не более 8—15% ( HirataT., Epcar J.R., Walsh A.,1983; Fleischman A.R.,1986). При сравнении перинатальных исходов в группах новорожденных с ЭНМТ, 1001 – 1500, 1501 – 2000 и 2001 – 2500 гр. Шалина Р. И. и др., 1999, пришли к заключению, что абдоминальное родоразрешение не позволяет полностью избежать развития мозговых дисфункций, но тем не менее способствует уменьшению числа детей с умеренно выраженными и тяжелыми нарушениями центральной нервной системы.
Изучение отдаленного катамнеза у детей группы высокого инфекционного риска от матерей с внутриутробным инфицированием также представляет большой интерес, поскольку имеются сведения, что у таких детей отмечаются симптомы поражения центральной нервной системы: отставание в психомоторном развитии, прогрессирующие нарушения зрения и слуха (Веденеева Г. Н. и др., 1997; Тареева Т.Г. и др., 1999; Hess D.,1993; Couvreus J. Et al., 1996).
По данным Волгиной С. Я. (2000), в структуре заболеваемости недоношенных детей с ЗРП, в различные периоды жизни выявлялись свои особенности. Доминирующее положение занимают болезни органов дыхания. У детей раннего возраста второе и третье места занимали болезни нервной системы и крови. К 7 годам жизни у значительного количества детей, родившихся с признаками ЗРП, сохраняются изменения неврологического статуса. Развитие этой патологии соотносится со степенью отставания фетометрических показателей и выраженностью признаков внутриутробного страдания плода.
Вывод: состояние здоровья маловесных детей в перинатальном и отдаленном периоде не позволяет приуменьшить значимость проблемы плацентарной недостаточности в настоящее время, а лишь еще раз указывает на необходимость ее детального изучения, своевременной профилактики и лечения.
Вся информация носит ознакомительный характер. Если у вас возникли проблемы со здоровьем, то необходима консультация специалиста.
Внутриутробная задержка развития плода
Общая информация
Краткое описание
Министерство здравоохранения Республики Казахстан
Научный центр акушерства, гинекологии и перинатологии
Основные клинические протоколы и приказы МЗ РК по акушерству и неонаталогии
Протокол: «Внутриутробная задержка развития плода»
Код (коды) по МКБ-10: O36.5 Недостаточный рост плода, требующий предоставления медицинской помощи матери
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Классификация:
1. По времени возникновения:
2. По типу развития:
— симметричная форма: пропорциональное уменьшение всех размеров плода;
— асимметричная форма: уменьшается только окружность живота плода, размер головки и размер трубчатых костей в норме (встречается чаще).
Факторы и группы риска
Материнские факторы:
— инфекции во время беременности у матери (сифилис, герпес, краснуха, токсоплазмоз, гепатит);
— сердечно-сосудистые осложнения (высокое кровяное давление, некоторые сердечные заболевания);
— преэклампсия или эклампсия;
— любая хроническая или длительная болезнь у матери: серповидно-клеточная анемия, системные заболевания, заболевания легких с развитием дыхательной недостаточности, заболевания почек и т.д.
Плацентарные факторы:
— дефекты, связанные с плацентой и пуповиной, которые ограничивают кровоснабжение плода (одна артерия в пуповине, обвитие пуповины вокруг части тела плода; также, истинный узел пуповины, оболочечное прикрепление пуповины);
— недостаточная масса и поверхность плаценты (менее 8% массы тела новорожденного);
— аномалии прикрепления плаценты (низкое расположение плаценты, предлежание плаценты).
Внешние факторы:
— медикаменты (варфарин и фенитоин);
— проживание выше 3000 м над уровнем моря.
Диагностика
Диагностические критерии:
— динамика ВДМ, отраженная в гравидограмме;
— биометрия в динамике;
— биофизический профиль (модифицированный);
— допплерометрия сосудов пуповины, изучение гемодинамики плода.
Перечень основных диагностических мероприятий
Биометрические тесты:
1. Ведение гравидограммы
Прогностическая ценность ВДМ увеличивается при использовании серии исследований и при графическом изображении показателей в виде гравидограммы. Данный график должен быть приложением к каждой обменной карте.
Гравидограмма является скрининговым методом для выявления низкой массы плода для данного срока беременности.
Гравидограмма
2. Ультразвуковая биометрия
Биофизические тесты
1. Модифицированный биофизический профиль плода (БПП).
Выполнение полного протокола исследования БПП требует значительных ресурсов: времени, специальной аппаратуры, обученного специалиста. Поэтому в последние годы предложено использование «модифицированного (сокращенного)» протокола БПП, который включает в себя определение АИ и результаты НСТ.
2. Измерение количества околоплодных вод
Используемые методики для измерения амниотической жидкости:
3. Нестрессовая кардитокография
Антенатальная кардиотокография при сроке беременности свыше 32 недель
Параметры
Нормальная КТГ
Угрожающая КТГ
Патологическая КТГ
Базальный ритм уд./мин.
Менее 100, более 180
Вариабельность базального ритма уд./мин. (средняя)
Амплитуда менее 5 или вариабельность отсутствует
Акцелерации за 30-40 мин.
1-2 или отсутствие при сохранной вариабельности
Отсутствие, при регистрации монотонного, низковариабельного или синусоидального ритма
Нет или неглубокие, вариабельные, ранние
Глубокие пролонгированные вариабельные (до 3-х мин.) или 1-2 поздние единичные
Поздние, неблагоприятные вариабельные (более 70 уд. в 1 мин. и продолжительностью более 60 сек.)
Динамическое наблюдение до родов
Динамический контроль КТГ ежедневный
Общая оценка ситуации, дальнейшее обследование, в некоторых случаях родоразрешение
Приложение
Поздние децелерации возникают в ответ на маточное сокращение, но начинаются либо на высоте схватки, либо с опозданием 15-30 сек. Чаще всего имеет правильную форму, общая продолжительность обычно больше, чем у ранней децелерации, а глубина не превышает 20-25 ударов в 1 мин. Причина поздних децелераций кроется в нарушении кровотока в системе мать-плацента-плод. Поздние децелерации никогда не регистрируются при нормальном состоянии плода и чаще всего сочетаются с другими изменениями кардиотокографических параметров. Поздние децелерации продолжительностью более 1 минуты, являются крайне неблагоприятным прогностическим признаком.
Вариабельные децелерации характеризуются различным временем возникновения. Они вариабельны по форме, продолжительности и глубине. Вариабельные децелерации возникают в силу различных причин, но чаще всего в связи с прижатием петель пуповины. Вариабельные децелерации глубиной от 25 до 60 уд. в 1 минуту и продолжительностью менее 1 минуты не характеризуют выраженное нарушение маточно-плодово-плацентарного кровотока. Децелерации с параметрами, превышающими указанные, относятся к тяжелым.
Знание основных параметров кардиотокограммы и их характеристики позволяют произвести визуальную или рутинную оценку кардиотокографической кривой, которая применима для определения состояния плода после 32 недель беременности. Только к этому сроку заканчивается формирование миокардиального рефлекса и становление цикла «активность-покой» плода. Чем меньше срок беременности, тем изменения на кардиотокограмме менее типичны и, соответственно, тем труднее их интерпретировать.
Для анализа кардиотокографической кривой с 26 недель беременности необходимо использовать автоматический анализ, который позволяет оценивать такие параметры кардиотокографической кривой, которые невозможно учесть при визуальной интерпретации. Эта особенность компьютерной обработки дает возможность расширить сроки проведения исследования. Компьютерный анализ параметров, недоступных при визуальной оценке кардиотокограмм, позволяет исключить субъективную интерпретацию записи и добиться высокой воспроизводимости результатов.
Допплерография (ДГ).
Показания для проведения допплерографии:
— возраст 38 лет и более;
— в анамнезе ЗВРП или гестоз;
Стандартизация проведения допплерографических исследований:
При изучении кривых скоростей кровотока в артериальных сосудах плода наиболее часто оценивают пиковую систолическую скорость кровотока (S), максимальную конечную диастолическую скорость кровотока (D) и усредненную по времени максимальную скорость кровотока (ТМАХ) с последующим расчетом индекса резистентности (ИР) и пульсационного индекса (ПИ).
СД соотношение имеет фиксированное значение и использование его недопустимо, так как численные значения индексов периферического сопротивления как в маточных артериях, так и в артериях плода и пуповины меняются на протяжении беременности.
Частота возможных исходов для плодов и новорожденных при различных видах диастолического компонента, измеренного при допплерометрии пупочной артерии (%)
Исход
Характеристика диастолического компонента кровотока
Расшифровка результатов 1 скрининга при беременности
Комбинированный пренатальный скрининг проводится на 11-14 неделе беременности при размере эмбриона не менее 45 мм и не более 84 мм. Это комплексное обследование плода для оценки параметров его развития. Основная его задача – раннее выявление пороков развития плода, профилактика детской инвалидности, снижение младенческой и детской смертности.
Первый скрининг состоит из инструментальной части – проведение УЗИ и лабораторной – анализ крови на определение концентрации хорионического гонадотропина (βХГЧ) и ассоциированного с беременностью протеина А (РАРР-А). Совокупные результаты этих показателей позволяют спланировать тактику ведения беременности.
Почему обследование проводится на сроке 11-14 недель
Первый триместр – это период формирования всех органов и структур организма. К концу первого триместра заканчивается эмбриональный и начинается фетальный период развития плода. Именно в сроке от 11 недель 1 дня до 13 недель 6 дней беременности наиболее хорошо визуализируются эхографические маркеры хромосомных аномалий.
Кому нужно пройти обследование
По результатам исследования можно судить о риске рождения детей с хромосомными болезнями и врожденными пороками развития, поэтому рекомендуется внимательно отнестись к вопросу и обследоваться всем беременным. Показаниями к обязательному пренатальному скринингу первого триместра являются:
Как подготовиться
Подготовка к первому скринингу выражается в щадящей диете. Погрешности питания могут сказаться на общем состоянии женщины и снизить точность результатов. За неделю до обследования:
За сутки до скрининга:
Желательно соблюдать умеренную физическую активность, если для этого нет противопоказаний. Также важны прогулки, полноценный отдых.
Проведение обследования
Анализ крови и УЗИ выполняются в один день, чтобы избежать погрешностей из-за разницы срока.
Только по расшифровке результатов УЗИ и анализа на гормоны делается вывод о возможных рисках.
Что показывает УЗИ
На скрининге при беременности производится фетометрия плода – определение размеров частей тела и оцениваются все анатомические структуры.
Полученные результаты сравниваются со статистической таблицей, в которой указан процентиль попадания в выборку нормативных значений. При показателях менее 5 и более 95 назначаются дополнительные обследования.
Во время ультразвукового исследования в 1 триместре оценивают следующие параметры: кости свода черепа и головной мозг, позвоночник, передняя брюшная стенка, конечности плода, структуры лица, органы грудной клетки и брюшной полости, а также основные эхографические маркеры хромосомных аномалий.
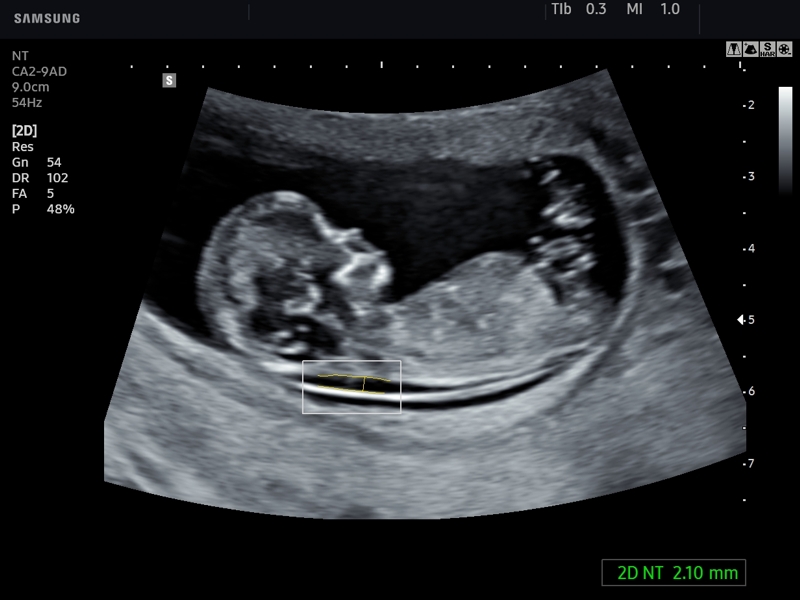
Толщина воротникового пространства (ТВП)
Область между внутренней поверхностью кожи плода и наружной поверхностью мягких тканей, покрывающих шейный отдел позвоночника. ТВП считается наиболее важным маркером хромосомных аномалий.
Это пространство после 13 недели начинает уменьшаться, поэтому возможность его оценить есть только на первом скрининге.
| Срок | Толщина воротниковой зоны в мм | ||
| Процентиль 5 | Процентиль 50 | Процентиль 95 | |
| 11 недель | 0,8 | 1,6 | 2,4 |
| 12 недель | 0,7 | 1,6 | 2,5 |
| 13 недель | 0,7 | 1,7 | 2,7 |
Несоответствие результатов нормативным значениям говорит о повышенном риске развития хромосомных патологий. В зависимости от сформировавшегося набора хромосом, это могут быть синдром Дауна, Патау, Эдвардса, Шерешевского-Тернера. Для уточнения диагноза в этом случае могут быть назначены биопсия хориона или плаценты, анализ пуповинной крови, околоплодных вод. Только после проведения дополнительных исследований можно поставить точный диагноз.
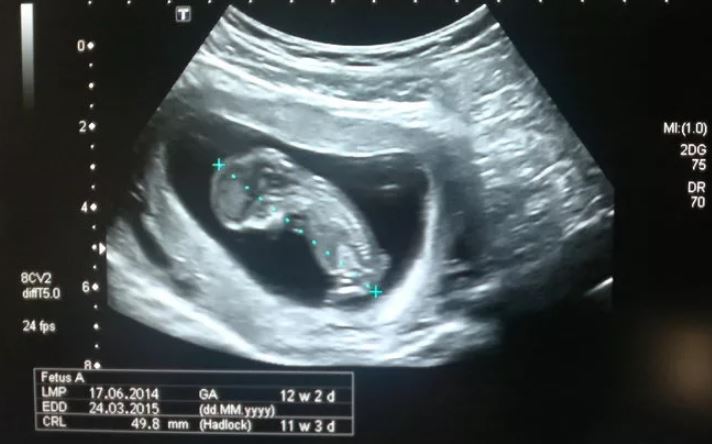
Копчико-теменной размер (КТР)
Показывает расстояние между копчиковой и теменной костями. По этому параметру на УЗИ определяют точный срок гестации, а также устанавливают соотношение массы плода к его КТР.
Незначительное отклонение от норм говорит об особенностях телосложения и не является поводом для беспокойства.
| Срок | Копчико-теменной размер в мм | ||
| Процентиль 5 | Процентиль 50 | Процентиль 95 | |
| 11 недель | 34 | 42 | 50 |
| 12 недель | 42 | 51 | 59 |
| 13 недель | 51 | 63 | 75 |
Если скрининг при беременности показал результаты, превышающие нормы, это указывает, что плод достаточно крупный. Показатель существенно меньше говорит либо о неправильно определенном сроке гестации (в этом случае проводится повторное обследование через 1-1,5 недели), либо о замедлении развития вследствие внутриутробной гибели, нарушенного гормонального фона или инфекционного заболевания матери, генетических отклонений.
Кости свода черепа и головной мозг
Уже с 11 недели при УЗ-исследовании можно обнаружить дефекты костей черепа, что говорит о тяжелых пороках развития плода, несовместимых с жизнью. Оценка головного мозга основана на изучении так называемой «бабочки» – сосудистых сплетений боковых желудочков. Четкая визуализация и ее симметричность говорит о нормальном развитии головного мозга.
| Срок | БПР, ЛЗР в мм | ||
| Процентиль 5 | Процентиль 50 | Процентиль 95 | |
| 11 недель | 13, 19 | 17, 21 | 21, 23 |
| 12 недель | 18, 22 | 21, 24 | 24, 26 |
| 13 недель | 20, 26 | 24, 29 | 28, 32 |
Носовая кость
К концу триместра она должна быть сформирована, четко визуализироваться.
| Срок | Носовая кость в мм | ||
| Процентиль 5 | Процентиль 50 | Процентиль 95 | |
| 11 недель | визуализируется, не измеряется | визуализируется, не измеряется | визуализируется, не измеряется |
| 12 недель | 2 | 3,1 | 4,2 |
| 13 недель | 2 | 3,1 | 4,2 |
Патологией носовой кости считается ее отсутствие, гипоплазия (очень маленькие размеры) и изменение ее эхогенности.
Диаметр грудной клетки, окружность головы и живота, длина бедренной кости также позволяют судить о пропорциональности развития.
Состояние сердца
При исследовании сердца оценивается его расположение, устанавливается наличие четырех камер сердца – два предсердия и два желудочка и оценивается их симметричность. Измеряется частота сердечных сокращений.
| Срок | Частота сердечных сокращений в ударах за минуту | ||
| Процентиль 5 | Процентиль 50 | Процентиль 95 | |
| 11 недель | 153 | 165 | 177 |
| 12 недель | 150 | 162 | 174 |
| 13 недель | 147 | 159 | 171 |
Венозный проток (ВП) – прямая коммуникация между пупочной веной и центральной венозной системой. При нормально развивающейся беременности кровоток в ВП представляет собой трехфазную кривую. Появление реверсного кровотока может говорить о наличии патологии плода.
Что показывает анализ крови
Результаты УЗИ сопоставляются с показателями ассоциированного с беременностью протеина А из плазмы матери (PAPP-A) и хорионическим гонадотропином человека (ХГЧ). Значения приведены в таблице:
| Срок | ХГЧ в нг/мл | PAPP-A в мЕд/л |
| 11 недель | 17,4 – 130,4 | 0,46 – 3,73 |
| 12 недель | 13,4 – 128,5 | 0,79 – 4,76 |
| 13 недель | 14,2 – 114,7 | 1,03 – 6,01 |
Отличия от референсных значений может говорить о патологиях матери или плода.
Интерпретация обследования
Первое исследование оценивается только по совокупности всех показателей. Отдельно взятый параметр не может стать основанием для точного заключения. В протоколе фиксируются данные УЗИ, анализа на гормоны, отражаются риски вероятных заболеваний и комплексный медианный коэффициент MoM. Он указывает совокупное отклонение полученных результатов от средних значений. Коэффициент должен находиться в интервале от 0,5 до 2,5. Рассчитывается он специализированными программами.
Что может повлиять на результат
Современное диагностическое оборудование позволяет оценить более 15 параметров плода, построить его объемную реконструкцию для исследования органов на ранних периодах развития, рассчитать возможные риски с высокой точностью. Обращайтесь в хорошо оснащенные клиники и доверяйте специалистам с подтвержденной квалификацией.