Карбонатная жесткость воды на что влияет
Карбонатная жесткость воды: определение, понятие жесткой и мягкой воды, химические и физические свойства, единицы измерения и способы устранения проблемы
Достоверная информация о качестве питьевой воды интересует всех. Этому посвящена масса сайтов в сети, но среди них преобладают ресурсы заинтересованных сторон: производителей бутилированной воды и фильтров для очистки. Поэтому лучше разбираться в «водном» вопросе с помощью независимых информационных ресурсов и собственной логики.
Все дело в солях, а если точнее – в их количестве. Если их много, вода жесткая, мало – вода мягкая. Дистиллированная вода солей не содержит вовсе, и сразу скажем, что в качестве питьевой она однозначно не годится.
Термин «жесткая» произошел неслучайно: ткань после стирки с мылом в воде с высоким содержанием солей на ощупь была на самом деле жесткой.
Жесткая вода
Жесткость бывает двух видов:
Нас с вами интересует первый вариант, потому что именно он является карбонатной жесткостью. У нее волнообразный сезонный характер. Дело в том, что гидрокарбонаты «подмешиваются» в природную воду во время ее протекания через горные породы типа известняков, гипса или доломитов. Если вода поверхностная, самый высокий процент «подмешивания» происходит зимой: зимняя вода относительно жестче. Меньше всего гидрокарбонатов в весенней воде, особенно во время половодья и паводков: идет серьезная разбавляющая добавка талых и дождевых вод.
Подземные природные воды, в отличие от поверхностных, более жесткие и постоянные по своему составу: от сезонов они никак не зависят.
Единицы измерения карбонатной жесткости воды в России и за рубежом
В единицах измерения удивительная международная путаница. Удивительная потому, что способы и единицы измерения других процессов или предметов приведены под единые международные измерительные системы давным-давно. Этим делом занимаются многочисленные метрологические международные и национальные организации. Почему карбонатная жесткость и другие свойства воды измеряются до сих пор в каждой стране по-своему, остается только гадать. Судите сами:
Теперь единицы измерения в странах в сравнении по количеству гидрокарбонатов в кубическом дециметре воды:
С этим международным хаосом справиться можно. На многих сайтах, посвященных воде, встроены специальные таблицы и калькуляторы для перевода данных из одной системы единиц измерения в другую. Чтобы понять, к примеру, какая карбонатная жесткость приемлема для экзотических золотых рыбок со всеми данными во французском сертификате.
Нормативы содержания солей в воде
По жесткости воды, включая карбонатную жесткость, ВОЗ никаких рекомендаций не дает. Лимиты указаны только для содержания двух щелочноземельных металлов: кальций в пределах 20–80 мг/л, а магний в пределах 10–30 мг/л.
Виды и свойства жесткой воды
Природные воды в основном характеризуются общей жесткостью, поэтому они делятся на группы по этому критерию:
Теперь внимание, несколько слов об одной очень простой химической реакции. Если прокипятить воду с растворенными в ней гидрокарбонатными солями, эти соли потеряют свою приставку «гидро» и превратятся в обычные карбонатные соли. А карбонатные соли никогда не были растворимыми, они формируются в виде осадка – той самой накипи, которую мы так не любим на дне чайника.
О накипи
В любой природной воде обязательно присутствуют хорошо растворимые гидрокарбонаты, которые при кипячении дадут нам накипь. Самое интересное, что любая бутилированная питьевая вода хорошего качества тоже даст нам накипь при кипячении. Так что тем, кто ошибочно полагает, натуральная родниковая вода не должна давать осадка при кипячении, пора освобождаться от этого стереотипа.
Не нужно бояться накипи, это вполне естественный химический процесс для любой качественной воды. Более того, если купленная вами бутилированная вода вообще не дает накипи, нужно проверить ее на содержание кальция и магния: скорее всего, их там нет в нужном количестве. Вы ведь покупали не дистиллированную воду, верно?
Настоящие жертвы жесткой воды: трубы, стояки и котлы
Соли магния и кальция выпадают осадком не только при кипячении, но и при обычных условиях. Вспомните белый налет на смесителях и трубах в ванной комнате. Это лишь то, что видно вашему глазу. А вот водопроводные трубы крупного калибра, котлы и стояки могут быть покрыты с внутренней стороны серьезным слоем известкового налета. Ни к чему хорошему он не приведет: трубы будут перегреваться и выходить из строя из-за свищей и формирования весьма неприятной подшламовой коррозии.
С другой стороны, слишком мягкая вода в водопроводной сети также принесет неприятности в виде коррозии металлических труб. Так что все хорошо в меру: умеренный уровень солей в воде в сочетании с контролем состояния внутренних стенок магистральных водных трубопроводов.
Ну а самый лучший способ решения «трубной» проблемы – производство и использование водопроводных труб из новых композитных материалов.
Способы умягчения воды
Если два первых метода относились к карбонатной жесткости, то с постоянной жесткостью бороться сложнее. Но и это вполне реально:
Теперь промышленные технологии избавления:
Жесткая вода и мифы о здоровье
Карбонатная жесткость воды негативно влияет на кожу: при умывании она ее сушит кожу. В такой воде плохо образуется пена при использовании мыла или других моющих веществ. Эти факты многократно проверенны и стоит принять их во внимание.
А вот с двумя другими «страшилками», связанными с потреблением воды с высокой карбонатной жесткостью, необходимо разобраться. Речь о поражении кожи в форме экземы и мочекаменной болезни – двух самых популярных заболеваниях, приводимых производителями бутилированной воды и водных фильтров для очистки.
Формулировки в таких источниках осторожные: «есть данные, что высокая жесткость способствует образованию мочевых камней…». А если заглянуть в профессиональные ресурсы для клинических врачей, то там вполне ясные. Большинство исследований свидетельствуют о том, что жесткость потребляемой воды никак не влияет на риск образования камней.
Такая же история с экземой и диатезом у детей. Одним словом, читайте медицинские ресурсы.
Вода для аквариума и ее показатели
Для обитателей аквариумов важны оба вида жесткости воды: и постоянная, и временная карбонатная.
Многочисленные тесты определения качества аквариумной воды выпускаются для определения постоянной жесткости – уровня ионов Ca++ и Mg++.
Нормативы карбонатной жесткости в аквариуме являются обязательными, так как играют важнейшую роль в жизни рыб.
Жесткость воды в аквариуме должна находится в пределах 3-15°Ж.
Важно помнить, что обитатели аквариума активно потребляют кальций, поэтому его концентрация будет постоянно снижаться. Это нужно контролировать и поддерживать норму состава аквариумной воды также постоянно.
В качестве заключения хочется пожелать читателям грамотного и взвешенного отношения к своему здоровью. Это означает информационную независимость и умение делать собственные выводы о том, как себя вести и какую воду пить.
Карбонатная жесткость воды на что влияет
Гидрокарбонатные ионы могли оказаться в воде не только при растворении солей кальция и магния, поэтому судить о наличии ионов Ca 2+ и Mg 2+ по содержанию гидрокарбонатных ионов можно далеко не всегда.
Если строго следовать определению карбонатной жесткости, то ее корректное измерение должно быть основано на кипячении заданного объема воды с последующим взвешиванием образовавшегося осадка (накипи). На практике это трудно выполнимо. Поэтому поступают иначе. Вот как определяют «карбонатную жесткость» с помощью общепринятой лабораторной методики.
И соляная кислота, и метиловый оранжевый очень распространенные реактивы. Их всегда можно купить в магазине химических реактивов, достать в школьных химических кабинетах, лабораториях водоканала. Они есть в любой химической лаборатории.
Приготовление реактивов
Для приготовления 0.05М раствора соляной кислоты 4 мл покупной 38% соляной кислоты растворяют в дистиллированной воде (примерно в 200-300 мл), затем доводят все той же водой раствор до 1 литра.
Концентрированная соляная кислота ОПАСНОЕ ВЕЩЕСТВО. ОНА НЕ ДОЛЖНА ПОПАДАТЬ НА РУКИ И ОДЕЖДУ. ВДЫХАНИЕ ЕЕ ПАРОВ ВРЕДНО!
Поэтому при работе с этим веществом соблюдайте максимальную осторожность.
ПРИ ЕГО РАЗБАВЛЕНИИ ВСЕГДА НАДО ДОБАВЛЯТЬ КИСЛОТУ В ВОДУ, А НЕ ВОДУ В КИСЛОТУ!
Разбавленная до указанной концентрации соляная кислота никакой опасности не представляет.
Для приготовления раствора индикатора небольшое его количество, 0.1 г растворяют в 100 мл дистиллированной воды. Точность здесь не требуется, можно все сделать на глазок.
Проведение анализа
Точно отмеряют 50 мл исследуемой воды. Добавляют несколько капель раствора метилового оранжевого, столько, чтобы окраска пробы получилось такой как в левом стаканчике на приведенном ниже рисунке:
Далее проводят титрование пробы кислотой до изменения цвета индикатора (правый стаканчик).
При титровании в растворе произойдут следующие реакции:
Давайте сравним это и приведенное выше уравнение, которое показывало, что происходит с гидрокарбонатом кальция при кипячении. Как и при кипячении, конечными продуктами этих реакций являются вода и углекислый газ. Только вот кальций никак тут не участвует. Это и понятно, ведь ионы водорода, которые образуются в растворе при добавлении туда соляной кислоты вступают в реакцию не с ионами кальция, а именно с гидрокарбонатными ионами.
То есть если вы титровали 50 мл воды 0.05 М соляной кислотой, то в этом случае карбонатная жесткость в мг-экв/л будет численно равна объему кислоты (в мл), израсходованному для титрования.
Например, если на титрование ушло 1.5 мл раствора кислоты, то карбонатная жесткость воды равна 1.5 мг-экв/л. Для перевода в градусы KH значение в мг-экв/л надо умножить на 2.804: 1.5*2.804=4.2°KH.
Что значит ‘мягкая вода’ и ‘жёсткая вода’
Чтобы не загружать голову терминами, обоснованиями и способами измерения жёсткости, можно всё это пропустить, и сразу перейти к способам изменения жёсткости воды.
Жёсткость и солёность
Жёсткость определяется именно солями кальция и магния (Ca и Mg), или солями жёсткости. Само понятие «жёсткость» пошло, видимо, от простого и понятного каждому процесса стирки белья: после жёсткой воды и бельё было жёстким вследствие того, что соли кальция осаждались на волокнах, изменяя их упругость и другие свойства. В мягкой воде, наоборот, этого не происходит, и ткани остаются мягкими.
Жёсткость общая и карбонатная
Жёсткость бывает разной. Та жёсткость, которая определяется растворёнными солями кальция (о ней, как правило, и идёт речь) называется кальциевой. Соответственно, та, которую обусловливают соли магния, зовётся магниевой. Эти два параметра редко используются в аквариумистике. Кроме того, в основном в природных водах преобладают соли кальция, а магний встречается в меньшем количестве, за редким исключением. Поэтому чаще всего, когда говорят о жёсткости, имеют в виду именно кальциевую жёсткость воды.
Карбонатную жёсткость ещё называют временной жёсткостью, потому что она может колебаться в зависимости от того, сколько карбоната кальция выпадает в осадок: чем больше его выпало, тем меньше остаётся в растворе. Правда, карбонаты могут растворяться в воде, превращаясь опять в гидрокарбонаты (или другие соли, о чём мы ещё поговорим). То есть карбонатная жёсткость постоянно немного колеблется. Это значит, что на неё мы можем повлиять (ниже расскажем, как это делается).
В каких единицах измеряют жёсткость
Но для большинства аквариумистов и это избыточно сложно.
Карбонатная жёсткость воды измеряется в тех же самых единицах с теми же самыми концентрациями, но только для карбонатов и гидрокарбонатов. В аквариумистике её выражают значком KH ( от немецкой аббревиатуры ).
Ничего страшного, это всё было для общего развития. На самом деле в аквариумистике это всё обычно не употребляется, и считать, переводить градусы жёсткости в миллимоли на литр никто не станет. Ну, если только очень захочется.
Ни рыбы, ни растения, ни сам аквариумист не ощутят изменения жёсткости на 1 градус. И даже на два, скорее всего, не заметят. Поэтому в аквариумистике принята приблизительная оценка жёсткости, которая выглядит примерно так:
Карбонатная жёсткость всегда меньше общей. Вот всегда. ВСЕГДА. ВСЕГДА-ВСЕГДА, и точка. Она нам обычно бывает нужна, когда мы выращиваем растения с особыми требованиями к воде или собираемся разводить мягководных рыбок (тех. которые в природе обитают в воде с низким содержанием кальция). Тут обычно расчёт примерно такой:
А как быть, когда получается результат, например, GH = 5, KH = 10? Такое может быть? Может, ещё как может. Но это не значит, что карбонатная жёсткость выше общей. Это связано со способом измерения жёсткости аквариумными тестами. Об этом мы сейчас тоже расскажем.
Как измеряется жёсткость аквариумной воды?
В аквариумистике обычно измерения производятся при помощи капельных тестов (все наиболее известные аквариумные фирмы производят такие тесты для измерения самых разных параметров воды). Жёсткость воды измеряется тестом на GH.
Как так? Почему только на GH? Очень просто. Этот тест определяет количество ионов кальция в воде при помощи реакции на соответствующие ионы. То есть тест на GH определяет ВЕСЬ кальций, который содержится в определённом объёме воды. И чем больше кальция в воде, тем интенсивнее будет цвет раствора в мерном стаканчике. А дальше мы по предложенной производителем шкале определяем соответствие цвета раствора определённому числу градусов жёсткости воды. То есть очень приблизительно определяем общую жёсткость.
А что покажет нам тест на KH? Правильно, он покажет повышение. Но не самой карбонатной жёсткости, а всех карбонат-ионов в растворе.
Собственно говоря, акварумисту гидрокарбонаты, в общем-то, важнее, потому что именно они определяют и буферность воды (об этом мы поговорим отдельно), и активную реакцию (рН), и оплодотворяемость икры рыб. Так что пользоваться этим показателем можно и нужно. Просто надо пнимать, что между собственно KH и «тестом на KH» есть существенная разница.
Зачем нам всё это надо?
Малавийских цихлид в мягкой воде не удержишь, им будет плохо
Для растений карбонатная жёсткость важна в трёх отношениях. Во-первых, чем выше карбонатная жёсткость, тем более стабильна кислотность воды (рН). Жёсткая вода имеет щелочную реакцию, и изменить её тем труднее, чем выше содержание гидрокарбонатов (это свойство называется буферностью). Во-вторых, каждому значению карбонатной жёсткости соответствует определённое количество растворённого в воде углекислого газа, доступного для растений. Чем выше жёсткость, тем менее доступен для растений углекислый газ и тем больше его должно поступать в систему. В-третьих, растения хоть и плохо, но могут поглощать углерод из гидрокарбонатов, что приводит к выпадению нерастворимого CaCO3 в осадок на листьях растений и образованию на них белого налёта. Это довольно опасный процесс, поскольку в результате карбонатная жёсткость хотя и снижается, но падает и буферность. Рыбы и растения могут страдать от резких скачков рН.
Икра голубых неонов, как и многих других харациновых, в жёсткой воде не оплодотворяется
Как управлять жёсткостью воды
Уменьшить общую жёсткость в аквариуме можно несколькими способами.
1. Разбавив аквариумную воду дистиллированной водой (в такой воде содержание растворённых солей сведено к возможному минимуму, почти к нулю). К сожалению, способ это довольно затратный: приобрести дистиллированную воду можно в автомагазине или в некоторых аптеках, но придётся за неё заплатить, а если нужно смягчать большой объём (200-300 л и более), то сумма получается внушительная.
А вообще даже собранную с шиферной крыши воду можно использовать для умягчения, если отстоять её около получаса (чтобы осела вся муть) и собрать основную часть, удалив осадок. Этим способом издавна пользовались разводчики мягководных рыбок, живущие в местах, где других источников мягкой воды нет.
Этот способ смягчения воды прост, безопасен и не требует каких-то специальных условий, кроме места в морозилке. Зато тратит драгоценное время (и испытывает терпение родных, которым почему-то именно в такие моменты морозилка бывает нужна позарез).
4. Сильно смягчить воду можно при помощи ионообменных смол, заменяющих ионы кальция и магния в пропускаемой через них воде на ионы натрия. Но это не самый удачный способ: высокая концентрация натрия препятствует усвоению растениями калия, а рыб, вследствие усиленной нагрузки на единственную почку, она часто приводит к водянке.
2. Ещё можно снижать карбонатную жёсткость пропусканием постоянного электрического тока через ёмкость, разделённую пористым материалом. Но это уже скорее из области фантастики, оно мало производительно по сравнению с кипячением.
4. В принципе, можно при помощи гашеной извести и пищевой соды уменьшить и некарбонатную, и карбонатную жёсткость, но в аквариумистике этот способ не применяется потому, что из раствора кальций и магний выводятся, но при этом заменяются натрием, который и для рыб, и для растений в больших количествах вреден.
5. Ещё можно использовать различные кондиционеры на основе сложных комплексных солей, образующих связывающие кальций и магний хелатные соединения. Например, раньше был популярен так называемый «Трилон-Б», эффективно смягчавший воду. Но такие реактивы не всегда просто добыть, и стоят они не особенно дёшево.
Проще и быстрее всего для смягчения воды использовать фильтр обратного осмоса. Не вдаваясь в физические подробности процесса, скажем, что под высоким давлением молекулы воды проталкиваются через микропористую мембрану, а более крупные ионы солей остаются в растворе и сливаются. Таким образом можно очень существенно снизить жёсткость воды (например, после нашего фильтра карбонатная и общая жёсткость вообще перестают тестироваться капельными тестами).
В старых книгах фильтры обратного осмоса признавались малопригодными для аквариумистов из-за очень высокой стоимости, громоздкости и трудности замены мембран. На сегодняшний день производители фильтров давно решили все эти проблемы, и в продаже можно найти модели стоимостью от 15 000 до 2 500 рублей. Мы пользуемся одной из самых бюджетных, но при этом вполне довольны качеством фильтрации, которое позволяет успешно содержать мягководные растения и разводить самых чувствительных рыб.
При использовании обратноосмотрической воды, как и дистиллированной, нужно помнить, что для постоянного содержания и рыб, и растений в чистом виде её использовать нельзя: ведь в ней отсутствуют практически все растворимые соли, в том числе жизненно необходимые для рыб и растений. Поэтому для постоянного содержания «осмотическую» и дистиллированную воду добавляют к обычной водопроводной, при помощи тестов достигая нужных показателей жёсткости. А для растений, содержащихся в значительных объёмах такой воды, обязательно необходимо вносить в воду микроэлементные удобрения и соли калия.
Ещё необходимо помнить, что при использовании воды, полученной путём обратного осмоса, её рН какое-то время остаётся тем же, что был в водопроводной воде. И только после нескольких часов отстаивания, по мере растворения углекислого газа, этот показатель сначала падает до нейтрального значения (рН = 7), а потом и переходит в кислую сторону (рН меньше 7). Если долго держать такую смягчённую воду, она может стать довольно кислой (рН может упасть до 5 и даже до 4). Это нужно учитывать, чтобы не создать стресс рыбам при подмене воды.
Как увеличивают жёсткость воды. Если в аквариуме, наоборот, вода слишком мягкая, то есть два пути её повышения:
Декорируя аквариумы известняком, мы повышаем жёсткость воды
2. Растворить в воде специальные соли. Можно воспользоваться для этой цели специальными солевыми смесями, которые производят аквариумные фирмы специально для тех, кто хочет содержать африканских озёрных цихлид, но мягкая вода не позволяет этого. К таким относятся, например, «Instant Cichlid» от Aquarium Systems, «Sera MineralSalt» и другие.
А можно воспользоваться простым рецептом, который рекомендуют американские аквариумисты: для малавийских цихлид на 20 литров осмосной воды они вносят
1 столовую ложку MgSO4,
1 столовую ложку пищевой соды (Na2CО3),
1 чайную ложку морской соли (не той, которая продаётся в продуктовых магазинах, а настоящей соли для морских аквариумов).
Ещё не помешает внести немного калия, особенно если в аквариуме предполагается выращивать водные растения (если растения будут основными обитателями аквариума, то воду вообще лучше подготавливать отдельно по особым рецептам).
Намного проще и приятнее использовать с этой целью крепкий раствор лимонной кислоты: чайная ложка растворяется в стакане горячей воды. Ну, или на глаз, сколько не жалко. Хотя в принципе лимонная кислота не особенно сильно раздражает кожу даже в высокой концентрации, лучше использовать её только в перчатках. Зато в отличие от уксусной она не имеет запаха, а с налётом тоже справляется отлично. Достаточно пропитать ей ватный диск или кусочек поролоновой губки, отжать (лить кислоту в аквариум нам ни к чему) и несколько раз провести этой губкой по карбонатному налёту. Результат вы увидите очень скоро. Чтобы кислота не попала в аквариум при подмене, после обработки стекло хорошо бы протереть мягкой водой. И проблема будет благополучно решена.
Карбонатная жесткость воды: что это и как влияет на вкус кофе
Нельзя просто выбрать воду с низким содержанием карбонатов


Чашка фильтр-кофе на 98,5% состоит из воды, а её качество имеет большое значение для кофе.
Общая и карбонатная жесткость — ключевые параметры, которые определяют качество воды. За общую жесткость отвечают хлорид кальция (CaCl2), сульфат кальция (CaSO4), хлорид магния (MgCl2) и сульфат магния (MgSO4). За карбонатную — бикарбонат калия (KHCO3) и бикарбонат натрия (NaHCO3).
Соли магния и кальция помогают извлечь из кофе больше вкуса и не выпадают в осадок при кипячении воды. А вот с бикарбонатами все не так просто. Вода, которая перенасыщена карбонатами, образует накипь. При кипячении воды соли выпадают в осадок и могут привести к поломке кофемашины.
Казалось бы, выбирайте воду с низким содержанием карбонатов, и проблема решена. Но недостаточное количество карбоната кальция в воде может вызвать коррозию бойлера и трубок. А главное — содержание бикарбонатов влияет на воспринимаемую кислотность кофе.
Мы уже рассказывали о том, как состав воды влияет на экстракцию. Теперь разбираемся, как карбонатная жесткость влияет на pH воды и вкус кофе.
Как карбонатная жесткость влияет на pH воды
Чтобы стабилизировать pH воды, нужна буферная система. А основная буферная система в воде — это как раз бикарбонаты Ca(HCO3)2. Если в воде будет много бикарбонатов, они «уничтожат» положительную кислотность кофе.
В кофе насчитывается более 40 органических кислот. От вида и соотношения кислот зависит вкус напитка: будет ли это приятная искристая кислотность или неприятная уксусная. Для этого в индустрии спешелти проводят эксперименты с ферментацией — процессом, при котором количество кислот в кофе увеличивается.

От вида и соотношения кислот в кофе зависит вкус напитка. А состав воды определяет экстракцию этих кислот
Большинство кислот в кофе слабые. Это значит, что даже незначительные отклонения в составе воды могут сильно повлиять на вкусовые свойства. Если взять воду с разным исходным ppm — уровнем минерализации — ppm кофе на выходе будет одинаковым, а вот вкус разным. Все потому, что разная вода по-разному растворяет вещества из кофе.
Итак, вкус кофе меняется в зависимости от параметров воды. Когда уровень pH понижается, растет кислотность воды, и кофе получается кислым. Если уровень pH повышается, во вкусе кофе появляется горечь. Чтобы уровень pH оставался стабильным, в воде должны содержаться бикарбонаты. Нужно только подобрать оптимальное соотношение минеральных веществ в воде.
Как подобрать допустимый диапазон карбонатной жесткости
Specialty Coffee Association выпустила стандарты, согласно которым допустимый диапазон карбонатной жесткости: ± 40 ppm. Карбонатная жесткость измеряется по шкале KH, а общая — по шкале GH.
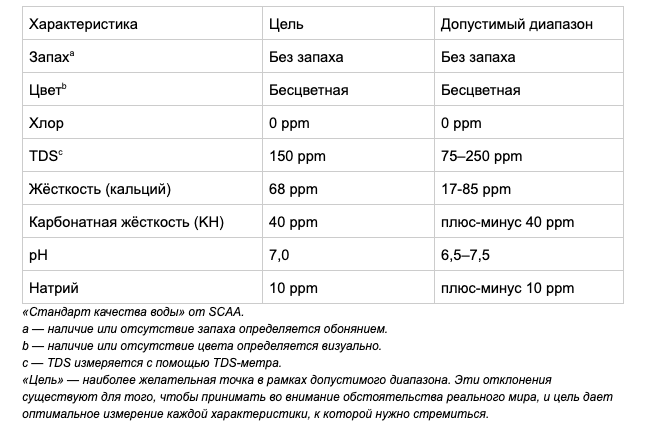
Целевые показатели воды от SCA
Спецификация расплывчата, непонятно, что означает «плюс-минус» в отношении диапазона KH. Максвелл Колонна-Дэшвуд и Кристофер Хэндон в книге «Вода для кофе. Наука. История. Руководство» провели серию экспериментов, чтобы проверить, что будет со вкусом кофе при разных соотношениях общей и карбонатной жесткости воды.
Максимальная общая жесткость и минимальная карбонатная жесткость (точка А)
Кислотность в кофе получается очень приглушенной.
Максимальная карбонатная жесткость и минимальная общая жесткость (точка B)
Вкус плоский, едкий, пережаренный.
Минимальная общая жесткость и минимальная карбонатная жесткость (точка С)
Вкус пустой, слегка уксусный.
Максимальная карбонатная жесткость и максимальная общая жесткость (точка D)
Вкус горький, терпкий, пустой.
Итак, чтобы получить сбалансированный вкус, в кофе должны быть кальций, магний и небольшое содержание буфера.
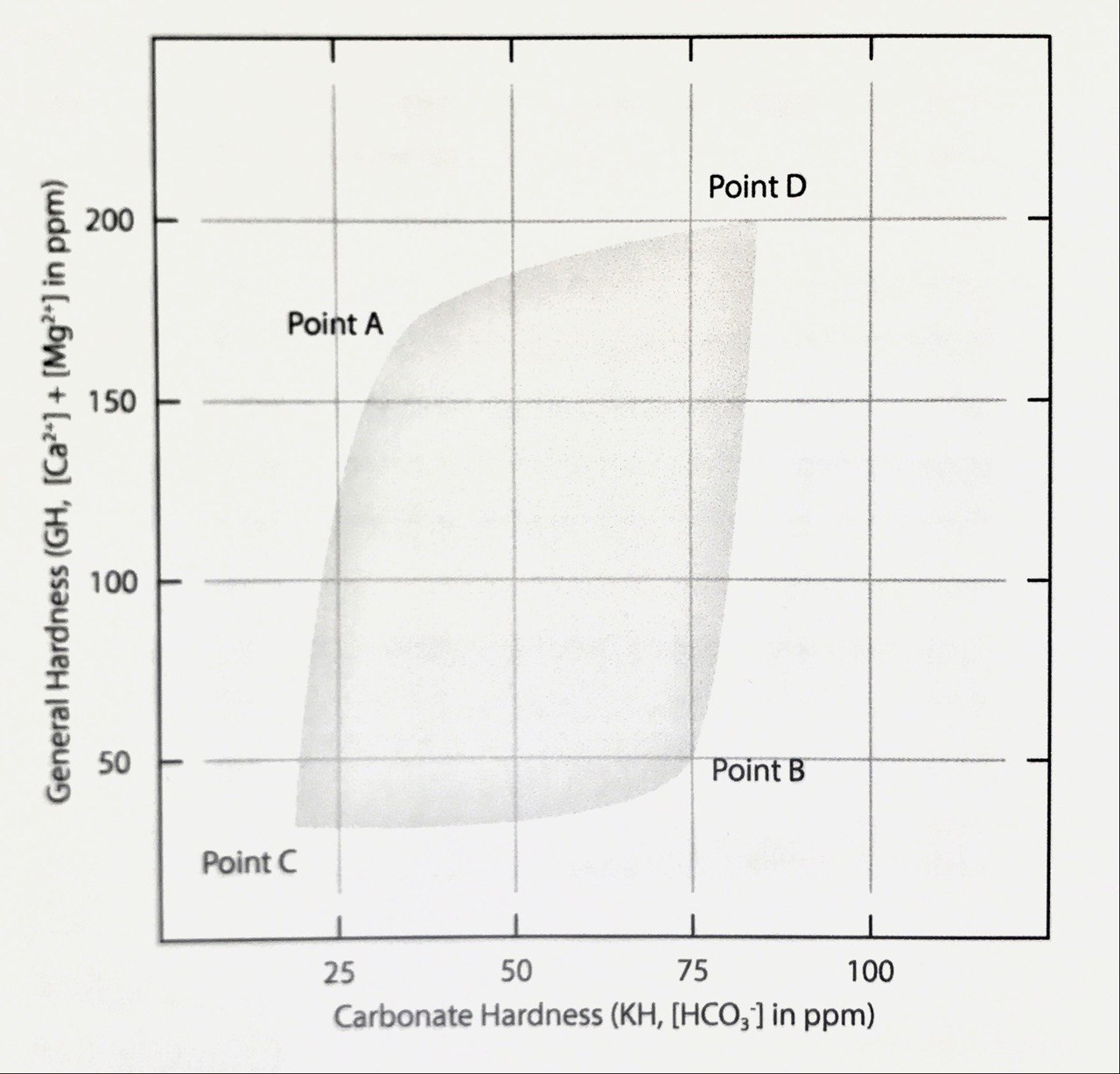
Исследуя карту воды, Максвелл Колонна-Дэшвуд и Кристофер Хэндон постарались найти границы для каждого параметра. Эти точки не являются конкретными значениями, но находятся в пределах погрешности около 10 ppm
Как показали эксперименты Максвелла Колонна-Дэшвуда и Кристофера Хэндона, для стабильного вкуса кофе в воде должно быть сохранено небольшое количество буфера. В качестве отправной точки вы можете использовать соотношение GH и KH 2:1.
Если баланс нарушен, проверьте состав воды и параметры водоподготовки. Для домашнего приготовления кофе выбирайте бутилированную воду с карбонатной жесткостью 50-70 мг/л при рН 7,0. Бариста могут менять параметры водоподготовки для кофемашины в сторону уменьшения или увеличения солей в воде.
Мы уже рассказывали о том, как выбрать воду для кофе, как контролировать качество воды, которая попадает в кофемашину и как измерить вкус кофе по специальным параметрам. Чтобы понять, как состав вашей воды влияет на готовый напиток, ориентируйтесь на вкус кофе. Экспериментируйте, пробуйте разную воду и меняйте параметры водоподготовки с учетом желаемого вкуса. Так вы сможете получить кофе с яркой приятной кислотности.
Что запомнить
В воде должно содержаться небольшое количество бикарбонатов — до 70 ppm. Они помогают держать pH воды под контролем, что положительно влияет на приятную кислотность кофе.
Правильно подбирайте воду для заваривания кофе. Обращайте внимание на показатель «гидрокарбонат» на этикетке, оптимальное значение — 50-70 мг/л при рН 7,0.
Важно не оценивать общую и карбонатную жесткость по отдельности. Их соотношение влияет на вкус кофе. Рекомендуемое соотношение GH и KH 2:1.
При высоком содержании карбоната киcлотность будет не цитрусово-ягодной, а плоской и землистой. При низком содержании карбоната вкус получается уксусным и кислым.
Вам может быть интересно:
Как быстро настроить вкусный эспрессо
10 апр 2019 · 6 мин. на чтение












.png)
