Кета питание диета что такое
С какой патологией призвана бороться кетодиета в неврологии?
Кетогенная диета эффективна при следующих состояниях: туберозный склероз, синдром Ретта, синдром Леннокса-Гасто, синдром дефицита переносчика глюкозы 1 типа (G1DS), генетические генерализованные эпилепсии и фокальные эпилепсии, резистентность к противосудорожным препаратам.
Опираясь на опыт экспертов 20 центров, использующих кетогенную диету в качестве терапии у более чем 2100 взрослых с эпилепсией в 10 странах, международная команда экспертов разработала рекомендации по применению кетодиеты у взрослых пациентов с лекарственно-устойчивой эпилепсией.
90% процентов медицинских центров используют модифицированную диету Аткинса, 84% используют классическую кетогенную диету и 63% используют модифицированную кетогенную диету и / или переход на продукты питания с низким гликемическим индексом.
Более половины центров (58%) используют масло триглицеридов со средней длиной цепи в сочетании с кетогеннной диетой для увеличения продукции кетоновых тел.
Наиболее важными факторами, влияющими на выбор кетодиеты, являются простота применения диеты для пациента (100%), предпочтения пациента и / или лица, осуществляющего уход за пациентом, домашние условия и режим питания (90% каждый фактор).
Исследователи рекомендуют предоставить взрослым пациентам идеи рецептов, индивидуальное обучение кетогенной диете у диетолога, а также рекомендации по планированию и приготовлению пищи перед началом диетотерапии.
В педиатрической практике пациенты с положительным терапевтическим ответом обычно остаются на кетогенной диете в течение 2 лет. У взрослых пациентов кетодиета не имеет ограничений по срокам назначения.
Противопоказания и предостережения в отношении кетодиеты одинаковы, как у детей, так и у взрослых пациентов.
Однако ряд общих состояний у взрослых, таких как гиперлипидемия, болезни сердца, сахарный диабет, низкая плотность костной ткани и беременность, требуют дополнительного внимания, осторожности и контроля при назначении кетодиеты.
Новые рекомендации содержат призыв к мониторингу кетонов (уровень βHB в крови или AA в моче) в первые месяцы кетодиеты в качестве объективного показателя соблюдения режима терапии и биохимического ответа.
Генетическое тестирование может быть рассмотрено у взрослых с когнитивными нарушениями и эпилепсией неизвестной этиологии.
Денситометрия должна проводиться каждые 5 лет.
При отсутствии подозрений на наличие нарушений основного обмена веществ биохимические исследования могут быть опущены.
Взрослым на фоне кетогенной диеты также следует рекомендовать принимать поливитаминные и минеральные добавки, а также пить больше жидкости.
Взрослым с лекарственно-устойчивой фокальной эпилепсией в первую очередь следует проводить хирургическое лечение.
Эксперты считают, что новые данные также подтверждают возможность использования кетодиеты при мигрени, болезни Паркинсона, деменции и рассеянном склерозе. На данный момент требуются дополнительные исследования, чтобы дать рекомендации по использованию кетодиеты при других неврологических патологиях.
Рекомендации были опубликованы 30 октября в интернет-журнале Neurology Clinical Practice.
Здоровое питание — рекомендации врача-эндокринолога
Структура статьи
Само словосочетание «здоровое питание» многими из нас воспринимается как непосильный груз ответственности. Часто кажется, что поменять пищевые привычки и придерживаться здорового питания – нетривиальный процесс.
Предлагаем рассмотреть базовые принципы и рекомендации. И начать, так скажем, с малого, постепенно эволюционируя…
Внимание! Все рекомендации даны без учета сопутствующих патологий наличия пищевой непереносимости или аллергии. В этих случаях Вы должны провести коррекцию, посоветовавшись с Вашим врачом.
Для чего нам нужна еда?
Итак, сначала надо понять, для чего нам нужна еда?
Еда является единственным источником энергии для нашего организма, а так же источником положительных эмоций. Кроме этого пища необходима для «строительства» новых клеток, поддержания жизнедеятельности организма в целом, нормальной работы органов и систем. Неправильное, несбалансированное питание может привести к развитию многих заболеваний, ухудшению внешнего вида, снижению настроения. Поэтому любые рекомендации по лечению разных заболеваний должны начинаться с коррекции питания.
Простые правила планирования питания
Чтобы пища поддерживала наше здоровье на хорошем уровне, необходимо соблюдать простые правила планирования здорового питания:
Из чего же состоит пища?
Всем известно со школьной скамьи, что пища состоит из углеводов, белков и жиров, так называемых питательных веществ, а так же содержит микроэлементы и витамины, которые не имеют питательной ценности, но поддерживают биохимические процессы.
Углеводы
Основными поставщиками энергии в организм и повышающими уровень сахара в крови являются углеводы. Это значит, что в результате химических превращений в организме углеводы расщепляются на молекулы воды, СО2 и АТФ (носители энергии) и этот процесс не требует больших энергетических затрат. Синтезированная энергия должна быть израсходована при мышечной работе. Если этого не происходит, то нереализованная энергия аккумулируется в жировом депо в виде триглицеридов. В случае отсутствия углеводов организм начинает «добывать» энергию из жиров и белков. В результате этих процессов вырабатываются побочные (токсические, например, кетоновые тела) продукты и тратится большое количество собственной энергии и ферментов, что приводит к напряжению пищеварительной системы, печени и почек. Поэтому питание, не содержащее углеводы не является здоровым.
Для поддержания энергетического баланса человеку необходимо потреблять около 300 гр углеводов в сутки или 50% от общей калорийности (1гр углеводов дает 4 ккал энергии).
По скорости расщепления в кишечнике, а так же по скорости повышения глюкозы в крови углеводы делятся на простые («быстрые»), сложные («медленные») и клетчатку. Простые углеводы дают энергию в течение 10-15 минут. Источниками простых углеводов (глюкоза, галактоза, сахароза, лактоза, мальтоза) являются продукты, содержащие рафинированный сахар, а так же сладкие фрукты, мед, молоко, пиво. Энергия, полученная в результате усваивания простых углеводов накапливается быстро и требует быстрой утилизации. Сложные углеводы расщепляются до простых в течение 30-60 мин. Источниками являются злаковые (крупы, мука), картофель. При длительной кулинарной обработке или механическом размельчении сложные углеводы перевариваются быстрее и по скорости повышения сахара приближаются к простым углеводам. Энергия, полученная в результате расщепления сложных углеводов, накапливается постепенно и дает длительную энергетическую поддержку организму. Клетчатка или пищевые волокна — незаменимый компонент пищи. Несмотря на то, что она не несет питательной ценности, она имеет ряд отличных функций для поддержания процессов пищеварения: регулирует скорость всасывания углеводов и жиров, стимулирует моторику кишечника, очищает кишечник от не переваренных продуктов. Суточная потребность в клетчатке 20-60 гр.
Белки
Белки — основной строительный материал в любом живом организме. Кроме этого белки несут еще 8 различных функций, благодаря которым происходит транспорт полезных веществ по крови, сохраняется водный баланс в клетках и межклеточном пространстве, осуществляется работа иммунный системы и др. В отсутствии углеводов белки берут на себя функцию поддержания энергетического обмена. Белки состоят из аминокислот, которые в свою очередь подразделяются на заменимые (могут образовываться в организме из различных веществ) и незаменимые (не образуются в организме, а поступают только с пищей). Источником незаменимых аминокислот являются животный белок, белок рыбы, молока, а так же частично белки бобовых, особенно сои. Поэтому продукты, содержащие бобовые могут явиться альтернативой при ограничении потребления мяса, непереносимости молочного белка. Также поставщиком белка являются злаковые.
Суточная потребность в белке около 0,8 гр на килограмм веса в сутки или 25% от общей калорийности ( 1 гр белка дает 4 ккал энергии). Белки животного происхождения должны составлять 20% от общего количества белка.
Жиры — основное депо энергии. Кроме этой функции жиры защищают внутренние органы от механического повреждения, от охлаждения или перегревания, способствуют всасыванию витаминов А,Д,Е,К. У жиров есть еще одна важная функция. Они являются основным материалом для синтеза стероидных гормонов и фосфолипидов — основного компонента клеточной стенки. К стероидным гормонам относят половые гормоны. При дефиците жиров в питании развивается их дефицит, что приводит к нарушению половой функции и бесплодию. При нарушении баланса потребляемых жиров появляется риск развития атеросклероза. Помните, что жиры не повышают сахар в крови.
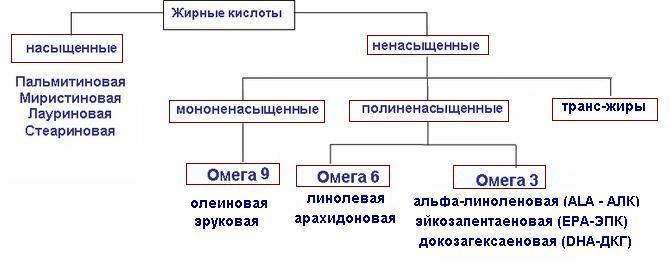
Жиры состоят из жирных кислот (ЖК), которые в свою очередь делятся на насыщенные и ненасыщенные. Вот так выглядит классификация жирных кислот:
Насыщенные ЖК имеют животное происхождение и в результате их метаболизма в организме образуется «вредный» холестерин, повышение которого приводит к атеросклерозу. Таким же негативным влиянием на организм обладают транс-жиры (ТЖ). ТЖ образуются при нагревании до высокой температуры любых жирных кислот.
Источником ненасыщенных ЖК являются растения и рыбий жир. Ненасыщенные жиры препятствуют развитию атеросклероза и являются составляющей «хорошего» холестерина. Особое значение имеет соотношение в рационе Омега ЖК. Наиболее полезными являются Омега 3 ЖК — они снижают холестерин, придают эластичность кровеносным сосудам, предупреждают образование тромбов, оказывают антиоксидантный эффект, улучшают состояние связок, обладают противовоспалительным действием. Поэтому в рационе человека оптимальное соотношение Омега 3 и 6 ЖК должно приближаться 1:4.
Содержание ЖК в продуктах
| Насыщенные жиры | Ненасыщенные жиры | ||
|---|---|---|---|
| Мононенасыщенные | Полиненасыщенные жиры | ||
| Омега-9 | Омега-3 | Омега-6 | |
| Сливочное масло и молочные жиры | Оливковое масло | Рыба и рыбий жир | Подсолнечное масло |
| Мясо, сало, животные жиры | Арахисовое масло | Льняное масло | Кукурузное масло |
| Пальмовое масло | Авокадо | Рапсовое масло | Орехи и семечки |
| Кокосовое масло | Маслины | Масло грецкого ореха | Хлопковое масло |
| Масло какао | Мясо птицы | Масло зародышей пшеницы | Соевое масло |
О Холестерине
Холестерин в организме синтезируется из насыщенных жирных кислот и уксусной кислоты (продукта распада углеводов). Это так называемый эндогенный холестерин. Часть холестерина поступает в организм экзогенным путем с продуктами животного происхождения (экзогенный холестерин). Холестерин играет важную роль в организме. Он является провитамином D3, служит исходным веществом для образования половых гормонов, гормонов надпочечников, участвует в образовании желчных кислот. Пожилым людям и лицам, предрасположенным к атеросклерозу, рекомендуется ограничить потребление продуктов с высоким содержанием холестерина, не исключая их полностью из рациона.
Суточная потребность в жирах составляет 25% от общей калорийности (при сжигании 1 гр жира выделяется 9 ккал энергии), причем животный жир должен составлять не более 10% от общего калоража. Количество потребляемого холестерина не должно превышать 300 мг/сут.
Витамины и микроэлементы
Нельзя забывать также о витаминах и микроэлементах, источником которых являются продукты как животного, так и растительного происхождения. Витамины играют важную роль в биохимических процессах. Они являются кофакторами для ферментов, то есть активаторами химических реакций. При дефиците витаминов нарушаются функции органов и систем. Витамины, содержащиеся в продуктах растительного происхождения, очень чувствительны к термической обработке, поэтому важно употреблять эти продукты в сыром виде. В организм витамины поступают двумя путями: экзогенный (с пищей) и эндогенный (синтезируются в кишечнике). Большинство поступает только с пищей. Важен и тот факт, что некоторые из них имеют очень короткий срок пребывания в организме, быстро разрушаются, поэтому их необходимо потреблять ежедневно.
Минимальная суточная норма потребления витаминов около 0,15 г. Потребность человека в отдельных витаминах обусловлена рядом факторов: возрастом, состоянием здоровья, характером деятельности, временем года, полноценностью питания, соответственно величина среднесуточной потребности варьируется.
В биохимических процессах человеческого организма задействованы 22 химических элемента (микроэлементы). Наиболее важными являются: кальций, фосфор, магний, натрий, калий, селен, цинк, медь, йод, хром, железо, кремний. Источниками этих микроэлементов являются продукты растительного и животного происхождения. При их дефиците в пище развиваются различные патологические состояния. И наоборот, на фоне какого-либо заболевания возникает дефицит микроэлементов из-за повышенного их расхода. В этих случаях необходимо увеличить их поступление. Подробнее о роли микроэлементов в организме человека мы поговорим отдельно. Важно помнить, что для здоровья организма необходим баланс поступающих с пищей как витаминов, так и микроэлементов.
Как рассчитать суточную потребность в питательных веществах?
Существуют два подхода к расчету потребляемых полезных веществ: среднепопуляционный и индивидуальный. Многие рекомендуемые меню в основе своей имеют первый подход, то есть не учитывают индивидуальные затраты энергии, наличие заболеваний, особенности региона проживания и др. Индивидуальный или персональный расчет как раз учитывает особенности пациента и осуществляется врачом-специалистом.
Шаг 1. При обоих подходах в первую очередь рассчитываются нормы потребления белков, жиров и углеводов с учетом необходимого суточного калоража рациона по формуле:
Суточный калораж (СК) для женщин (примерный расчет основного обмена):
Если Вы ведете малоподвижный образ жизни, тогда умножьте полученную величину на 1.1, при умеренной физической нагрузке — на 1.3, при тяжелой работе — на 1.5. Однако, если Вы можете посчитать затраты энергии на работу в течение суток, используя специальные таблицы, то просто прибавьте полученное число к результатам расчета по формуле.
Так же индивидуальный основной обмен можно определить, пройдя исследование состава тела (Анализ состава тела с помощью биоимпедансного метода) и тогда формула расчета Вам не понадобится.
Если перед вами стоит задача по снижению веса, то суточный калораж надо снизит на 20%.
p>Шаг 2. После того, как Вы рассчитали суточный калораж, переходим к расчету суточных норм потребления белков, жиров и углеводов.
Для нормального функционирования человеку необходимо потреблять в сутки белков и жиров по 25% от общего калоража и 50% углеводов. Зная, что 1 г белков и углеводов в процессе расщепления дают по 4 ккал энергии, а 1 г жиров — 9 ккал, то формула расчета суточной потребности питательных веществ будет выглядеть так:
Шаг 3. Последним шагом в формировании Вашего меню будет распределение калорийности в течение суток.
Рекомендованы следующие подходы:
| Прием пищи | Шестиразовое питание | Пятиразовое питание | Трехразовое питание |
|---|---|---|---|
| завтрак | 20-25% | 20-25% | 20-25% |
| 2-й завтрак | 10-15% | — | — |
| обед | 25-30% | 40-45% | 35% |
| полдник | 10-15% | — | — |
| ужин | 20% | 20-25% | 25% |
| 2-й ужин | 5-10% | 5-10% | — |
Вопросы организации питания
В этой статье описаны самые общие правила, касающиеся здоровых людей. Если Вы имеете какую-либо проблему со здоровьем, то с врачом-специалистом необходимо обсудить индивидуальный рацион. В клинике ЦЭЛТ такую профессиональную помощь можно получить на консультации врача-эндокринолога. Мы всегда готовы помочь!
Кетогенная диета в лечении фармакорезистентных эпилепсий
Проблема поиска эффективных методов лечения эпилепсии сохраняет свою актуальность, так как, несмотря на появление нового поколения противосудорожных средств, в 10–20% случаев отмечается резистентное течение заболевания. При отсутствии эффекта
Проблема поиска эффективных методов лечения эпилепсии сохраняет свою актуальность, так как, несмотря на появление нового поколения противосудорожных средств, в 10–20% случаев отмечается резистентное течение заболевания. При отсутствии эффекта от применения соответствующего виду припадка препарата и развитии выраженных побочных эффектов возникает необходимость отмены лекарственной терапии, что, соответственно, требует применения альтернативных методов лечения [7].
Можно утверждать, что диетотерапия является первым эффективным методом лечения эпилепсии, известным человечеству в течение многих веков. Голодание при лечении эпилепсии применялось с библейских времен, а также эпизодически практиковалось в Средние века. Но первое научное сообщение на эту тему датируется 1921 г., когда на заседании Американской ассоциации врачей известный педиатр R. Geylin сообщил об успешном опыте лечения голодом больных эпилепсией [6]. В ходе исследования продолжительность голодной паузы составила 21 день, и у некоторых пациентов удалось достичь 100-процентного успеха. При исследовании механизма действия голода R. Wilder в 1921 г. предположил, что терапевтический эффект обусловлен устанавливающимся в организме состоянием кетоза. Автор предложил собственную диету с высоким содержанием жиров и резким ограничением белков и углеводов, обеспечивающую развитие биохимических изменений в организме, соответствующих таковым при голодании, с целью поддержания высокого уровня кетоза в течение длительного времени. В 1924 г. R. Wilder разработал кетогенную диету (КД), и этот метод лечения с успехом применялся в 1930–1940-х гг., в связи с отсутствием на тот момент эффективных противосудорожных препаратов (применялся фенобарбитал и бромиды). В конце 30-х гг. прошлого столетия начался этап бурного развития фармакологического направления в лечении эпилепсии, и интерес к кетогенной диете упал.
Второй всплеск популярности кетогенной диеты относится к началу 1990-х гг., что связано с деятельностью известного американского кинопродюсера Д. Абрахамса, двухлетний сын которого страдал эпилепсией. «Тысячи припадков, несчетное количество препаратов, 5 детских неврологов и 2 гомеопата, одно безуспешное хирургическое вмешательство — все было зря» [6]. Однако благодаря применению кетогенной диеты припадки прекратились в течение первых дней лечения.
Д. Абрахамс приложил много усилий для популяризации кетогенной диеты: история его сына была рассказана по телевидению, в печати, был создан фильм на основе реальных событий с участием известных киноактеров. Организация фонда Чарли обеспечила финансовую поддержку дальнейших исследований по применению кетогенной диеты.
Как и любое модное направление, метод кетогенной диеты завоевал множество горячих поклонников. Но были и скептики. К первым можно отнести Whelless (1995), утверждавшего, что по эффективности кетогенная диета превосходит любой антиконвульсант, созданный за последние 50 лет [6]. Гораздо большее число противников диеты обсуждали трудности, связанные с соблюдением режима, и жесткие ограничения. И только проведенное в 1998 г. первое мультицентровое исследование позволило объективно судить об эффективности этого метода. Было доказано, что при применении кетогенной диеты у 60–75% пациентов с фармакорезистентными припадками отмечается положительный эффект в виде снижения частоты приступов более чем на 50% [5, 10].
Известно, что формула физиологической нормы питания составляет 1:1:4, где на 1 часть белков и 1 часть жиров приходится 4 части углеводов, и источником энергии служат углеводы. При голодании организм расходует запасы углеводов, а в случае полного их истощения в качестве источника энергии начинает использовать жиры, которые расщепляются до β-гидроксибутирата и ацетоацетата, что приводит к кетонемии. Именно кетоны обеспечивают антиконвульсантный эффект. Голодание как способ контроля над припадками имеет существенный недостаток, так как при истощении запасов жиров начинается распад белков, что может привести к фатальному исходу. Кетогенная диета обеспечивает развитие биохимических изменений в организме, сходных с таковыми при голодании, но, что особенно важно, поддерживает этот тип энергетического метаболизма в течение длительного времени без значимых нарушений белкового обмена.
Кетогенная диета — это индивидуально рассчитанная и жестко контролируемая диета с высоким содержанием жиров и ограничением белков и углеводов в соотношении 4:1 (жиры: белки + углеводы) (Freeman et al., 2000). Для усиления эффекта диета может быть оптимизирована под наблюдением опытного диетолога, поскольку даже самые незначительные ошибки, такие, как больший объем калорий в диете, больший объем жидкости или применение медикаментозных препаратов, содержащих углеводы, могут нарушить диету и тем самым спровоцировать возобновление припадков.
Нам не встретилось данных о применении КД в лечении фармакорезистентных форм эпилепсии в отечественной литературе. В связи с этим впервые в России в 2002-2003 гг. было проведено собственное исследование в рамках договора о сотрудничестве между ГУ НИИ питания РАМН и Научно-практическим центром медицинской помощи детям с пороками развития черепно-лицевой области и врожденными заболеваниями нервной системы на базе отделения психоневрологии.
Протокол проведения КД состоял из нескольких этапов.
При хорошей переносимости диеты и стабильности соматических и неврологических показателей ребенок выписывался из стационара с инструкцией по соблюдению КД в домашних условиях.
Катамнестическое наблюдение проводилось через месяц от начала диеты, а далее ежеквартально в течение первого года (при необходимости чаще) и включало в себя осмотр педиатра-диетолога, невролога, анализ динамики частоты и характера припадков, проведение клинико-лабораторных и инструментальных обследований, предусмотренных протоколом.
В процессе наблюдения осуществлялась коррекция диеты в соответствии с изменением массы тела пациента, степенью кетоза или переносимостью отдельных приемов пищи.
В нашем исследовании приняли участие 10 мальчиков в возрасте от 1,5 до 18 лет (средний возраст 9,5 лет), у всех пациентов отмечалось фармакорезистентное течение эпилепсии с минимальным количеством припадков до 2 в неделю. Все пациенты большую часть своей жизни страдали эпилептическими приступами: средняя продолжительность жизни с припадками у детей младшей возрастной группы (моложе 15 лет) составила 82%, у пациентов старшей возрастной группы (15–18 лет) — 77%.
У пациентов отмечались следующие клинические варианты эпилептических приступов: атипичные абсансы, изолированные миоклонические абсансы и статусы миоклонических абсансов, тонические, тонико-клонические припадки, изолированные и серийные аксиальные спазмы, фокальные моторные припадки со вторичной генерализацией и без нее. У всех пациентов наблюдалось сочетание 2 и более типов припадков.
В нашем исследовании у 5 (50%) из 10 пациентов через год применения кетогенной диеты отмечался положительный эффект (снижение частоты припадков на 50% и более), у 2 детей зарегистрировано полное прекращение припадков.
Данные последних неконтролируемых ретроспективных исследований достаточно разноречивы [3, 4, 6, 9]. По результатам исследований E. Vining et al. (1998), положительный эффект отмечался в 38% случаев, из них полное прекращение припадков — в 9,8% случаев. J. Freeman et al. (1998) сообщали о снижении частоты припадков на 50% и более по крайней мере у 50% пациентов, в том числе о полном прекращении припадков у 7% пациентов. D. Nordli et al. (1997) считают, что положительный результат может быть достигнут у одной-двух третей пациентов, начинающих применение диеты.
В литературе доминирует мнение, что для КД характерна возраст-зависимая эффективность, т. е. наиболее благоприятные результаты отмечаются у детей младшего возраста (G. Coppola et al., 2002; E. Kossoff et al., 2002), что объясняется более быстрым развитием кетоза и более стабильным его состоянием у младших детей. Согласно другим исследованиям (T. Swink et al., 1997; M. Freeman et al., 1998), диета была одинаково эффективна и хорошо переносилась во всех возрастных группах пациентов. В нашем исследовании у 2 детей (3 года и 6 лет) припадки в течение года не возобновились, еще у 2 детей (4 года и 18 лет) частота припадков снизилась более чем на 50%, что позволяет говорить о более высокой эффективности кетогенной диеты у пациентов младшего возраста.
Представляем собственное наблюдение
Пациент Н., 6 лет, вес — 23 кг, рост — 119 см. Д/З: криптогенная парциальная (лобнодолевая) эпилепсия с фокальными припадками с нарушением сознания. Поступил 29 марта 2002 г. для проведения курса диетотерапии.
Жалобы при поступлении на припадки, возникающие через 0,5-1 ч после засыпания или за 1-2 ч до пробуждения.
В начале приступа открывает глаза, глазные яблоки заведены вверх и вправо, отмечается медленное поднимание рук вверх и их тоническое напряжение с мелкими симметричными подергиваниями в мышцах кистей, тоническим напряжением в ногах, клониями в нижнелицевой мускулатуре справа (рот приоткрыт, слюнотечение не отмечается), ритмичными клоническими морганиями, учащенным шумным дыханием.
В финале приступа эпизодически наблюдается мочеиспускание. Продолжительность приступов — 1-2 мин, частота — 1–2 раза за ночь.
Жалобы на нарушение поведения, двигательную гиперактивность, гетероагрессию, аффективные реакции, задержку речевого развития — говорит отдельные слоги, лепечет слова (до 10 слов).
Ребенок от первой беременности, протекавшей с угрозой прерывания в течение всего срока беременности (матка в тонусе). Роды стремительные. Вес при рождении — 3200 г. Раннее развитие без отставания. Ходит с 1 г. 1 мес, лепечет слова с 1 г, с тех пор существенного развития речи не отмечается. С 7-месячного возраста отмечаются приступы с утратой сознания, общей атонией, на фоне гипертермии, продолжительностью до 40 мин. Всего около 6 фебрильных эпизодов, по поводу которых с 9 мес получал бензонал 100 мг/сут и клоназепам 1,5 мг/сут без эффекта. Впервые в возрасте 2 лет 8 мес появились приступы без фебрильной провокации в виде «замираний» с заведением глазных яблок вверх с сохранной реактивностью (реагировал на оклик) в течение 10 мин; если приступ продолжался более 10 мин, то отмечались постепенная утрата сознания и появление моторных симптомов (клоний в руках). Применение бензонала и суксилепа, дифенина, депакина хроно, финлепсина было неэффективно. С 3 лет на фоне суксилепа приступы «замираний» стали короче, но частота увеличилась до 25 раз в сутки. Кроме того, появились генерализованные припадки астатического и тонико-клонического характера, в ряде случаев с адверсивным компонентом и развитием постприступного пареза в правых конечностях. При обследовании в ПНО НПЦ в апреле 2001 г. клинико-ЭЭГ-данные свидетельствовали о наличии у пациента криптогенной парциальной (лобнодолевой) эпилепсии с абсансами и вторично генерализованными припадками. При проведении видео-ЭЭГ- мониторинга были зарегистрированы гипомоторные припадки с остановкой взгляда, произвольной деятельности, сопровождаемые появлением в ЭЭГ разрядов генерализованной эпилептиформной активности по типу «атипичного» абсанса с началом и амплитудным преобладанием в левой лобной области.
При поступлении в апреле 2001 г. получал суксилеп, бензонал, клоназепам и карбамазепин. В отделении при замене карбамазепина на вальпроевую кислоту существенного эффекта не отмечалось; был введен ламиктал в дозе 15 мг/кг/сут. При отмене бензонала учащались гипомоторные приступы, при снижении дозы клоназепама возобновлялись генерализованные тонико-клонические припадки. С декабря 2001 г. на фоне снижения дозы ламиктала появились фокальные приступы вышеуказанного характера во время сна.
Объективно на апрель 2002 г. в соматическом статусе — признаки мезенхимальной недостаточности, гиперподвижность суставов в рамках синдрома Элерса-Данлоса; в неврологическом статусе — тотальная мышечная гипотония, арефлексия, единичные диффузные миоклонии, положительный симптом Хвостека с обеих сторон.
МРТ головного мозга: признаков очаговых изменений в веществе головного мозга не выявлено, незначительная вентрикуломегалия.
ЭхоКГ: признаки пролапса митрального клапана I степени.
ЭКГ: синусовая дыхательная аритмия (65–100), нарушение проводимости в правой ножке пучка Гиса. Возможна небольшая гипертрофия миокарда левого желудочка.
УЗИ органов брюшной полости: признаки холестаза, метаболических изменений почек.
ЭЭГ: умеренные диффузные изменения с вспышками β-активности в передних отделах и вспышками диффузной, с высокой степенью билатеральной синхронизации δ-активности с включением комплексов острая/медленная волна в левой лобно-височной области.
Заключение генетика: синдром Элерса-Данлоса II типа (с пролапсом митрального клапана).
Заключение психолога: IQ = 74, моторные функции, игровая деятельность, навыки самообслуживания — 8, сфера общения, эмоционально-волевая деятельность и предметно-конструктивный праксис — 7, речевая деятельность — 7,5.
Заключение логопеда: нарушения артикуляционной моторики, нарушения фонематического слуха, фразовая речь отсутствует.
Биохимия крови: белок — 75 г/л, триглицериды — 0,6 ммоль/л, АЛТ/АСТ — 23,3/42,4 U/l, амилаза — 112,8 U/l.
При поступлении пациент получал клоназепам — 3 мг/сут, ламиктал — 150 мг/сут, бензонал — 250 мг/сут (75х75х100), суксилеп — 375 мг/сут. Концентрация антиконвульсантов в крови иммуноферментным методом (аппарат TDX/FLX): фенобарбитала — 18,1; 34,6 (норма 10–40 мг/мл), суксилепа — 67,1; 70,7 (норма 50–100 мг/мл).
Первые сутки диеты: голодная пауза — с 18.00 9.04.2002: утром, 6.45 — припадок во время сна. Повышение кетоза до 10 ммоль/л к 22.00, глюкоза — 4,6– 3,6 ммоль/л.
Вторые сутки диеты: кетоз — 12–14 ммоль/л, к утру подъем температуры до субфебрильных цифр, общая вялость, падение уровня глюкозы в течение дня до 2,8-2,2 ммоль/л, в связи с чем было начато введение коктейля на полдник и ужин в дозе 1/3 от суточной калорийной потребности (45х45 мл). Припадки не отмечались. Нарастание концентрации фенобарбитала до 36,0; 38,3 мг/мл, суксилепа — 80,7; 86,1 мг/мл.
Третьи-четвертые сутки диеты (питание кетогенным коктейлем): припадков нет, уровень кетоза стабильный — 12–16 ммоль/л, уровень глюкозы — 2,1 ммоль/л утром, вечером 3,2, сохраняется субфебриллитет без явных катаральных проявлений, вялость, сонливость, динамическая атаксия, получает коктейль (45х45х90х90), ест с аппетитом.
Пятые сутки (рацион диеты вводится с обеденного приема пищи): сохраняются сонливость, вялость, вероятно, обусловленные барбитуровой интоксикацией. Нарастание концентрации фенобарбитала при суточной дозе бензонала 225 мг — до 44,8; 45,7 мг/мл; при суточной дозе суксилепа 375 мг — до 81,6; 93,2 мг/мл на фоне высокого кетоза. Доза бензонала снижена до 210 мг/сут. Уровень глюкозы — 3,8-4,0 ммоль/л, уровень кетоза — 10–16 ммоль/л. Биохимия крови: снижение белка крови — 64,8 г/л, снижение холестерина — с 4,8 до 2,7 ммоль/л, нарастание триглицеридов с 0,6 до 2,2 ммоль/л, нарастание АЛТ/АСТ — 58,3/71,4 U/L, снижение амилазы — с 112,8 до 73,0 U/L. ЭКГ: нарастание ЧСС — 100–111, признаки нарушения кровоснабжения миокарда задней стенки левого желудочка (возможно гипертрофированного). В неврологическом статусе: выраженная локомоторная атаксия, вялость, снижение двигательной активности.
Шестые сутки диеты: аппетит повышен, съедает предложенные блюда полностью. Сохраняется субфебриллитет без явных катаральных явлений. Отмечаются общая слабость, общий гипергидроз, динамическая атаксия.
Седьмые сутки диеты: стал более активным, сонливости не отмечается. Показатели глюкозы соответствуют возрастным нормативам.
Восьмые сутки диеты, 17.04.2002: показатели глюкозы и кетонов стабильные (12–16). Самочувствие хорошее, активен.
9–13-е сутки диеты: уровень кетоза стабильный — 12–16 ммоль/л, уменьшилась динамическая атаксия.
13-е сутки диеты: уровень кетоза — 12–14 ммоль/л, самочувствие хорошее, состояние стабильное.
Выписан домой. Припадков нет. Биохимические показатели крови на 14-е сутки диеты: белок — 58,1 г/л, снижение мочевины — до 2,0 с 6,3 ммоль/л, нарастание АЛТ/АСТ — 74,7; 76,5 U/L, амилаза — 106 U/L. Концентрация в крови фенобарбитала — 41,9; 42,0 мг/мл; суксилепа — 72,2; 78,1 мг/мл.
ЭЭГ в динамике: положительная динамика в виде снижения доли медленной активности, индекса спайковой активности. Эпилептиформная активность имеет диффузный характер.
Сохраняется противосудорожная терапия: бензонал — 200 мг/сут (суточная доза снижена на 50 мг/сут), клоназепам — 3 мг/сут, суксилеп — 375 мг/сут, ламиктал — 150 мг/сут.
В течение первого месяца диеты на фоне ОРВИ однократно генерализованный тонико-клонический припадок на фоне гипертермии до 39°.
Контрольное ультразвуковое исследование органов брюшной полости через 1 мес: без отрицательной динамики. Биохимия крови: общий белок — 73,5 г/л, нормализация уровня трансаминаз — до 12,1/39,2 U/L. Нарастание в крови концентрации суксилепа — 375 мг/сут: 88,6; 102,2 мг/мл; фенобарбитала при дозе бензонала 200 мг/сут — 35,5; 38, 9 мг/мл.
Второй месяц диеты, май 2002 г.: уровень кетоза эпизодически снижается спонтанно до 4-5 ммоль/л, затем вновь повышается до терапевтического диапазона. Со второго месяца диеты отмечаются нарушения сна (не может заснуть до 2-3 ч ночи), бурные аффективные реакции в виде вспышек гетероагрессии, немотивированного возбуждения, плача, фиксации на желаемом, истерические реакции, усилился логоневроз (применяет произвольные приемы для начала речи — трогает себя за нос, выгибает туловище), слащавость, назойливость, периодически чувство голода.
Четвертый месяц диеты, июль 2002 г.: припадки не отмечаются. Сохраняются нарушения сна и поведения, периодически жалобы на голод, прекратившиеся при стабилизации уровня кетоза (путем оптимизации диеты) и при расширении питьевого режима.
Пятый месяц диеты, август 2002 г.: вес — 21,5 кг (-1,5 кг), рост 120 (+1 см); снижение дозы бензонала до 150 мг/сут.
Шестой месяц диеты, сентябрь 2002 г.: припадки не отмечаются, сон нормализовался.
Седьмой месяц диеты, октябрь 2002 г.: припадков нет, уровень кетоза стабильный. Сохраняются поведенческие нарушения — гетероагрессия, конверсионные реакции, сон нормализовался, на еду не обращает внимания. В интеллектуальном развитии прекратился логоневроз, научился считать до 5, знает цифры (увлеченно часами может рассматривать циферблат и проговаривать числа), расширился речевой запас, стал повторять за мамой стихи, сохраняются нарушения внимания (концентрации внимания, трудности сосредоточения, быстрое переключение, быстрая отвлекаемость, трудности усвоения инструкций), отсутствие произвольного контроля поведения.
Противосудорожная терапия: бензонал — 150 мг/сут (доза снижена почти вполовину по сравнению с исходной, концентрация фенобарбитала в крови — 23,9; 26,9 мг/мл), суксилеп — 375 мг/сут (уровень концентрации 83,5; 84,7 мг/мл), клоназепам — 3 мг/сут, ламиктал — 150 мг/сут. Показатели крови соответствуют возрастным нормативам.
Восьмой месяц диеты, ноябрь 2002 г.: состояние стабильное, припадков нет.
Девятый месяц диеты, декабрь 2002 г.: вес — 20 кг (-3 кг), рост — 121 (+0) см; состояние стабильное, припадков нет; сохраняются эмоциональные нарушения и нарушения поведения (аффективные реакции, аутоагрессия, нарушения внимания, слезливость, трудности социальной адаптации, фиксация на предметах (цифрах, машинах)).
Заключение психолога: сфера общения и моторные функции — 8, эмоционально-волевая деятельность и речевая сфера — 7, конструктивный праксис, игровая деятельность и навыки самообслуживания — 7,5, предметная деятельность — 5.
Через 1,5 года (ноябрь 2003 г.): вес — 23 кг (+0 кг). Припадки не возобновились. Считает до 50, сохраняется легкий логоневроз, различает цвета. Объективно: сухожильная гиперрефлексия с обеих сторон, эмоциональные нарушения в виде агрессии (направленная вербальная: «я убью тебя, плачь»), фиксация на темах, предметах, речевые эмболы, знает стихи. Доза бензонала снижена в 2 раза, клоназепама — вполовину, отменены ламиктал и суксилеп. ЭЭГ: на фоне умеренных диффузных изменений выявляется устойчивый фокус эпилептиформной активности в лобно-центральной области слева.
Особенности при введении диеты: полное прекращение припадков, наличие субфебриллитета при введении диеты в течение 8 дней без явных катаральных признаков, вероятно, метаболического характера (кетоз, метаболический ацидоз, вегетативные нарушения — общий гипергидроз), развитие барбитуровой интоксикации на фоне диеты (снижение дозы барбитурата на 1/3 в течение первого месяца и наполовину за 6 мес), нарастание уровня трансаминаз в течение первых 14 дней и нормализация через месяц, переносимость диеты хорошая, инсомнии (трудности засыпания до 2-3 ч ночи). Кетоз стабилизировался при расширении питьевого режима. Нарушения поведения в виде бурных аффективных реакций, нарушения сна, фиксированность на идеях, предметах (машинах, цифрах), элементы аутизма, трудности социальной адаптации.
Можно заключить, что в нашем исследовании кетогенная диета была эффективной и при парциальной, и при генерализованной эпилепсии. У 50% пациентов отмечался положительный эффект применения кетогенной диеты (снижение частоты припадков более 50%).
Таким образом, кетогенная диета является альтернативным немедикаментозным методом лечения эпилепсии, эффективность которого наиболее высока у детей младшего возраста. КД представляет реальную перспективу в лечении фармакорезистентных эпилепсий, при которых хирургическое лечение не может быть осуществлено. Исследование динамики поведенческих и эмоциональных нарушений при диетотерапии требует дальнейших исследований.
По вопросам литературы обращайтесь в редакцию.
Е. Л. Усачева, кандидат медицинских наук
С. О. Айвазян, кандидат медицинских наук
Т. Н. Сорвачева, доктор медицинских наук
Е. А. Пырьева, кандидат медицинских наук
И. Я. Конь, академик РАЕН, доктор медицинских наук, профессор
А. Г. Притыко, академик РАЕН, доктор медицинских наук, профессор
М. Ю. Шорина, К. В. Осипова
НЦ медицинской помощи детям с пороками развития черепно-лицевой области и врожденными заболеваниями нервной системы, НИИ питания РАМН, Москва