Кислотные свойства у фенола выражены сильнее чем
Фенолы
Гидроксисоединения – это органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Гидроксисоединения делят на спирты и фенолы.
| Спирты – это гидроксисоединения, в которых группа ОН соединена с алифатическим углеводородным радикалом R-OH. Если гидроксогруппа ОН соединена с бензольным кольцом, то вещество относится к фенолам. |
Общая формула предельных нециклических спиртов: CnH2n+2Om, где m ≤ n.
Классификация фенолов
По числу гидроксильных групп:
| Соединения, в которых группа ОН отделена от бензольного кольца углеродными атомами – это не фенолы, а ароматические спирты: |
Строение фенолов
В фенолах одна из неподеленных электронных пар кислорода участвует в сопряжении с π–системой бензольного кольца, это является главной причиной отличия свойств фенола от спиртов.
Химические свойства фенолов
Сходство: как фенол, так и спирты реагируют с щелочными металлами с выделением водорода.
Отличия:
1. Кислотные свойства фенолов
| Фенолы являются более сильными кислотами, чем спирты и вода, т. к. за счет участия неподеленной электронной пары кислорода в сопряжении с π-электронной системой бензольного кольца полярность связи О–Н увеличивается. |
Раствор фенола в воде называют «карболовой кислотой», он является слабым электролитом.
1.1. Взаимодействие с раствором щелочей
В отличие от спиртов, фенолы реагируют с гидроксидами щелочных и щелочноземельных металлов, образуя соли – феноляты.
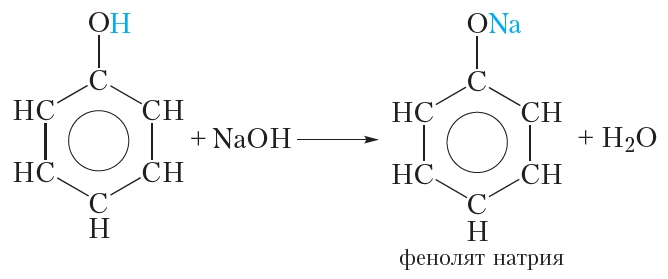
| Например, фенол реагирует с гидроксидом натрия с образованием фенолята натрия |
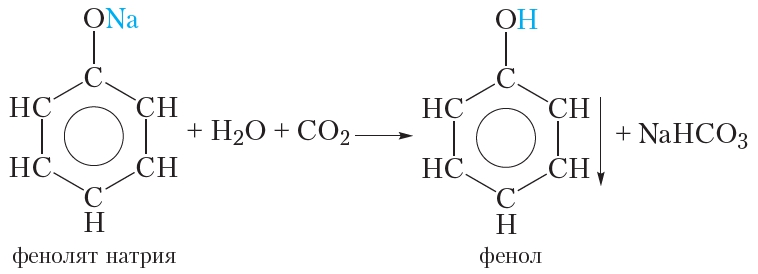
Так как фенол – более слабая кислота, чем соляная и даже угольная, его можно получить из фенолята, вытесняя соляной или угольной кислотой:
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Фенолы взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются феноляты. При взаимодействии с металлами фенолы ведут себя, как кислоты.
2. Реакции фенола по бензольному кольцу
| Наличие ОН-группы в бензольном кольце (ориентант первого рода) приводит к тому, что фенол гораздо легче бензола вступает в реакции замещения в ароматическом кольце. |
2.1. Галогенирование
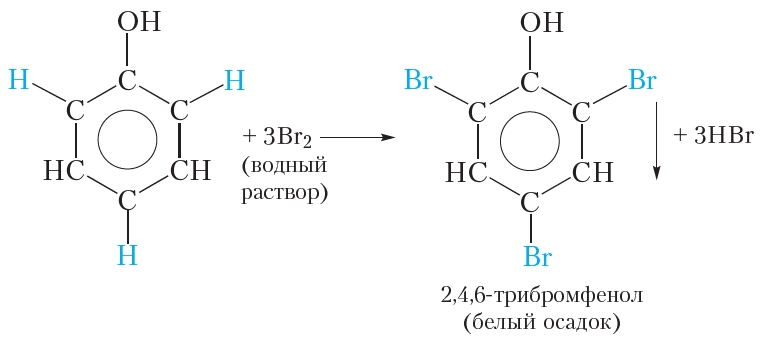
| Фенол легко при комнатной температуре (без всякого катализатора) взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол). |
2.2. Нитрование
Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов.
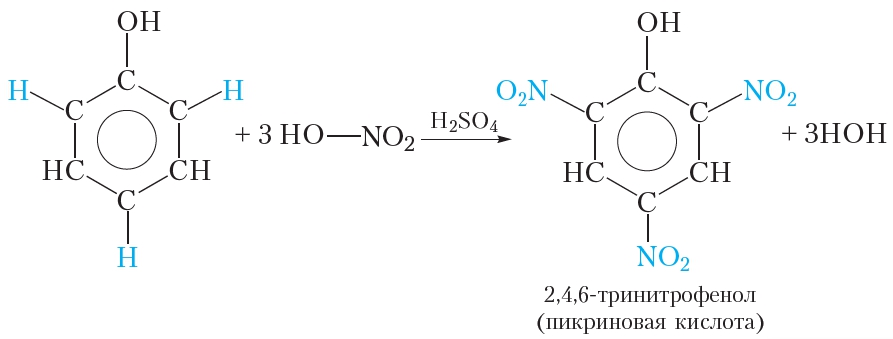
| Например, при нитровании фенола избытком концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота): |
3. Поликонденсация фенола с формальдегидом
С формальдегидом фенол образует фенолоформальдегидные смолы.
4. Взаимодействие с хлоридом железа (III)
При взаимодействии фенола с хлоридом железа (III) образуются комплексные соединения железа, которые окрашивают раствор в сине-фиолетовый цвет. Это качественная реакция на фенол.
5. Гидрирование (восстановление) фенола
Присоединение водорода к ароматическому кольцу.
Продукт реакции – циклогексанол, вторичный циклический спирт.
Получение фенолов
1. Взаимодействие хлорбензола с щелочами
При взаимодействии обработке хлорбензола избытком щелочи при высокой температуре и давлении образуется водный раствор фенолята натрия.
При пропускании углекислого газа (или другой более сильной кислоты) через раствор фенолята образуется фенол.
2. Кумольный способ
Фенол в промышленности получают из каталитическим окислением кумола.
Первый этап процесса – получение кумола алкилированием бензола пропеном в присутствии фосфорной кислоты:
Второй этап – окисление кумола кислородом. Процесс протекает через образование гидропероксида изопропилбензола:
Суммарное уравнение реакции:
3. Замещение сульфогруппы в бензол-сульфокислоте
Бензол-сульфокислота реагирует с гидроксидом натрия с образованием фенолята натрия:
Получается фенолят натрия, из которого затем выделяют фенол:
Класс: 10
Презентация к уроку
Форма урока: комбинированный (2 часа).
Оборудование: мультимедийная установка, шаростержневые модели бензола, этилового спирта, презентация “Химические свойства фенола”.
На ученических столах: коллекция изделий на основе фенолформадегильной смолы, FeCl3, чайная заварка.
1. Организационный момент.
2. Актуализация опорных знаний и мотивация познавательной деятельности.
Учитель: В основе учения об органических веществах лежит теория химического строения А.М.Бутлерова. Объясните почему?
(Ответ: Эта теория раскрывает взаимосвязь между строением веществ и их свойствами, показывает, что свойства веществ неслучайные).
Из каких двух знакомых фрагментов состоит молекула фенола?
Сформулируйте 3 положение теории А.М.Бутлерова.
3. Определение темы урока, целей и задач урока.
Учитель задаёт вопрос: Как вы считаете, какой будет тема урока?
(Ученики высказывают версии, формулируют с помощью учителя тему урока.
Записывают тему урока в тетрадь). Слайд 3.
4. Изучение нового материала.
Учитель: Свойствами каких соединений формально должен обладать фенол?
(Ответ: фенол должен сочетать свойства аренов (бензола) и одноатомных спиртов).
Учитель: Оказывается, это не совсем так.
Именно поэтому фенолы рассматриваются отдельно от класса спиртов.
Учитель: Как Вы думает, в чем причина?
(Ответ: причина кроется в том, что в результате взаимного влияния гидроксильной группы и ароматического радикала химические свойства этих фрагментов изменяются, а фенол в целом приобретает некоторые особенные свойства). (Слайд: 7).
4.1. Кислотные свойства фенола.
Ученики предполагают, что для фенола характерна реакция с Ме (IА). (Слайды: 8, 9).
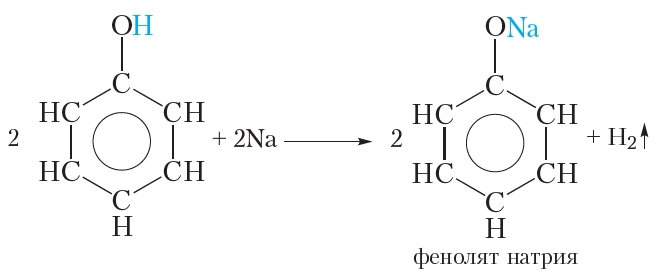
2 C6H5OH +2 Na —> 2 C6H5ONa + H2
В отличие от спиртов фенол взаимодействует с щелочами.
C6H5OH + NaOH
C6H5ONa + H2O
Вопрос: что происходит с солями в водном растворе? Какова реакция среды в растворе фенолята натрия? (Ответ: они гидролизуются; среда щелочная). (Слайд: 13).
Учитель: первым названием фенола было карболовая кислота. Однако кислота эта значительно слабее не только сильных, но даже некоторых неорганических кислот, даже угольной:
C6H5ONa + CO2 +H2O —> C6H5OH
+NaHCO3.
Вопрос: Чем обусловлено различие кислотных свойств спиртов и фенола?
Вопрос: как можно получить сложные и простые эфиры?
Ученики высказывают свои предположения. Затем идет объяснение.
Учитель: в отличие от спиртов, фенолы не образуют сложных эфиров при действии на них карбоновых кислот, для этого можно использовать хлорангидриды кислот. H3CC(O)Cl+HO–C6H5 —> H3C–C(O)–O–C6H5+HCl (Слайд: 16).
В качестве исходных веществ для получения простых и сложных эфиров используются также феноляты. (Слайды: 17, 18).
Затем ученики составляют уравнения возможных реакций получения эфиров. (Слайд: 19). (На усмотрение учителя данное упражнение может быть выполнено учениками в качестве домашнего задания).
4.2. Реакции электрофильного замещения.
Учитель: Почему реакции электрофильного замещения в бензольном кольце фенола протекают легче, чем у бензола, и в более мягких условиях? (Слайд: 20).
Хлорирование (Слайд: 22).
Реакция с бромной водой- качественная реакция. (Слайд: 23, 24).
Аналогичные закономерности наблюдаются при нитровании фенола. Однако при действии на фенол разбавленной азотной кислотой можно получить смесь монозамещенных нитропроизводных: о-нитрофенола и п-нитрофенола. (Слайд: 25).
Электроноакцепторные свойства нитрогрупп значительно усиливают кислотность тринитрофенола. Он является примерно в миллиард раз более сильной кислотой по сравнению с фенолом, и в 100 раз сильнее фосфорной кислоты. (Слайд: 28).
4.3. Реакция поликонденсация.
Работа с коллекцией изделий на основе фенолформадегильной смолы.
4.5. Взаимодействие с раствором хлорида железа (III).
Качественной реакцией на фенол и его гомологи является образование окрашенных комплексов с раствором хлорида железа (III). (Слайд 33, 34).
В экстрактах многих растений, особенно обладающих дубильным и вяжущим действием, содержатся вещества, называемые “танины”. В состав их молекул входит большое число фенольных остатков. Они также дают с хлорным железом интенсивное окрашивание. Ученики проводят опыт: в пробирку наливают 2-3 мл холодной чайной заварки светло-желтого цвета и добавляют 2-3 капли раствора хлорида железа (III). Жидкость приобретает чернильный цвет. В чайных листах содержится большое количество танина, придающего напитку терпкий вяжущий привкус.
Объяснение: фенолы легко окисляются даже под действием кислорода воздуха. На воздухе фенол постепенно окрашивается в розовато-красный цвет. При окислении фенола сильными окислителями основным продуктом окисления является хинон. Двухатомные фенолы окисляются легче. При окислении гидрохинона также образуется хинон.
Окисление фенола и гидрохинона. (Слайд 37, 38). На усмотрение учителя данный материал может быть рассмотрен на элективных курсах при подготовке к ЕГЭ.
5. Заключительная часть.
Задания для закрепления материала и развития логического мышления. (Слайд 39-41).
6. Подведение итогов урока. Рефлексия.
Учитель предлагает ученикам определить результаты урока, сравнить их с целями.
7. (Слайд 42). Домашнее задание.
Параграф 18 по учебнику О.С.Габриелян, И.Г.Остроумов, С.Ю.Пономарев. Химия. 10 класс (М. Дрофа, 2014); стр. 193 № 1-10.
Химия. 10 класс
§ 28. Химические свойства, получение и применение фенола
Химические свойства фенола
В молекуле фенола имеется гидроксильная группа, следовательно, можно ожидать, что фенол будет проявлять химические свойства, присущие спиртам. В то же время из-за влияния бензольного кольца на гидроксильную группу некоторые свойства фенола отличаются от химических свойств спиртов.
1. Взаимодействие со щелочными металлами
Подобно спиртам, фенол реагирует со щелочными металлами. Если в расплавленный фенол пометить кусочек металлического натрия, наблюдается выделение водорода (температура плавления фенола невысока и составляет всего 41 °С). В ходе реакции атом водорода гидроксильной группы замещается на атом натрия:
В результате образуется фенолят натрия. Феноляты, подобно алкоголятам, представляют собой твёрдые солеподобные вещества.
Реакция фенола со щелочными металлами свидетельствует о том, что фенол, как и спирты, проявляет слабые кислотные свойства.
2. Взаимодействие со щелочами (отличие фенола от спиртов)
Кислотные свойства фенола выражены сильнее, чем у спиртов. Это проявляется в том, что, в отличие от спиртов, фенол взаимодействует со щелочами:
Образующийся фенолят натрия хорошо растворяется в воде. Таким образом фенол умеренно растворим в воде, но хорошо растворяется в растворе гидроксида натрия, так как при этом образуется растворимый фенолят натрия. Усиление кислотных свойств фенола по сравнению со спиртами обусловлено влиянием бензольного кольца, которое приводит к уменьшению прочности связи О—Н. В результате атом водорода гидроксильной группы молекулы фенола может замещаться на атом металла не только при взаимодействии со щелочными металлами, но и со щелочами.
По кислотным свойствам фенол превосходит не только спирты, но и воду. Поэтому феноляты, в отличие от алкоголятов, не разлагаются водой. Наличие у фенола кислотных свойств отражает его тривиальное название — карболовая кислота.
Тем не менее фенол — очень слабая кислота. Даже угольная кислота сильнее фенола и поэтому вытесняет его из фенолята натрия:
Эту реакцию можно осуществить следующим образом. Через раствор фенолята натрия пропускают углекислый газ, при этом наблюдается помутнение раствора, так как образующийся фенол выпадает в осадок.
3. Взаимодействие с бромной водой (отличие фенола от бензола)
В молекуле фенола содержится бензольное кольцо, следовательно, можно ожидать, что фенол будет проявлять химические свойства, присущие ароматическим углеводородам, например бензолу. Как вы уже знаете, для бензола характерны реакции замещения атомов водорода. Так, бензол в присутствии катализатора реагирует с бромом. При этом протекает реакция замещения одного атома водорода на бром:
Бромную воду бензол не обесцвечивает!
В молекуле фенола гидроксильная группа влияет на свойства бензольного кольца, облегчая замещение атомов водорода, поэтому взаимодействие фенола с бромом легко протекает и без катализатора. Так, при смешивании разбавленного раствора фенола с бромной водой наблюдается обесцвечивание бромной воды и выпадение белого осадка. Уравнение протекающей реакции:
В результате реакции происходит замещение трёх атомов водорода бензольного кольца атомами брома и образуется 2,4,6-трибромфенол. Отметим, что замещение атома водорода бензольного кольца атомом брома возможно и для бензола, но условия протекания реакции гораздо более жёсткие, чем для фенола. Для этого требуется бром, а не бромная вода, а также катализатор. Бромирование фенола протекает в мягких условиях, что свидетельствует о повышенной реакционной способности бензольного кольца фенола. Это обусловлено влиянием гидроксильной группы, которая облегчает замещение атомов водорода в положениях 2, 4, 6 бензольного кольца молекулы фенола.
4. Взаимодействие с азотной кислотой
При взаимодействии фенола со смесью концентрированных азотной и серной кислот можно заместить три атома водорода бензольного кольца на группы —NO2:
В результате реакции образуется 2,4,6-тринитрофенол. Кислотные свойства 2,4,6-тринитрофенола выражены значительно сильнее, чем у фенола. Тривиальное название 2,4,6-тринитрофенола — пикриновая кислота. Пикриновая кислота и её соли являются взрывчатыми веществами.
Рассмотренные химические свойства фенола демонстрируют взаимное влияние атомов в молекулах органических соединений: бензольное кольцо усиливает кислотность гидроксильной группы молекулы фенола, в свою очередь, гидроксильная группа влияет на бензольное кольцо, облегчая замещение атомов водорода в положениях 2, 4, 6.
Тема №22 «Характерные свойства фенолов»
Фенолы — органические вещества, молекулы которых содержат радикал фенил, связанный с одной или несколькими гидроксогруппами.
Характерные свойства фенолов
Оглавление
Строение фенолов
Гидроксильная группа в молекулах органических соединений может быть связана с ароматическим ядром непосредственно, а может быть отделена от него одним или несколькими атомами углерода. Можно ожидать, что в зависимости от этого свойства вещества будут существенно отличаться друг от друга из-за взаимного влияния групп атомов. И действительно, органические соединения, содержащие ароматический радикал фенил С6Н5—, непосредственно связанный с гидроксильной группой, проявляют особые свойства, отличные от свойств спиртов. Такие соединения называются фенолами.
Фенолы — органические вещества, молекулы которых содержат радикал фенил, связанный с одной или несколькими гидроксогруппами. Так же как и спирты, фенолы классифицируют по атомности, т. е. по количеству гидроксильных групп.
Одноатомные фенолы содержат в молекуле одну гидроксильную группу:
Многоатомные фенолы содержат в молекулах более одной гидроксильной группы:
Существуют и другие многоатомные фенолы, содержащие три и более гидроксильных групп в бензольном кольце.
Познакомимся подробнее со строением и свойствами простейшего представителя этого класса — фенолом С6Н5ОН. Название этого вещества и легло в основу названия всего класса — фенолы.
Физические свойства фенолов
Фенол — твердое, бесцветное кристаллическое вещество, t° = 43 °С, t° = 181 °С, с резким характерным запахом. Ядовит. Фенол при комнатной температуре незначительно растворяется в воде. Водный раствор фенола называют карболовой кислотой. При попадании на кожу он вызывает ожоги, поэтому с фенолом необходимо обращаться осторожно!
Химические свойства фенолов
Кислотные свойства. Атом водорода гидроксильной группы обладает кислотным характером. Кислотные свойства у фенола выражены сильнее, чем у воды и спиртов. В отличие от спиртов и воды, фенол реагирует не только с щелочными металлами, но и со щелочами с образованием фенолятов:
Однако кислотные свойства у фенолов выражены слабее, чем у неорганических и карбоновых кислот. Так, например, кислотные свойства фенола примерно в 3000 раз меньше, чем у угольной кислоты. Поэтому, пропуская через водный раствор фенолята натрия углекислый газ, можно выделить свободный фенол.
Добавление к водному раствору фенолята натрия соляной или серной кислоты также приводит к образованию фенола:
Качественная реакция на фенол
Фенол реагирует с хлоридом железа (III) с образованием интенсивно окрашенного в фиолетовый цвет комплексного соединения.
Эта реакция позволяет обнаруживать его даже в очень ограниченных количествах. Другие фенолы, содержащие одну или несколько гидроксильных групп в бензольном кольце, также дают яркое окрашивание сине-фиолетовых оттенков в реакции с хлоридом железа (III).
Реакции бензольного кольца
Наличие гидроксильного заместителя значительно облегчает протекание реакций электрофильного замещения в бензольном кольце.
1. Бромирование фенола.
В отличие от бензола для бромирования фенола не требуется добавления катализатора (бромида железа (III)). Кроме того, взаимодействие с фенолом протекает селективно (избирательно): атомы брома направляются в орто- и параположения, замещая находящиеся там атомы водорода. Селективность замещения объясняется рассмотренными выше особенностями электронного строения молекулы фенола.
Так, при взаимодействии фенола с бромной водой образуется белый осадок 2,4,6-трибромфенола:
Эта реакция, так же как и реакция с хлоридом железа (III), служит для качественного обнаружения фенола.
2. Нитрование фенола также происходит легче, чем нитрование бензола. Реакция с разбавленной азотной кислотой идет при комнатной температуре. В результате образуется смесь орто- и параизомеров нитрофенола:
При использовании концентрированной азотной кислоты образуется 2,4,6-тринитрофенол — пикриновая кислота, взрывчатое вещество:
3. Гидрирование ароматического ядра фенола в присутствии катализатора происходит легко:
4. Поликонденсация фенола с альдегидами, в частности, с формальдегидом происходит с образованием продуктов реакции — фенолформальдегидных смол и твердых полимеров.
Взаимодействие фенола с формальдегидом можно описать схемой:
В молекуле димера сохраняются «подвижные» атомы водорода, а значит, возможно дальнейшее продолжение реакции при достаточном количестве реагентов:
Реакция поликонденсации, т. е. реакция получения полимера, протекающая с выделением побочного низкомолекулярного продукта (воды), может продолжаться и далее (до полного израсходования одного из реагентов) с образованием огромных макромолекул. Процесс можно описать суммарным уравнением:
Образование линейных молекул происходит при обычной температуре. Проведение же этой реакции при нагревании приводит к тому, что образующийся продукт имеет разветвленное строение, он твердый и нерастворим в воде. В результате нагревания фенолформальдегидной смолы линейного строения с избытком альдегида получаются твердые пластические массы с уникальными свойствами. Полимеры на основе фенолформальдегидных смол применяют для изготовления лаков и красок, пластмассовых изделий, устойчивых к нагреванию, охлаждению, действию воды, щелочей и кислот. Они обладают высокими диэлектрическими свойствами. Из полимеров на основе фенолформальдегидных смол изготавливают наиболее ответственные и важные детали электроприборов, корпуса силовых агрегатов и детали машин, полимерную основу печатных плат для радиоприборов. Клеи на основе фенолформальдегидных смол способны надежно соединять детали самой различной природы, сохраняя высочайшую прочность соединения в очень широком диапазоне температур. Такой клей применяется для крепления металлического цоколя ламп освещения к стеклянной колбе. Таким образом, фенол и продукты на его основе находят широкое применение.
Шпаргалка
Справочный материал для прохождения тестирования:


















 C6H5ONa + H2O
C6H5ONa + H2O +NaHCO3.
+NaHCO3.