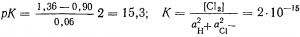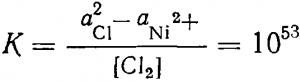Рафинированный никель что это
Рафинированный никель что это
Еще несколько лет назад приобрести мебель прямо с производственной площадки было немного проблематично. Покупались предметы интерьера только в мебельных магазинах, где к.
Металлоконструкции все чаще используются для строительства сооружений и зданий разного назначения. Скорость проведения работ, доступность – важные плюсы технологии. В.
Российская компания «Изорок» производит одноименный утеплитель. Минеральная основа присутствует во всей этой категории продукции бренда. Несколько модификаций.
Бурение скважин является широко популярной услугой, которая помогает не быть зависимым от централизованного водоснабжения, получить собственный источник чистой воды.
Как правило, для заведений общественного питания необходимо специальное оборудование. Без холодильного стола на кухни ни как не обойтись. Это оборудование объединяет в.
Незастекленный балкон является своеобразным бельмом на глазу современных апартаментов, заметно проигрывающим в своей эстетике тем балконным конструкциям, на которых уже.
Как только на рынке появились первые лампочки, они имели цоколь е27, они и сегодня пользуется очень большим спросом. Это стандартизация мирового масштаба, практически в.
Строительная сфера очень развита, сегодня можно увидеть объекты только на подготовленных сухих площадках, но и на воде. Обратите внимание на современный порт, большая.
Электролитическое рафинирование никеля

Анодное растворение чернового никеля в серной кислоте из-за малого тока обмена требует значительной поляризации. При малой скорости образования ионов Ni 2+ по мере повышения плотности тока на аноде возникают пленки окислов.
1 — аноды; 2 — катод; 3 — диафрагма
Если учесть высокое перенапряжение кислорода на пленке окислов, образование их до начала реакции представляется вполне вероятным. В сульфатном электролите никелевый анод растворяется с малым выходом по току при потенциале 1,5—
Даже небольшие добавки хлоридов предупреждают пассиви рование анода. Образование окисных пленок становится менее вероятным вследствие разрушения их, например по реакции:
Хлор не выделяется и не накапливается в электролите: он окисляет медь, никель, сульфиды и другие составляющие анодов и шлама, в частности
Константу равновесия (163) легко вычислить из формул (162,6) и (39)
pК = ( — 0,23 —1,36):0,06)2 = —53
Подставив значение aNi2+ = 1 г-ион/л и аСl-=0,1 г-ион/л в
Из сопоставления равновесных концентраций хлора в реакциях (163) и (164) очевидна невозможность образования окисной пленки на никелевых анодах даже при весьма малой активности ионов хлора.
В практике электролиза никеля, начиная с 1939 г., постепенно повышается ионное отношение Сl — : SO 2 4 — в электролите с 0,15 до 1,5. Состав одного из современных растворов дан ниже:
г-ион/л (моль/л) 1,50 1,1 1,2 1,7 0,08
Полная замена сульфатов хлоридами не выгодна: электропроводность от этого повысится, и напряжение на ванне станет
ниже, но уменьшится и приход тепла, необходимый для поддержания температуры электролита около 60° С.
Заводские аноды содержат 80—92% никеля. Содержание примесей должно быть не более: меди 5, железа 4, кобальта 1, платиноидов — преимущественно платины и палладия суммарно 0,1%.
Несмотря на присутствие хлоридов, аноды требуют значительной поляризации, несколько понижаемой подогревом раствора. Они растворяются при потенциале около 0,35 В, который почти на 0,6 В положительнее равновесного. Дополнительной причиной тому служат неметаллические включения и поверхностные отложения в виде корки, вызывающей концентрационную поляризацию.
Основная составляющая анодов — твердый раствор меди и никеля, содержащий включения сульфидов тех же металлов и примеси.
Медь переходит в раствор по схеме 13 (см. табл. 4), а кроме того, дает комплексные ионы:
Сu + Сl — — е = СuСl (рПР = 5,92), Е° = 0,14 В,
Для сульфида меди вычислено:
Cu2S + 2Сl — — 2е = 2CuCl + S; Е 0 = 1,05 В,
Из сопоставления этих данных с потенциалом растворяющегося анода видна малая вероятность растворения Cu 2S, он накапливается в поверхностной корке и шламе, где бывает до 20% меди. Сульфид никеля также здесь присутствует, хотя потенциал его окисления сравнительно невелик:
Надо заметить, что электрический контакт частиц сульфидов в слое шлама на поверхности анодов, вероятно, нарушает присутствующая здесь элементарная сера. Присутствие элементарной серы в шламе и в корке на аноде подтверждает это. Вместе с тем накапливаются и ионы SO 2 4 — электролите. Окисление S 2-
или S 0 до сульфата многостадийно из-за возможности промежуточного образования SO 2 3 — и S nO 2 m — .
По литературным данным, из суммарных уравнений для кислых растворов приемлемо следующее:
Селениды и теллуриды меди и никеля вместе с платиновыми металлами и не полностью растворенными обломками анодов выпадают в шлам, выход которого составляет приблизительно
2—5% от массы чернового никеля.
Статья на тему Электролитическое рафинирование никеля
Похожие страницы:
Понравилась статья поделись ей
Никель это металл. Применение, свойства, марки, история открытия, достоинства и недостатки никеля





История открытия Никель Niccolum
Открытие элемента Niccolum — Никель (англ., франц. и нем. Nickel) открыт в 1751 г. Однако задолго до этого саксонские горняки хорошо знали руду, которая внешне походила на медную и применялась в стекловарении для окраски стёкол в зелёный цвет. Все попытки получить из этой руды медь оказались неудачными, в связи с чем в конце XVII в. руда получила название купферникель (Kupfernickel), что приблизительно означает «Медный дьявол».
Данную руду (красный никелевый колчедан NiAs) в 1751 г. исследовал шведский минералог Кронштедт. Ему удалось получить зелёный окисел и путём восстановления последнего — новый металл, названный никелем.







Биологическая роль
Никель — микроэлемент, который необходим всем живым организмам. Его среднее содержание в растениях — 0,00005 %, в наземных животных — 0,000001 %, в морских — 0,00016 % массы тела.
Роль никеля в организме изучена не до конца. Известно, что он участвует в ферментативных реакциях и влияет на окислительные процессы. Он содержится в легких, печени, мышцах, поджелудочной и щитовидной железах, некоторых отделах головного мозга. Микроэлемент также накапливается в ороговевших тканях человека, животных и птиц, в том числе в волосах и перьях.
Избыточное содержание никеля в растениях приводит к уродливым формам, в организме животных — к различным глазным заболеваниям (кератоконъюнктивитам, кератитам).
Пары и пыль никеля токсичны и могут вызывать поражения кожи, легких и носоглотки, а частое вдыхание паров металла опасно появлением злокачественных новообразований.
Металл оказался похож на железо во своим свойствам
Бергман получил металл в более чистом виде, он установил, что по своим свойствам металл похож на железо; более подробно никель изучали многие химики, начиная с Пруста. Никкел — ругательное слово на языке горняков. Оно образовалось из искажённого Nicolaus — родового слова, имевшего несколько значений. Но главным образом слово Nicolaus служило для характеристики двуличных людей; кроме того, оно обозначало «озорной маленький дух», «обманчивый бездельник» и т. д.
В русской литературе начала XIX в. употреблялись названия николан (Шерер, 1808 и Захаров, 1810), николь и никель (Двигубский, 1824).





Химические параметры
Атомы никеля имеют следующую электронную формулу 3d84s2. Самое стабильное его состояние — это окисление.
Никель образовывает смеси уровнем оксидирования +1, +2, +3 и +4. Смеси никеля с уровнем оксидировния +4 встречаются нечасто и отличаются неустойчивостью.
Еще одно отличительное свойство металла его устойчивость к коррозии. Причём, эта устойчивость сохраняется на воздухе, воде и некоторых агрессивны средах, например, щелочах и кислотах. Это свойство обусловлено тем, что на поверхности образуется плотная оксидная пленка, которая обладает защитными свойствами. Между тем, никель смешивается со слабой смесью азотной кислоты или в нагретой сконцентрированной серной.
Никель неторопливо входит в реакцию с соляной или смесью серной кислоты. Азотная кислота в концентрированной форме, образовывает на деталях из никеля оксидный слой.
При вступлении в связь с оксидом углерода появляется ядовитое вещество под названием карбонил, он обладает следующей формулы Ni(CO)4.
Мелкий порошок отличается тем, что может загореться на воздухе. Кстати, никель горит только в порошкообразном виде. В этом процессе происходит образование двух оксидов и двух гидрооксидов. Существуют несколько солей никеля — ацетат, хлорид, нитрат и сульфат.
Соли могут быть растворены в воде. Такие смеси обладают зеленым окрасом. Сухие соли окрашены в желтые оттенки.
Никель может образовывать различные виды соединений, в т. ч., координационные и комплексные. Как пример можно рассмотреть диметилглиоксимат, который выдает красный окрас в кислой среде и применяемый при проведении качественного анализа для выявления никеля.
Смесь сульфата никеля в воде обладает зеленым окрасом.
При проведении разных реакций он может образовывать сочетания с тетраэдрической и с двумерной квадратной структурой.
В качественном и количественном исследовании, проводимого для выявления никеля применяют смесь бутандиондиоксима. Еще эта смесь имеет и второе наименование реактив Чунаева. Так звали учёного, выявившего, что эта смесь помогает выявлять никель.
Физические свойства Никель Niccolum
Основные свойства Niccolum Никель — серебристо-белый металл, не тускнеет на воздухе. Имеет гранецентрированную кубическую решетку с периодом a = 0,35238 нм, пространственная группа Fm3m. В чистом виде весьма пластичен и поддается обработке давлением. Является ферромагнетиком с точкой Кюри 358 °C.
Изотопы Niccolum Никель
Наличие и определение изотопов Niccolum
Нахождение в природе и производство
Больше всего никеля содержится в глубоких слоях. В земной коре — его 0,0058%, в ультраосновных породах — 0,2 %. Если верить гипотезе, что земное ядро состоит из никелистого железа, общее содержание никеля в земле составляет примерно 3%. Никель также обнаружен в некоторых метеоритах.
В земной коре этот металл соседствует с железом и магнием, с которыми он имеет сходную валентность. В минералах магния и железа никель содержится в виде изоморфной примеси. Также существует 53 известных науке минерала никеля. Большая часть из них была образована под воздействием давления и высоких температур, например, при застывании магмы. Сульфидные руды, содержащие данный металл, имеют в своем составе медь. Некоторые руды никеля включают железо, серу, мышьяк, кобальт, магний.
Больше всего этого металла добывается на территории России. Крупные никелевые рудники также находятся в Канаде, Австралии, Новой Каледонии, Индонезии и на Кубе.
Больше всего никеля (около 80%) получают из сульфидных медно-никелевых руд, значительно меньше — из силикатных (окисленных) руд.
Интересные факты
Получение
Общие запасы никеля в рудах на начало 1998 года оцениваются в количестве 135 млн т., в том числе достоверные — 49 млн.т. Основные руды никеля — никелин (купферникель) NiAs, миллерит NiS, пентландит (FeNi)9S8 — содержат также мышьяк, железо и серу; в магматическом пирротине также встречаются включения пентландита. Другие руды, из которых тоже добывают Ni, содержат примеси Co, Cu, Fe и Mg. Иногда никель является основным продуктом процесса рафинирования, но чаще его получают как побочный продукт в технологиях других металлов. Из достоверных запасов, по разным данным, от 40 до 66 % никеля находится в «окисленных никелевых рудах» (ОНР), 33 % — в сульфидных, 0,7 % — в прочих. По состоянию на 1997 г. доля никеля, произведённого переработкой ОНР, составила порядка 40 % от общемирового объёма производства. В промышленных условиях ОНР делят на два типа: магнезиальные и железистые.
Тугоплавкие магнезиальные руды, как правило, подвергают электроплавке на ферроникель (5—50 % Ni+Co, в зависимости от состава сырья и технологических особенностей).
Наиболее железистые — латеритовые руды перерабатывают гидрометаллургическими методами с применением аммиачно-карбонатного выщелачивания или сернокислотного автоклавного выщелачивания. В зависимости от состава сырья и применяемых технологических схем конечными продуктами этих технологий являются: закись никеля (76-90 % Ni), синтер (89 % Ni), сульфидные концентраты различного состава, а также металлические никель электролитный, никелевые порошки и кобальт.
Менее железистые — нонтронитовые руды плавят на штейн. На предприятиях, работающих по полному циклу, дальнейшая схема переработки включает конвертирование, обжиг файнштейна, электроплавку закиси никеля с получением металлического никеля. Попутно извлекаемый кобальт выпускают в виде металла и/или солей.[11] Ещё один источник никеля: в золе углей Южного Уэльса в Англии — до 78 кг никеля на тонну. Повышенное содержание никеля в некоторых каменных углях, пефтях, сланцах говорит о возможности концентрации никеля ископаемым органическим веществом. Причины этого явления пока не выяснены.
«Никель долгое время не могли получить в пластичном виде вследствие того, что он всегда имеет небольшую примесь серы в форме сульфида никеля, расположенного тонкими, хрупкими прослойками на границах металла. Добавление к расплавленному никелю небольшого количества магния переводит серу в форму соединения с магнием, которое выделяется в виде зерен, не нарушая пластичности металла.»[12]
Основную массу никеля получают из гарниерита и магнитного колчедана.
Содержание
Примечания
Применение
В 2015 году 67 % потребления никеля пришлось на производство нержавеющей стали, 17 % на сплавы без железа, 7 % на никелирование и 9 % на прочие применения, такие как аккумуляторы, порошковая металлургия и химические реактивы[13].
Сплавы
Никель является основой большинства суперсплавов — жаропрочных материалов, применяемых в аэрокосмической промышленности для деталей силовых установок.
Никелирование
Никелирование — создание никелевого покрытия на поверхности другого металла с целью предохранения его от коррозии. Проводится гальваническим способом с использованием электролитов, содержащих сульфат никеля(II), хлорид натрия, гидроксид бора, поверхностно-активные и глянцующие вещества, и растворимых никелевых анодов. Толщина получаемого никелевого слоя составляет 12—36 мкм. Устойчивость блеска поверхности может быть обеспечена последующим хромированием (толщина слоя хрома — 0,3 мкм).
Бестоковое никелирование проводится в растворе смеси хлорида никеля(II) и гипофосфита натрия в присутствии цитрата натрия:
N i C l 2 + N a H 2 P O 2 + H 2 O → N i + N a H 2 P O 3 + 2 H C l <\displaystyle <\mathsf
Процесс проводят при рН 4—6 и 95 °C[14].
Производство аккумуляторов
Производство железо-никелевых, никель-кадмиевых, никель-цинковых, никель-водородных аккумуляторов.
Химическая технология
Во многих химико-технологических процессах в качестве катализатора используется никель Ренея.
Радиационные технологии
Нуклид 63Ni, излучающий β—частицы, имеет период полураспада 100,1 года и применяется в крайтронах, а также детекторах электронного захвата (ЭЗД) в газовой хроматографии.
Медицина
Монетное дело
Никель широко применяется при производстве монет во многих странах[15]. В США монета достоинством в 5 центов носит разговорное название «никель»[16].
Музыкальная промышленность
Также никель используется для производства обмотки струн музыкальных инструментов.
Цены на никель
Золото — 19,29 г/см³

С давних времен люди покупают, продают и даже убивают за этот драгоценный металл. Да что люди, целые страны занимаются скупкой золота. Лидером государств с самыми крупными запасами золота на данный момент является Америка. И вряд ли наступит пора, когда в золоте не будет нужды.
Говорят, что деньги не растут на деревьях, но золото — растет! Небольшое количество золота можно найти в листьях эвкалипта, если тот находится на золотоносной почве.
ИТС 12-2019 Производство никеля и кобальта
1.3.3. Получение рафинированного никеля
Как было показано выше, при переработке сульфидных и окисленных никелевых руд никель и кобальт обычно концентрируются в богатых промежуточных продуктах, за исключением гидрометаллургических технологий, использующих метод жидкостной экстракции, который позволяет производить товарные катодные металлы без промежуточного осаждения концентратов. К этим богатым промпродуктам, пригодным для дальнейшего рафинирования с получением товарных никеля и кобальта, относятся: файнштейн (сульфидные руды), штейн, смешанные никель-кобальтовые гидроксиды (или карбонаты), смешанные никель-кобальтовые сульфиды (окисленные никелевые руды).
Способы переработки сульфидных никелевых продуктов чрезвычайно разнообразны (табл.1.25) и определяются составом и экономическими соображениями с учётом географического положения и исторических особенностей развития конкретных предприятий. Однако обзор мировой практики получения рафинированного никеля показывает практически повсеместное распространение процессов гидрометаллургического рафинирования файнштейна. Наряду с получением никеля электроэкстракцией в мировой практике достаточно широко применяется карбонил-процесс, позволяющий получать никелевую продукцию с высокой добавленной стоимостью. Он реализован на предприятиях Vale: Copper Cliff (Канада) и Clydach (Великобритания), а также на заводе Jinchuan (Китай) компании Jinchuan Group и на комбинате Североникель (АО КГМК, ПАО «ГМК «Норильский никель», Россия). На заводах Copper Cliff и Jinchuan также осуществляют электролитическое рафинирование сульфидных анодов.
На ряде предприятий с целью упрощения технологической схемы Ni-Cu-МПГ файнштейны медленно охлаждают, что способствует раскристаллизации, при этом образуются крупные индивидуальные зерна хизлевудита 
65% Ni, 17% Cu и высоким содержанием Au, Ag и МПГ направляется на конвертирование в конвертерах TBRC и далее на карбонилирование. Разделение меди от никеля в немагнитной фракции осуществляется флотацией. Полученный никелевый сульфидный концентрат (
71% Ni, 0,9% Cu) поступает на окислительный обжиг с получением NiO для отправки на завод компании Clydach (Великобритания), где он перерабатывается карбонил-процессом при атмосферном давлении. Медный сульфидный концентрат (
74% Cu, 4% Ni) поступает в медеплавильное производство. Промпродукт (подситовый продукт измельчения и очистки медного концентрата), содержащий
66% Ni и 6,6% Cu, обжигают и далее рафинируют карбонилированием на Copper Cliff.
Презентация по теме «Электролитическое рафинирование никеля»
Онлайн-конференция
«Современная профориентация педагогов
и родителей, перспективы рынка труда
и особенности личности подростка»
Свидетельство и скидка на обучение каждому участнику
Описание презентации по отдельным слайдам:
Электролитическое рафинирование никеля
Анодный никель – сложный по составу сплав, содержащий по крайней мере, двенадцать металлических элементов, включая железо и химические соединения металлов с селеном, теллуром, кислородом и серой
ЦЕЛЬ РАФИНИРОВАНИЯ ЧЕРНОВОГО НИКЕЛЯ СВОДИТСЯ К ПОЛУЧЕНИЮ ЧИСТОГО КАТОДНОГО НИКЕЛЯ НЕ НИЖЕ МАРОК Н-0 И Н-1 И ПОПУТНОМУ ИЗВЛЕЧЕНИЮ ПРИСУТСВУЮЩИХ В АНОДНОМ МЕТАЛЛЕ ЦЕННЫХ СПУТНИКОВ – КОБАЛЬТА, ПЛАТИНОИДОВ, ЗОЛОТА, СЕРЕБРА, МЕДИ, СЕЛЕНА И ТЕЛЛУРА. МАРКИ ЭЛЕКТРОЛИТНОГО НИКЕЛЯ Н-0 И Н-1 СОГЛАСНО ГОСТ 849-70 ДОЛЖНЫ СОДЕРЖАТЬ НИКЕЛЯ И КОБАЛЬТА СООТВЕТСВЕННО НЕ МЕНЕЕ 99,99% И 99,93%
Электролитическое рафинирование никеля – сложный электрохимический процесс. Никель является электроотрицательным металлом и поэтому такие примеси как кобальт, железо,цинк, медь, а также катионы водорода могут совместно с ним или раньше разряжаться на катоде.
Главная задача электролиза — получение никеля высших марок (ГОСТ 849—70) HO, Н1У, H1 с содержанием 99,99—99,93% никеля + кобальта и попутное извлечение кобальта и платиновых металлов, ценность которых выше ценности никеля.
Основная особенность электролиза никелевого анода на промышленных установках заключается в том, что на катоде вместе с никелем могут осаждаться медь, водород, железо, кобальт и еще ряд металлов. Чтобы обеспечить осаждение на катоде только никеля, при электролизе катодное пространство в электролитной ванне отделяют от анодного диафрагменной ячейкой (ящиком), которую делают из брезента или другой плотной ткани, натянутой на каркас ячейки. Помещая катодную основу в диафрагменную ячейку (рис. 1), разделяют электролит в ванне на два объема. Электролит внутри катодной ячейки называют католитом, а находящийся вокруг анода — анолитом.
Анолит содержит медь и другие примеси; поскольку они растворяются на аноде вместе с никелем, то могут загрязнить катодный осадок. Поэтому анолит выводят из электролитной ванны и он поступает на очистку от примесей в отдельной аппаратуре. Очищенный раствор — католит — непрерывно заливают внутрь диафрагмы со скоростью 20—30 л/ч на каждую катодную ячейку, чтобы уровень католита в диафрагме был всегда на 25—30 мм выше уровня анолита.
Катодный процесс. На катоде происходит электрохимическое восстановление никеля с образованием на катодной основе плотного слоя металла: Ni2+ + 2е = Ni. На эту реакцию расходуется основная доля электрического тока Анодный процесс. Основным анодным процессом является растворение никеля: Ni — 2е = Ni2+. Аналогично растворяются железо, кобальт, медь, содержащиеся в анодах. Выход по току. Проходящий через анод электрический ток расходуется не только на растворение никеля, но и на растворение других металлов, а также на выделение водорода и кислорода Основные показатели электролиза никеля В электролитной ванне устанавливают 31—45 катодов и 32— 47 анодов. Электролиз ведут при температуре католита 70—75° С и плотности тока 260—360 А м2 площади катода. Выход никеля по току достигает 96% при напряжении на ванне 2,6—3 В. Расход энергии постоянного тока колеблется в пределах от 2400 до 3300 кВт*ч/т никеля.
Курс повышения квалификации
Охрана труда
Курс профессиональной переподготовки
Библиотечно-библиографические и информационные знания в педагогическом процессе
Курс профессиональной переподготовки
Охрана труда
Ищем педагогов в команду «Инфоурок»
Номер материала: ДБ-1409993
Не нашли то что искали?
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Педагогам Северной Осетии в 2022 году будут выплачивать надбавки за стаж
Время чтения: 2 минуты
Трехлетнюю олимпиаду среди школ запустят в России в 2022 году
Время чтения: 1 минута
Учителям предлагают 1,5 миллиона рублей за переезд в Златоуст
Время чтения: 1 минута
В Оренбурге школьников переведут на дистанционное обучение с 9 декабря
Время чтения: 1 минута
Путин поручил не считать выплаты за классное руководство в средней зарплате
Время чтения: 1 минута
ВПР для школьников в 2022 году пройдут весной
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.