Ребенок выпил беродуал что делать
Хронический и острый бронхит: чем опасна болезнь и как её лечить
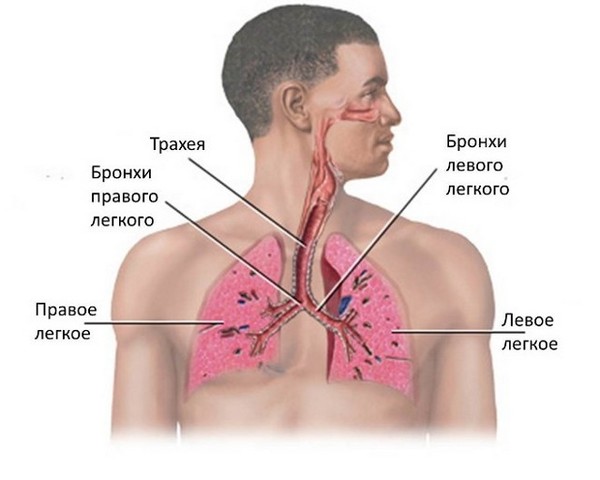
Бронхит – это патологическое состояние, при котором развивается воспаление бронхов. В свою очередь, бронхи – это пути, которые проводят воздух от трахеи к тканям легких, согревают воздушный поток, увлажняют и очищают его. Находятся они в нижней части трахеи и представляют собой две крупных ветви.
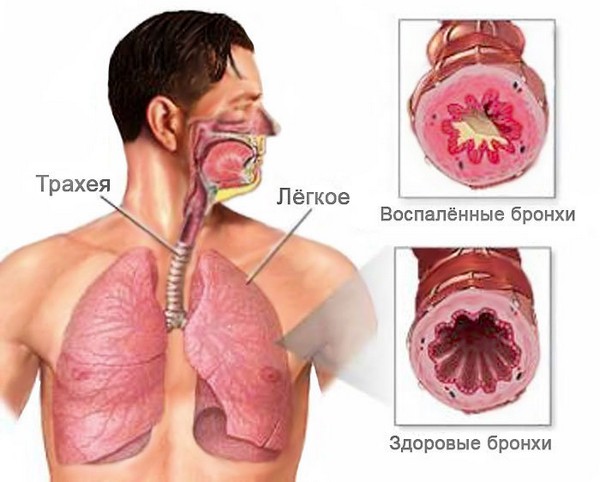
Болезнь вызывает воспаление слизистой оболочки или всей толщи бронхиальных стенок. Начинается чрезмерное выделение слизи, затрудняется дыхание. Организм пытается самостоятельно вывести лишнюю слизь, поэтому появляется сильный мучительный кашель. Патология может переходить из кратковременной острой в продолжительную хроническую форму, поэтому требует комплексного незамедлительного лечения.
Острый бронхит
Развивается в подавляющем большинстве случаев и представляет собой распространенное осложнение острой респираторной инфекции. Зачастую диагностируется у детей, так как они более восприимчивы к подобным инфекциям.
При остром поражении бронхов происходит размножение условно-патогенной микрофлоры. Слизистая меняет свою структуру, развивается поражение верхних слоев и стенок бронхов. Формируется отек слизистой, эпителиальные клетки отторгаются организмом, появляются инфильтраты на подслизистом слое. Процессы сопровождаются тяжелым продолжительным кашлем, который может сохраняться даже после излечения пациента.
Острая форма лечится в течение 3-4 недель. На протяжении этого времени восстанавливается структура и функции бронхов. При правильной и своевременной терапии прогноз благоприятный.
Хронический бронхит
При хроническом бронхите кашель с выделением мокроты наблюдается на протяжении не менее двух лет в течение трех месяцев ежегодно. При этом важно исключить наличие других причин кашля.
Такая форма чаще возникает у взрослых, так как формируется только при длительном раздражении бронхов. Причиной раздражения может быть не только многократно перенесенное острое заболевание, но и сигаретный дым, газы, пыль, химические испарения и прочие отрицательные факторы.
Продолжительное воздействие на слизистую бронхов неблагоприятных факторов вызывает изменения в слизистой, постепенное повышение выделения мокроты. Существенно снижается способность бронхов проводить воздух, а вентиляция легких нарушается.
Формы хронического бронхита
В зависимости от характера воспалительных процессов выделяют:
С учетом наличия нарушения проходимости (обструкции) дыхательных путей бронхит может быть:
По причинам развития болезни выделяют:
Причины заболевания
При острой и хронической формах причины развития патологического состояния бронхов несколько отличаются.
Острый бронхит в 90% случаев формируется в результате попадания в организм вирусной инфекции: гриппа, аденовируса, респираторно-синцитиального, коревого или коклюшного вируса, а также прочих возбудителей. Реже болезнь становится результатом бактериального поражения стафилококком, стрептококком, пневмококком и др.
Среди прочих факторов, которые способствуют развитию острой формы болезни:
При хронической форме основной причиной развития признано курение. У курильщиков болезнь диагностируют в 2-5 раз чаще, чем у некурящих людей. Табачный дым наносит вред как при активном, так и при пассивном курении.
Среди прочих предпосылок развития хронической формы – повторно перенесенные и частые острые бронхиты, ОРВИ, пневмонии, болезни носоглотки. Инфекционная составляющая в таких условиях усугубляет уже имеющееся поражение бронхов.
Симптомы бронхита
Признаки патологии отличаются в зависимости от острой или хронической формы течения болезни:
Осложнения
Острый бронхит может провоцировать осложнение в виде бронхопневмонии – инфекционно-воспалительного процесса, который поражает легкие, вызывает лихорадку, сухой кашель, общую слабость.
Бесконтрольное прогрессирование хронического заболевания приводит к регулярным острым пневмониям и со временем переходит в обструктивную болезнь легких. При этом сужается просвет и отекает слизистая дыхательных путей, частично разрушаются легочные ткани.
Хронический бронхит также может стать причиной развития легочной гипертензии, сердечно-легочной недостаточности, эмфиземы легких, бронхоэктатичской болезни, пневмонии и ряда других опасных заболеваний.
Когда стоит обратиться к врачу
Крайне важно не пускать болезнь на самотек. К врачу нужно обращаться при появлении первых симптомов возможного бронхиального поражения: кашля, повышенной температуры, недомогания. Врач проведет диагностику, укажет, как и чем лечить бронхит и кашель, а дальнейшая терапия пройдет в домашних условиях под контролем доктора. В большинстве случаев патология не требует госпитализации.
Бесконтрольное течение острой болезни в большинстве случаев приводит к усугублению симптоматики, повторному развитию заболевания, переходу в хроническую болезнь и формированию осложнений.
Чтобы определить болезнь и изучить степень поражения бронхов, необходима комплексная диагностика пациента и изучение клинической картины. Этим занимается терапевт или педиатр, который назначает необходимые для диагностики обследования. При необходимости он направляет пациента на консультации к пульмонологу и другим смежным специалистам.
Если по результатам опроса и осмотра у врача появились подозрения на бронхит или другие схожие болезни, назначаются дополнительные обследования:
Среди возможных дополнительных исследований: эхокардиография, электрокардиография, бронхография и др.
Лечение
Терапия бронхита носит комплексный характер, так как преследует цель избавить организм от инфекции, восстановить проходимость бронхов, устранить усугубляющие болезнь факторы.
В первые дни острой фазы необходимо придерживаться постельного режима, много пить, соблюдать молочно-растительную диету. Крайне важно отказаться от курения и поддерживать влажность воздуха в помещении, где находится больной, на уровне 40-60%.
Медикаментозная терапия острой стадии cводится к приему препаратов, которые облегчают симптомы и предотвращают развитие осложнений. Для этого используют:
Важную роль играет физиотерапия. Улучшить состояние пациента помогает лечебная гимнастика, физиотерапия, вибрационный массаж.
Хроническая форма заболевания требует продолжительного лечения как при обострении, так и во время ремиссии. Схема терапии предусматривает прием перечисленных препаратов по назначению врача, а также интенсивную программу легочной реабилитации, которая помогает снизить проявления болезни.
Максимально важно устранить из жизни пациента причину, которая спровоцировала развитие хронического бронхита, вести здоровый образ жизни, укреплять иммунитет и правильно питаться.
Профилактика бронхита
Профилактика легочных заболеваний – это комплексный и систематический процесс, цель которого – укрепить защитные силы организма и минимизировать воздействие факторов риска. Для этого необходимо в первую очередь отказаться от курения, защищать легкие от пыли, вредных химических соединений, слишком горячего или сухого воздуха. В рамках профилактики важно своевременно лечить хронические инфекции, предотвращать аллергические реакции и обязательно обращаться к врачу при первых признаках заболевания, проходить ежегодную вакцинацию от гриппа и пневмонии.
Неотложная терапия бронхиальной астмы у детей
По данным эпидемиологических исследований распространенность бронхиальной астмы среди детей в России составляет от 5,6 до 12,1% [1]. Бронхиальная астма ведет к снижению качества жизни больных, может быть причиной инвалидизации детей. Выраженные обостре
По данным эпидемиологических исследований распространенность бронхиальной астмы среди детей в России составляет от 5,6 до 12,1% [1]. Бронхиальная астма ведет к снижению качества жизни больных, может быть причиной инвалидизации детей. Выраженные обострения этого заболевания представляют определенную угрозу для их жизни. Своевременное проведение в этом периоде астмы адекватной состоянию больных терапии позволяет добиться восстановления бронхиальной проходимости и предотвратить развитие осложнений болезни.
Возникновение обострений бронхиальной астмы у детей обусловливается обструкцией бронхов, связанной с усилением воспаления слизистой оболочки бронхов, бронхоспазмом, скоплением мокроты в просвете бронхов. Наиболее частой причиной развития обострений бронхиальной астмы у детей является предрасположеность к аллергии, острые респираторные вирусные и бактериальные инфекции. Приступ бронхиальной астмы, как проявление ее обострения, характеризуется возникновением затрудненного свистящего дыхания, сопровождаемого удлиненным выдохом; кашля, ощущения заложенности в груди. При легком приступе бронхиальной астмы общее состояние больных обычно не нарушено. В легких прослушивается небольшое количество свистящих хрипов, отмечается небольшое удлинение выдоха, при этом одышка незначительна, а втяжение уступчивых мест грудной клетки едва заметно. В случаях приступа бронхиальной астмы средней тяжести у больных по всему полю легких прослушиваются свистящие хрипы, выявляется втяжение уступчивых мест грудной клетки, продолжительность выдоха в два раза превышает продолжительность вдоха, частота дыхания увеличивается на 50%. При осмотре ребенка над легкими обнаруживается коробочный оттенок перкуторного звука, отмечается тахикардия, нарушение общего состояния. Больные нередко принимают вынужденное положение сидя. Тяжелый приступ бронхиальной астмы характеризуется возникновением признаков дыхательной недостаточности в виде цианоза носогубного треугольника, крыльев носа, мочек ушей. Вследствие выраженного нарушения бронхиальной проходимости свистящие хрипы прослушиваются как при вдохе, так и при выдохе. Наблюдается заметное втяжение уступчивых мест грудной клетки, выраженное удлинение выдоха, превышающее по продолжительности вдох более чем в два раза, число дыханий увеличивается более чем на 50%. У больных обнаруживается тенденция к повышению артериального давления, отмечается выраженная тахикардия.
Обострение бронхиальной астмы у некоторых детей носит пролонгированный характер в виде астматического состояния (Status asthmaticus). Основной причиной его развития является несвоевременное и неадекватное состоянию больного лечение. Другими причинами астматического состояния могут быть контакт больного с причинно-значимыми аллергенами, наслоение острого респираторного заболевания, воздействие ирритантов, необоснованно быстрая отмена или снижение дозы глюкокортикостероидов, бронхиальная инфекция [2]. Причиной возникновения тяжелых обострений бронхиальной астмы у детей также могут быть резкое ухудшение экологической ситуации за счет загрязнения воздушной среды химическими соединениями, изменение метеоситуации.
Критериями астматического состояния являются следующие клинические признаки: наличие некупирующегося приступа бронхиальной астмы более 6–8 часов, неэффективность лечения ингаляционными бронхоспазмолитическими препаратами симпатомиметического ряда, нарушение дренажной функции легких (неотхождение мокроты), наличие признаков дыхательной недостаточности.
Стадия относительной компенсации астматического состояния характеризуется клинической картиной затянувшегося тяжелого приступа бронхиальной астмы, сопровождающегося гипоксемией (PaO2 55–60 мм рт. ст.), нередко гиперкапнией (PaCO2 60–65 мм рт. ст.), и респираторным алкалозом. У некоторых детей обнаруживается респираторный или метаболический ацидоз.
В стадии нарастающей дыхательной недостаточности, характеризуемой возникновением синдрома молчания в легких, при астматическом состоянии вследствие тотальной обструкции бронхов отмечается ослабление, а в последующем исчезновение дыхательных шумов, вначале в отдельных сегментах легких, затем в долях его и в целом легком. Развивается диффузный цианоз, появляются признаки сердечно-сосудистой недостаточности с падением артериального давления. Обнаруживается гипоксемия (PaCO2 50–55 мм рт. ст.), гиперкапния (PaCO2 65–75 мм рт. ст.), метаболический ацидоз.
В случаях продолжающегося ухудшения состояния больных может развиться глубокая дыхательная недостаточность, характеризующаяся отсутствием дыхательных шумов в легких, адинамией, последующей потерей сознания и судорогами, возникновением асфиксии.
При тяжелых обострениях бронхиальной астмы признаками выраженной дыхательной недостаточности, несущей угрозу жизни больного, являются:
Более быстрое развитие приступа астматического удушья отмечается в случаях, когда он является одним из проявлений системной аллергической реакции.
Терапию обострений бронхиальной астмы проводят с учетом тяжести и характера осуществлявшегося лечения. При сборе данных анамнеза выясняют причины, вызвавшие обострение болезни, препараты, ранее использовавшиеся для снятия обострений, применялись ли в этих целях глюкокортикостероиды. Оценку состояния больного бронхиальной астмой проводят на основании осмотра, исследования легочных функций. При тяжелых обострениях астмы целесообразно проведение рентгеновского исследования легких, определение уровня газов крови.
Объективную информацию о выраженности обструкции бронхов дает определение пиковой скорости выдоха, падение которой при бронхиальной астме находится в прямой зависимости от тяжести развернувшегося обострения бронхиальной астмы. Величины пиковой скорости выдоха в пределах от 50 до 80% свидетельствуют об умеренно выраженных или легкой степени нарушениях бронхиальной проходимости. Показатели пиковой скорости выдоха менее 50% от должных значений указывают на развитие тяжелого обострения бронхиальной астмы.
Полезным в оценке состояния больного может быть определение насыщения кислородом крови. Снижение насыщения кислородом крови менее 92% свидетельствует о наличии у больного тяжелого обострения бронхиальной астмы. Выявление при исследовании капиллярной или артериальной крови гипоксемии и гиперкапнии свидетельствует о развитии у больного тяжелой обструкции бронхов. При тяжелых обострениях бронхиальной астмы целесообразно проведение рентгенографического исследования легких, при котором иногда выявляют ателектаз, пневмомедиастинум, воспалительный процесс в легких.
Для лечения обострений бронхиальной астмы в настоящее время используются бронхоспазмолитики (β2-адреномиметики, М-холиноблокаторы, препараты теофиллина, комбинированные бронхоспазмолитические препараты), глюкокортикостероиды (системные, ингаляционные) и муколитические средства (ацетилцистеин, амброксол и др.).
Для оказания неотложной помощи при бронхиальной астме у всех больных используются бронхоспазмолитики. β2-адреномиметики — сальбутамол (Вентолин, Сальбен), фенотерол (Беротек), тербуталин (Бриканил), кленбутерол (Спиропент), избирательно стимулируя β2-адренорецепторы, обладают мощным быстро наступающим бронходилатирующим действием.
Выраженным бронходилатирующим действием обладают блокаторы М-холинорецепторов, снижающие влияние парасимпатической нервной системы и в связи с этим дающие эффект расслабления гладкой мускулатуры бронхов. Препарат этой группы бронходилататоров ипратропиум бромид (Атровент) при ингаляционном применении оказывает бронхоспазмолитический эффект через 30 минут с достижением его максимума через 1,5–2 часа.
Сочетанное применение антихолинергических средств и β2-агонистов в виде препарата «Беродуал» для ингаляционного введения дает более выраженный терапевтический эффект, чем изолированное применение Беротека.
Бронходилатирующее действие препаратов метилксантинового ряда, в том числе Эуфиллина, связано с их способностью блокировать рецепторы аденозина и тем самым воздействовать на пуринергическую тормозящую систему, усиливать синтез и секрецию эндогенных катехоламинов в коре надпочечников. Препараты теофиллинового ряда стимулируют дыхание и сердечно-сосудистую систему, снижают давление в малом круге кровообращения.
Глюкокортикостероиды, оказывая выраженное противовоспалительное и иммунодепрессивное действие, уменьшая отек слизистой оболочки бронхов и секреторную активность бронхиальных желез, являются эффективными средствами лечения детей с острой бронхиальной астмой.
Муколитические средства (ацетилцистеин, карбоцистеин, амброксол) могут назначаться детям с бронхиальной астмой для облегчения откашливания мокроты в связи с их способностью снижать ее вязкость.
Первичная помощь на амбулаторном этапе детям с легким и среднетяжелым обострением бронхиальной астмы включает проведение следующих лечебных мероприятий:
В табл. представлены подходы к выбору типа ингалятора для детей с бронхиальной астмой с учетом эффективности доставки препарата, экономической эффективности, безопасности, простоты и удобства применения.
Дозированные аэрозольные ингаляторы (Ветолин, Саламол Эко, Саламол Эко легкое дыхание) содержат в 1 ингаляционной дозе 100 мкг сальбутамола. При легком и среднетяжелом обострении бронхиальной астмы они назначаются по 2 ингаляционных дозы на прием с интервалом между ингаляциями в 2 минуты. Содержащий сальбутамол порошковый дозированный ингалятор имеет в 1 ингаляционной дозе 200 мкг препарата, детям его назначают по 1 ингаляционной дозе на прием.
Дозированный аэрозольный ингалятор на основе Беродуала содержит в 1 ингаляционной дозе 50 мкг фенотерола и 20 мг ипратропиума бромида, детям старше 6 лет Беродуал назначается по 2 ингаляционные дозы на прием.
Введение β2-агонистов в виде дозированных аэрозолей наиболее эффективно для детей старше 7 лет, способных в должной мере овладевать техникой пользования ингалятором. Для детей 3–7 лет и младшего возраста эффективно лечение дозированными аэрозолями β2-агонистов с помошью спейсеров. Введение с помощью ингаляторов пудры бронхоспазмолитиков наиболее эффективно для детей 3–7 лет. Введение растворов b2-агонистов при помощи небулайзеров чаще проводят детям младшего возраста и больным с тяжелыми обострениями бронхиальной астмы, когда они из-за тяжести состояния не могут осуществить должным образом ингалирование препарата.
Для проведения небулайзерной терапии детям с обострениями бронхиальной астмы наиболее часто используют растворы Вентолина и Беродуала.
Вентолин выпускается в пластиковых ампулах по 2,5 мл, содержащих 2,5 мг сальбутамола сульфата. При легком приступе бронхиальной астмы разовая доза составляет 0,1 мг (или 0,02 мл) на 1 кг массы тела, при среднетяжелом приступе астмы — 0,15 мг (0,03 мл/кг). При тяжелом приступе бронхиальной астмы Вентолин назначают по 0,15 мг или 0,03 мл на 1 кг массы тела с интервалом между ингаляциями препарата 20 минут. Длительная (в течение 24–48 часов и более) терапия Вентолином через небулайзер проводится в дозе 0,15 мг/кг каждые 4–6 часов.
Беродуал для ингаляций через небулайзер назначается детям с бронхиальной астмой до 6 лет в дозе 0,5 мл (10 капель), от 6 до 14 лет — 0,5–1 мл (10–20 капель). Разовая доза Беродуала ингалируется через небулайзер в 2–4 мл физиологического раствора.
Небулайзерная терапия Беродуалом по сравнению с проводимым лечением Вентолином более эффективна при обострениях бронхиальной астмы, вызванных острой респираторной вирусной инфекцией, воздействием химических поллютантов.
У детей с нетяжелым обострением бронхиальной астмы возможно пероральное применение бронхоспазмолитиков.
Сальбутамол (Вентолин) детям в возрасте от 2 до 6 лет назначают внутрь 3–4 раза в сутки в дозе 0,5–2 мг, от 6 до 12 лет — 2 мг, старше 12 лет — 2–4 мг.
Тербуталин (Бриканил) детям в возрасте 3–7 лет назначают внутрь 2–3 раза в сутки в дозе 0,65–1,25 мг, от 7 до 15 лет — в дозе 1,25 мг.
Кленбутерол назначают внутрь в суточной дозе 2 мкг на 1 кг массы тела, суточную дозу распределяют на 3–4 приема.
Эуфиллин назначают в дозе 4 мг/кг массы тела 3–4 раза в сутки.
Терапия тяжелых обострений бронхиальной астмы у детей должна проводиться в условиях стационара.
Факторами высокого риска развития тяжелых обострений бронхиальной астмы у детей являются:
Развивающиеся при тяжелом обострении бронхиальной астмы выраженная одышка, тахикардия, участие в акте дыхания вспомогательной дыхательной мускулатуры, появление признаков, угрожающих жизни больного (цианоза, синдрома молчания в легких, ослабления дыхания, общей слабости, падения пиковой скорости выдоха (ПСВ)
И. И. Балаболкин, доктор медицинских наук, профессор, член-корреспондент РАМН
НЦЗД РАМН, Москваф
Оказание скорой медицинской помощи при острых аллергических заболеваниях
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
к.м.н. И.В. Сидоренко, профессор И.С. Элькис,
к.м.н. А.В. Тополянский, профессор А.Л. Верткин
Научный Центр здоровья детей РАМН, Москва
ММА имени И.М. Сеченова
МГМСУ им. Н.А. Семашко
Станция скорой и неотложной медицинской помощи, Москва
Национальное научно-практическое общество скорой медицинской помощи, Москва
П о данным Национального научно–практического общества скорой медицинской помощи, за последние 3 года число вызовов по поводу острых аллергических заболеваний в целом по РФ возросло на 18%. При этом их частота в разных регионах составляет от 1 до 5% всех случаев выездов бригад скорой медицинской помощи.
Основные причины возникновения и патогенез
Патогенез аллергических реакций изучен на сегодняшний день достаточно полно и подробно описан во многих отечественных и зарубежных монографиях по аллергологии и клинической иммунологии. В любом случае в ткани шокового органа или органа–«мишени», которым могут быть кожа, бронхи, желудочно–кишечный тракт и т.д., появляются признаки аллергического воспаления. Центральная роль в реализации этих иммунопатологических реакций принадлежит иммуноглобулинам класса Е (IgE), связывание которых с антигеном приводит к выбросу из тучных клеток медиаторов аллергии (гистамина, серотонина, цитокинов и др.).
Наиболее часто аллергические реакции развиваются при воздействии ингаляционных аллергенов жилищ, эпидермальных, пыльцевых, пищевых аллергенов, лекарственных средств, антигенов паразитов, а также при ужалении и укусах насекомых. Лекарственная аллергия наиболее часто развивается при применении анальгетиков, сульфаниламидов и антибиотиков из группы пенициллинов, реже цефалоспоринов. Кроме того, высока частота развития латексной аллергии.
Клиническая картина, классификация и диагностические критерии
С точки зрения оказания помощи и оценки прогноза острые аллергические заболевания можно классифицировать следующим образом (табл. 1):
Легкие – аллергический ринит (круглогодичный или сезонный), аллергический конъюнктивит (круглогодичный или сезонный), крапивница.
Средней тяжести и тяжелые – генерализованная крапивница, отек Квинке, острый стеноз гортани, среднетяжелое обострение бронхиальной астмы, анафилактический шок.
Наибольшую настороженность при оказании медицинской помощи на догоспитальном этапе должны вызывать прогностически неблагоприятные случаи развития у пациентов жизнеугрожающих состояний: тяжелый приступ астмы (status asthmaticus), анафилактический шок, отек Квинке в области гортани, острый стеноз гортани.
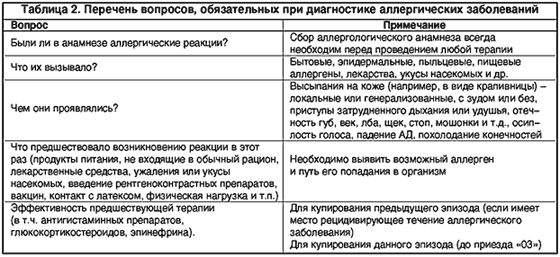
При анализе клинической картины аллергической реакции врач скорой медицинской помощи должен получить ответы на вопросы, представленные в таблице 2.
При начальном осмотре следует оценить наличие: стридора, диспноэ, свистящего дыхания, одышки или апноэ; гипотензии или синкопе; изменений на коже (высыпаний по типу крапивницы, отеков Квинке, гиперемии, зуда); гастроинтестинальных проявлений (тошноты, болей в животе, диареи); изменений сознания. Если у больного стридор, выраженная одышка, гипотензия, аритмия, судороги, потеря сознания или шок, то данное состояние рассматривается как жизнеугрожающее.
Лечение острых аллергических заболеваний
При острых аллергических заболеваниях на догоспитальном этапе неотложная терапия строится по направлениям:
Прекращение дальнейшего поступления в организм предполагаемого аллергена. Например, в случае реакции на лекарственный препарат, введенный парентерально или при укусе/ужалении насекомых – наложение жгута выше места инъекции или укуса на 25 мин (каждые 10 минут необходимо ослаблять жгут на 1–2 минуты); к месту инъекции или укуса – лед или грелка с холодной водой на 15 мин; обкалывание в 5–6 точках и инфильтрация места инъекции или укуса 0,3 – 0,5 мл 0,1% раствором эпинефрина с 4,5 мл изотонического раствора хлорида натрия.
Противоаллергическая терапия (антигистаминные препараты или глюкортикостероиды). Введение антигистаминных препаратов показано при аллергическом рините, аллергическом конъюнктивите, крапивинице. Терапию глюкокортикоидами (ГКС) проводят при анафилактическом шоке и при отеке Квинке (в последнем случае – препарат выбора): внутривенно вводят преднизолон (взрослым – 60–150 мг, детям – из расчета 2 мг на 1 кг массы тела). При генерализованной крапивнице или при сочетании крапивницы с отеком Квинке высокоэффективен бетаметазон 1–2 мл внутримышечно. При отеке Квинке для предупреждения влияния на ткани гистамина необходимо комбинировать антигистаминные препараты нового поколения (лоратадин) с глюкокортикоидами.
Симптоматическая терапия. При развитии бронхоспазма – показано ингаляционное введение b 2–агонистов и других бронхолитических и противовоспалительных препаратов через небулайзер. Коррекцию артериальной гипотонии и восполнение объема циркулирующей крови проводят с помощью введения солевых и коллоидных растворов (изотонического раствора хлорида натрия 500–1000 мл, гидроксиэтилированного крахмала 500 мл, полиглюкина 400 мл). Применять вазопрессорные амины (допамин 400 мг на 500 мл 5% глюкозы, норадреналин 0,2 – 2 мл на 500 мл 5% раствора глюкозы; доза титруется до достижения уровня систолического давления 90 мм рт.ст.) можно только после восполнения объема циркулирующей крови. При брадикардии возможно введение атропина в дозе 0,3–0,5 мг подкожно (при необходимости введение повторяют каждые 10 минут). При наличии цианоза, диспноэ, сухих хрипов показана также кислородотерапия.
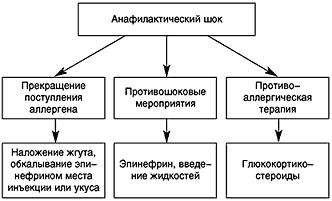
Противошоковые мероприятия (рис. 1). При анафилактическом шоке больного следует уложить (голова ниже ног), повернуть голову в сторону (во избежание аспирации рвотных масс), выдвинуть нижнюю челюсть, удалить съемные зубные протезы. Подкожно вводят эпинефрин в дозе 0,1 – 0,5 мл 0,1% раствора (препарат выбора), при необходимости инъекции повторяют каждые 20 минут в течение часа под контролем уровня АД. При нестабильной гемодинамике с развитием непосредственной угрозы для жизни возможно внутривенное введение эпинефрина. При этом 1 мл 0,1% раствора эпинефрина разводится в 100 мл изотонического раствора хлорида натрия и вводится с начальной скоростью 1 мкг/мин (1 мл в мин). При необходимости скорость может быть увеличена до 2–10 мкг/мин. Внутривенное введение эпинефрина проводится под контролем частоты сердечных сокращений, дыхания, уровня АД (систолическое артериальное давление необходимо поддерживать на уровне более 100 мм рт.ст. у взрослых и > 50 мм рт.ст. у детей). Лекарственные средства, применяемые при аллергических заболеваниях различной степени тяжести и их эффективность представлены в таблице 3.
Рис. 1. Алгоритм лечения анафилактического шока
Клиническая фармакология лекарственных средств, применяемых для лечения острых аллергических заболеваний
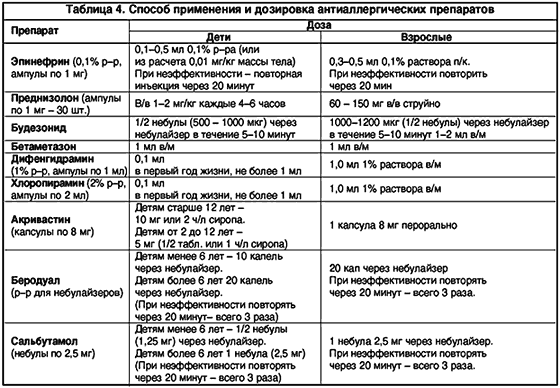
Способ применения и дозировка антиаллергических препаратов представлены в таблице 4.
Эпинефрин является прямым стимулятором a – и b –адренорецепторов, что обусловливает все его фармакодинамические эффекты. Механизм противоаллергического действия реализуется:
Способ применения и дозировка антиаллергических препаратов представлены в таблице 4.Эпинефрин является прямым стимулятором – и –адренорецепторов, что обусловливает все его фармакодинамические эффекты. Механизм противоаллергического действия реализуется:
• стимуляцией a –адренорецепторов, сужением сосудов органов брюшной полости, кожи, слизистых оболочек, повышением артериального давления;
• положительным инотропным действием (увеличивается сила сердечных сокращений за счет стимуляции b 1–адренорецепторов сердца);
• стимуляцией b 2–адренорецепторов бронхов (купирование бронхоспазма);
• подавлением дегрануляции тучных клеток и базофилов (за счет стимуляции внутриклеточной цАМФ).
При парентеральном введении препарат действует непродолжительно (при внутривенном – 5 мин, при подкожном – до 30 мин), так как быстро метаболизируется в окончаниях симпатических нервов, в печени и других тканях с участием моноаминооксидазы (МАО) и катехол–О–метилтрансферазы (КОМТ).
Побочные эффекты: головокружение, тремор, слабость; сильное сердцебиение, тахикардия, различные аритмии (в том числе желудочковые), появление болей в области сердца; затруднение дыхания; увеличение потливости; чрезмерное повышение артериального давления; задержка мочи у мужчин, страдающих аденомой предстательной железы; повышение уровня сахара в крови у больных сахарным диабетом. Описаны также некрозы тканей при повторном подкожном введении в одно и то же место вследствие местного сужения сосудов.
Противопоказания: артериальная гипертензия; выраженный церебральный атеросклероз либо органическое поражение головного мозга; ишемическая болезнь сердца; гипертиреоз; закрытоугольная глаукома; сахарный диабет; гипертрофия предстательной железы; беременность. Однако даже при этих заболеваниях возможно назначение эпинефрина при анафилактическом шоке по жизненным показаниям и под строгим врачебным контролем.
Механизм противоаллергического действия глюкокортикоидов основан на следующих эффектах:
• иммунодепрессивное свойство (подавление роста и дифференцировки иммунных клеток – лимфоцитов, плазмоцитов, уменьшение продукции антител);
• предупреждение дегрануляции тучных клеток и выделения из них медиаторов аллергии;
• уменьшение проницаемости сосудов, повышение артериального давления, улучшение бронхиальной проходимости.
Для парентерального введения при проведении неотложной терапии на догоспитальном этапе применяется преднизолон. Для лечения бронхиальной астмы, аллергического ринита, аллергического конъюнктивита разработаны топические формы глюкокортикостероидов (флутиказон, будезонид). Побочные эффекты системных ГКС: артериальная гипертензия, возбуждение, аритмия, язвенные кровотечения. Побочные эффекты топических ГКС: осиплость голоса, нарушение микрофлоры с дальнейшим развитием кандидоза слизистых, при применении высоких доз – атрофия кожи, гинекомастия, прибавка массы тела и др. Противопоказания: язвенная болезнь желудка и 12–перстной кишки, тяжелая форма артериальной гипертензии, почечная недостаточность, повышенная чувствительность к глюкокортикоидам в анамнезе.
Бетаметазон – глюкокортикостероидный препарат, состоит из 2 мг динатрия фосфата и 5 мг дипропионата бетаметазона. Бетаметазона динатрия фосфат обеспечивает быстроту наступления эффекта. Пролонгированное действие обеспечивается за счет бетаметазона дипропионата. Препарат оказывает иммунодепрессивное, противоаллергическое, десенсибилизирующее и противошоковое действие. Бетаметазон биотрансформируется в печени. Доза препарата зависит от степени тяжести заболевания и клинической картины течения. Применяется для лечения острых аллергических заболеваний в виде внутримышечных инъекций по 1–2 мл. При однократном введении существенных побочных действий не отмечено.
Антигистаминные средства (блокаторы Н1–гистаминовых рецепторов)
Существует несколько классификаций антигистаминных препаратов. Согласно одной их них, выделяют препараты первого, второго и третьего поколения (при этом до сих пор дискутируется вопрос о принадлежности разных препаратов ко 2–му или 3–му поколению). В другой, более популярной среди клиницистов классификации, выделяют классические антигистаминные препараты, например, хлоропирамин, и препараты нового поколения (акривастин, фексофенадин, лоратадин и др.)
Необходимо отметить, что для классических антигистаминных препаратов, в отличие от препаратов нового поколения, характерной является короткая продолжительность действия при относительно быстром наступлении клинического эффекта. Многие из них имеются в парентеральных формах. Все это определяет широкое использование классических антигистаминных средств и в настоящее время.
Хлоропирамин – один из широко применяемых классических антигистаминных препаратов. Обладает значительной антигистаминной активностью, периферическим антихолинергическим и умеренным спазмолитическим действием. При приеме внутрь быстро и полностью абсорбируется из ЖКТ. Максимальная концентрация в крови достигается в течение первых 2 часов, терапевтический уровень концентрации сохраняется 4–6 часов. Эффективен в большинстве случаев для лечения сезонного и круглогодичного аллергического ринита и конъюнктивита, крапивницы, атопического дерматита, экземы; в парентеральной форме – для лечения острых аллергических заболеваний, требующих неотложной помощи. Обладает широким диапазоном используемых терапевтических доз. Не накапливается в сыворотке крови, поэтому не вызывает передозировки при длительном применении. Для препарата характерно быстрое наступление эффекта и небольшая продолжительность (в том числе и побочного) действия. Может комбинироваться с другими Н1–блокаторами с целью увеличения продолжительности противоаллергического действия. Выпускается в таблетках и в ампулах для внутримышечного и внутривенного введения.
Антигистаминные препараты нового поколения лишены кардиотоксического действия, конкурентно влияют на гистамин, не метаболизируются печенью (например, фармакокинетика акривастина не меняется даже у больных с нарушенными функциями печени и почек) и не вызывают тахифилаксии.
Акривастин – препарат с высокой антигистаминной активностью при минимально выраженном седативном и антихолинергическом действии. Особенностью его фармакокинетики является низкий уровень метаболизма и отсутствие кумуляции и привыкания. Акривастин предпочтителен в случае, когда нет необходимости постоянного противоаллергического лечения. Желатиновая капсула быстро всасывается в желудке, обеспечивая быстрое наступление эффекта. Препарат обладает коротким периодом действия, что позволяет использовать гибкий режим дозирования. Нет кардиотоксического действия. Селективно влияя на Н1–рецепторы, не раздражает слизистую желудка. Нет воздействия на Н2–рецепторы.
Лоратадин – антигистаминный препарат нового поколения безрецептурного отпуска.
Показания к применению: аллергический ринит (сезонный и круглогодичный), аллергический конъюнктивит, крапивница, генерализованная крапивница, отек Квинке, аллергические реакции на укусы насекомых, зудящие дерматозы (контактные аллергодерматиты, хронические экземы).
У препарата отсутствуют такие побочные эффекты, как сонливость, сухость во рту, головная боль, головокружение.
Бронхоспазмолитики: b 2–агонисты короткого действия и холинолитики
Беродуал – комбинированный бронхоспазмолитический препарат, содержащий два бронхорасширяющих вещества: фенотерол ( b 2–агонист) и ипратропиум бромид (холинолитик). Одна доза беродуала содержит 0,05 мг фенотерола и 0,02 мг ипратропиума бромида.
Сальбутамол – селективный агонист b 2– адренорецепторов. Бронхорасширяющий эффект сальбутамола наступает через 4–5 минут. Действие препарата постепенно возрастает до своего максимума к 40–60 минуте. Период полувыведения 3–4 часа, продолжительность действия – 4–5 часов.
Способ применения: с помощью небулайзера; небулы по 2,5 мл, содержащая 2,5 мг сальбутамола в физиологическом растворе. Назначаются 1–2 небулы (2,5–5,0 мг) на ингаляцию в неразбавленном виде. Если улучшения не наступает, проводят повторные ингаляции по 2,5 мг каждые 20 мин. в течение часа.
Типичные ошибки в применении лекарственных средств при лечении острых аллергических заболеваний на догоспитальном этапе
• Изолированное назначение Н1–гистаминовых блокаторов при тяжелых аллергических реакциях, равно как и при бронхообструктивном синдроме, не имеет самостоятельного значения и на догоспитальном этапе лишь приводит к неоправданной потере времени.
• Использование дипразина опасно еще и усугублением гипотонии.
• Позднее назначение ГКС; необоснованное применение малых доз ГКС.
• Использование отдельных препаратов, не показанных для лечения аллергических заболеваний (глюконата кальция, хлористого кальция и пр.).
• Наличие в табеле оснащения бригад скорой помощи препаратов однонаправленного действия экономически неоправданно.
• Неиспользование топических ГКС и b 2–агонистов при аллергическом стенозе гортани и бронхоспазме.
Больные с тяжелыми аллергическими заболеваниями должны быть обязательно госпитализированы. При легких аллергических заболеваниях вопрос о госпитализации решается в каждом случае индивидуально.
ПРИЛОЖЕНИЕ
Аллергический стеноз верхних дыхательных путей у детей
Основные причины возникновения и патогенез
Синдром обструкции верхних дыхательных путей (круп, острый стенозирующий ларинготрахеит) у детей – одна из частых причин обращения за неотложной помощью. Выделяют острый аллергический стеноз гортани и стеноз, развивающийся на фоне ОРВИ.
Основной причиной развития аллергического стеноза верхних дыхательных путей с преимущественной локализацией процесса в области гортани является сенсибилизация организма к пищевым и лекарственным аллергенам, а также к аллергенам микроклещей домашней пыли (Dermatophagoides pteronyssinus и Dermatophagoides farinae), животных и др.
Острый аллергический стеноз верхних дыхательных путей чаще наблюдается у детей с наследственным предрасположением к аллергии. Развитию крупа нередко предшествует появление симптомов кожной и респираторной аллергии. Благоприятствуют возникновению аллергического стеноза гортани и такие анатомические особенности этого органа у детей, как мягкость хрящевого скелета, короткое и узкое преддверье и высоко расположенная гортань, наличие нежной, богатой клеточными элементами слизистой оболочки и рыхлого, с обильной сосудистой сетью и большим количеством тучных клеток подслизистого слоя. Указанные особенности строения слизистой и подслизистой оболочек особенно характерны для окруженного плотным перстневидным хрящом участка гортани. Эта область проецируется на подсвязочное пространство, в ней и развивается у детей максимально выраженный отек. Чаще круп развивается у детей в возрасте от 6 месяцев до 3 лет, при этом мальчики страдают им в 3–4 раза чаще, чем девочки.
Патогенетическую основу аллергического стеноза верхних дыхательных путей составляют IgЕ–опосредуемые аллергические реакции, вызывающие развитие в слизистой оболочке гортани воспаления в виде отека, гиперсекреции слизи, спазма гладкой мускулатуры верхних дыхательных путей; у отдельных больных возникает также бронхоспазм. Развитие острого стенозирующего ларинготрахеита может быть связано и с воздействием вирусной инфекции, химических поллютантов, изменением метеоситуации.
Клиническая картина, классификация и диагностические критерии
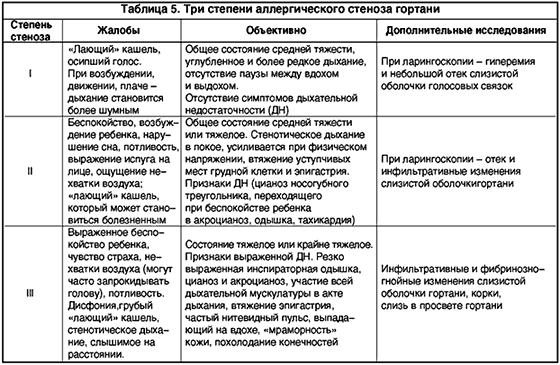
Острый стеноз гортани является причиной развития дыхательной недостаточности и нарушения общего состояния ребенка. Различают три степени стеноза в зависимости от выраженности сужения гортани:
I степень стеноза гортани – компенсированный стеноз;
II степень – субкомпенсированный стеноз;
III степень – декомпенсированный стеноз (табл. 5).
У детей с аллергическим стенозом гортани обычно выявляют отягощенную аллергическими реакциями и заболеваниями наследственность, нередко у них отмечаются также проявления атопического дерматита, пищевой и лекарственной аллергии. Для этого варианта крупа характерно внезапное развитие стеноза «на фоне полного здоровья», при отсутствии катаральных явлений, нормальной температуре тела, а также сравнительно быстрое купирование симптомов болезни при назначении адекватной терапии. У ряда детей одновременно с проявлениями аллергического стеноза гортани развивается бронхообструктивный синдром.
Острый стеноз гортани, развивающийся на фоне острой респираторной инфекции, характеризуется более постепенным началом болезни, возникновением стеноза на фоне катаральных явлений со стороны верхних дыхательных путей, повышением температуры, развитием симптомов интоксикации, воспалительных изменений в общем анализе крови.
Стеноз гортани необходимо дифференцировать с дифтерией гортани, инородным телом дыхательных путей, обструктивным бронхитом, заглоточным абсцессом, бронхиальной астмой, коклюшем, пневмонией с проявлениями дыхательной недостаточности.
Лечение острого стеноза гортани
Дети с острым стенозом гортани подлежат обязательной госпитализации. Проводимая при остром стенозе гортани терапия должны быть патогенетической и направленной на восстановление воздушной проходимости верхних дыхательных путей. Лечение проводится с учетом выраженности стеноза гортани, начинается бригадами СМП на вызове, продолжается по пути следования в стационар. Время оказания догоспитальной помощи больному не должно превышать 60 минут.
Для лечения острого стеноза гортани в компенсированной стадии (I степень) на догоспитальном этапе используются ингаляции глюкокортикостероидов (будезонида через небулайзер в дозе 0,25 мг, при неэффективности или отсутствии небулайзеров применяются антигистаминные препараты: в/м (хлоропирамин, 2%–ный раствор, 0,1 мл в первый год жизни) или перорально (для детей от 12 лет – акривастин (7 мг, капсула) или лоратадин 10 мг (1 табл. или 2 чайных ложки сиропа).
Терапия острого стеноза гортани в стадии неполной компенсации (II степень) начинается с ингаляций глюкокортикостероидов через небулайзер в дозе 0,5 мг. При неэффективности проводят повторные ингаляции будезонида в той же дозе через небулайзер с интервалом в 20 минут (максимально 3 раза).
При отсутствии небулайзеров применяются антигистаминные препараты (хлоропирамин в/м), системные глюкокортикостероиды (преднизолон из расчета 2 мг/кг). При недостаточном эффекте дополнительно назначается подкожное введение 0,1 % раствора эпинефрина из расчета 0,01 мг/кг массы тела.
Стеноз гортани III степени протекает с проявлениями дыхательной и сердечно–сосудистой недостаточности, нарушением метаболических процессов, признаками токсикоза, что обусловливает необходимость немедленной госпитализации. На догоспитальном этапе лечение стеноза гортани III степени также начинается с ингаляций глюкокортикостероидов через небулайзер в дозе 1 мг.
При возникновении бронхообструктивного синдрома лечение проводится растворами b 2–агонистов короткого действия (беродуала по 10–20 капель детям до 6 лет или сальбутамола – 1/2–1 небула детям старше 6 лет) через небулайзер.