живые аденовирусы человека что это простыми словами
Иммунолог объяснила, зачем вакцине аденовирус и насколько он опасен
Ученый-иммунолог из парижского Университета Пастера Дарья Карташева-Эберц объяснила, как вирусы ведут себя в организме, что происходит при вакцинации и почему аденовирус из «Спутника V» на самом деле не встраивается в человеческую ДНК.
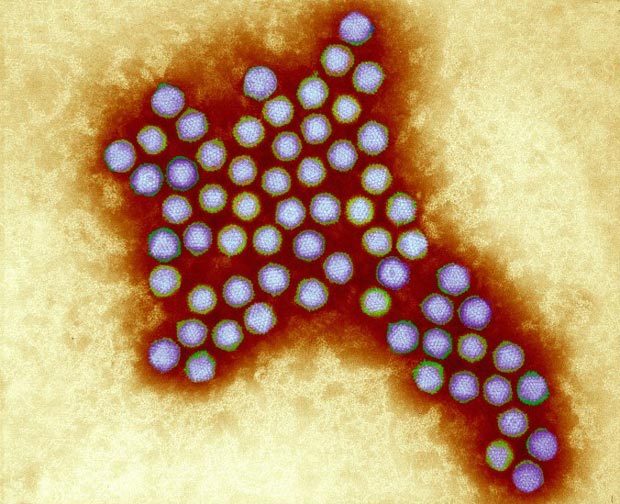
Все известные человеку вирусы делятся на ДНК- и РНК-содержащие, говорит эксперт. Аденовирус как раз из первых, его генетический материал представлен двойной цепочкой ДНК. Проникнув в клетку, вирус пробирается к ядру. Внутрь ядра входит только цепочка ДНК и несколько сцепленных с ней вирусных белков.
«В ядре вирусная ДНК начинает переписывать каждый пункт своей инструкции на отдельные листочки, что мы называем вирусные РНК. Вирусные РНК выходят из ядра клетки и уже в цитоплазме с помощью клеточного «завода» по производству белков начинают готовить белки вируса по РНК-рецептам. Как только они готовы, вирусные белки бегут обратно в ядро», — пишет иммунолог в своем блоге в Instagram.
В это же время, отмечает эксперт, ДНК вируса, помимо переписывания инструкции в виде РНК, еще удваивается, утраивается, то есть реплицируется. Прибежавшие белки помогают репликации, но также окружают новые копии ДНК, формируя новую вирусную частицу. В итоге клетка разрушается и частица высвобождается.
По словам Карташевой-Эберц, аденовирусы не способны «резать» человеческую ДНК, а также не имеют фермента для встраивания. «Природа этого не предусмотрела для аденовирусов», — подчеркнула иммунолог.
У аденовирусов, используемых в «Спутнике V», также вырезана часть ДНК, которая отвечает за репликацию. Попадая в клетку, вирус переписывает рецептуру в РНК, а далее производит белки, но размножения и сборки не происходит. Вместо этого ученые вставили рецепт по приготовлению S-белка коронавируса. Когда такой аденовирус поможет создать его белок, внутренние клеточные сенсоры почувствуют, что внедрился чужеродный агент, и начнут с ним бороться.
Аденовирус в вакцине — это просто транспорт по доставке рецепта белка коронавируса в клетку, чтобы иммунная система увидела его и начала «собирать армию». А сам аденовирус будет в итоге уничтожен иммунной системой после подачи сигнала SOS, заключила ученый.
Что такое аденовирус
Что если вам скажут, будто одна и та же группа вирусов может вызывать все на свете заболевания, – от банальной простуды до инфекций мочевого пузыря? Несколько странно, не так ли? И определенно это не та новость, которую хотелось бы услышать в преддверии гриппозно-простудного сезона (за что просим прощения).
Однако это соответствует действительности: представители группы патогенов, называемых аденовирусами, в некоторых случаях могут быть смертельно опасны. Корреспондент сайта « Health » обратился к эксперту в области инфекционных болезней за разъяснениями вопросов о том, что в сущности представляют собой аденовирусы, какие симптомы они могут вызывать и как можно вылечиться.
И вот что необходимо знать.
Согласно информационным материалам Центров по контролю и профилактике заболеваний (CDC), аденовирусами называют группу обычных вирусов, способных вызывать широкий спектр заболеваний, включая обычную простуду, желудочный грипп, ангину, бронхит, диарею, эпидемический конъюнктивит, лихорадку, – словом, все заболевания, протекающие с умеренно выраженной симптоматикой и, как правило, поддающиеся лечению в домашних условиях. Однако некоторые штаммы аденовирусов приводят к более серьезным проблемам, например, к инфекциям мочевых путей или воспалению легких.
Поскольку аденовирусы чрезвычайно разнообразны, вызываемая ими симптоматика также варьирует очень широко. В основном, развиваются респираторные заболевания и конъюнктивиты. Это означает, что именно аденовирусы «виновны» в большинстве регистрируемых случаев кашля, хрипов и зудящих красных глаз.
Отличие аденовирусов от прочих вирусов (например, от вируса гриппа) заключается в том, что первые не обязательно предпочитают холодное время года. «Аденовирусные инфекции наблюдаются круглогодично, – говорит Фрэнк Эспер, доктор медицины, педиатр, специализирующийся на инфекционных болезнях в Кливлендской клинике. – Лето нравится аденовирусу не меньше, чем зима».
Наиболее типичный путь распространения аденовирусной инфекции – через прямой контакт, например, прикосновение, кашель, чихание, рукопожатие, или же через прикосновение к зараженной поверхности с последующим касанием собственного рта, носа, глаз. Реже аденовирусы распространяются через инфицированный кал (при смене подгузника больному ребенку, например) или через воду (в общественных бассейнах и т.п.).
«Могут ли аденовирусы представлять опасность для жизни? – В некоторых случаях, да. Восемнадцатилетняя студентка колледжа при Университете Мэриленда умерла от аденовирусной инфекции во время эпидемической вспышки 2018 года, когда заболело 40 студентов и 15 из них пришлось госпитализировать».
«Как правило, – продолжает доктор Эспер, – под угрозой оказываются лица с ослабленной иммунной системой. Если у вас практически нет иммунитета, тогда аденовирус становится действительно серьезной проблемой».
Именно это случилось с погибшей девушкой, которая, как сообщает « Washington Post «, страдала и боролась с болезнью Крона, – разновидностью хронического кишечного воспаления, – постоянно принимая поддерживающие препараты в связи с данным заболеванием (определенные группы медикаментов, – используемые, в частности, для контроля болезни Крона и лечения рака, – в индивидуальных случаях могут стать причиной иммунодефицитного состояния).
Впрочем, аденовирусы могут становиться опасными даже для лиц с нормально функционирующей иммунной системой. Случится это или нет, зависит от конкретных осложнений аденовирусной инфекции. «Скажем, вирусный миокардит, т.е. воспаление сердечной мышцы, – объясняет доктор Эспер, – может развиться и у иммунокомпетентного человека, и это осложнение может стать фатальным».
«Существует ли лечение от аденовирусов? – Нет, специфическая терапия аденовирусных инфекций пока не разработана, и применяемые в этих случаях безрецептурные лекарства служат лишь для облегчения симптоматики (т.е. для устранения болей или лихорадки, снижения температуры и т.д.)».
В связи с этим приходится повторять, что лучшим средством против аденовирусных инфекций является их профилактика. Это означает частую и тщательную гигиену рук, исключение случаев употребления пищи или напитков из общей с контагиозным человеком посуды, и избегание любых людей, кто открыто кашляет или чихает (возможно, стоило бы им напомнить: хотя бы используйте локоть, пожалуйста).
В экстремальных случаях применяется препарат под названием цидофовир, но, опять же, его назначают крайне редко. По словам Ф.Эспера, «препарат очень токсичен, он сам по себе может стать причиной тяжелого состояния, например, почечной недостаточности. Обычно мы воздерживаемся от этиотропного лечения аденовирусов и прибегаем к выжидательной тактике. Больной должен быть в очень тяжелом состоянии, чтобы пришлось назначать эти медикаменты».
В общем и целом, для здорового человека аденовирусы не должны составлять особую проблему, – тем не менее, будет разумным соблюдать все меры предосторожности и, если вы все же заболели, защитить близких людей с помощью санитарно-гигиенического режима.
Ученый из МФТИ раскрыл процесс создания вакцины от коронавируса
Как создают вакцину от коронавируса?
Об эксперте: Павел Волчков — кандидат биологических наук, вирусолог, генетик, заведующий Лабораторией геномной инженерии Московского физико-технического института (МФТИ).
Существует много разных подходов к созданию вакцины от COVID-19. Она может быть вирусной, инактивированной, векторной, на основе нуклеиновых кислот. Какая из них окажется самой эффективной — пока никто точно не знает. Если вы разработчик, то можете выбрать любую и принять участие в большой мировой гонке по созданию долгожданной прививки. А можете, как ученые из МФТИ, сознательно отказаться от возможных бенефитов и неспешно заняться разработкой экспериментальной вакцины нового типа.
Одни из самых популярных на сегодняшний день — это рекомбинантные или векторные вакцины. Они изготавливаются на основе вирусов-носителей или вирусных векторов. Как это работает? Вы берете какие-то вирусные частицы, «вычищаете» из них все патогенные составляющие и на их место вставляете нужные вам элементы — генетический материал вируса, против которого изготавливается вакцина. По такому принципу была создана прививка от вирусного гепатита B или ротавирусной инфекции. И по такому же принципу сегодня многие разработчики создают вакцину от COVID-19. В частности, в России векторную вакцину от коронавируса разработали в НИИ эпидемиологии и микробиологии имени Н.Ф. Гамалеи.
Павел Волчков:
«Чем хорош вирусный вектор? Он способен инфицировать клетки только один раз и не может размножаться в организме человека дальше. Такая особенность делает рекомбинантные вакцины довольно безопасными. При этом в качестве вирусного вектора можно использовать буквально любой вирус из библиотеки человеческих патогенов. Выбор зависит от того, для какого заболевания вы изготавливаете вакцину. Потому что одни вирусы лучше заражают мышцы, другие — легкие, третьи — центральную нервную систему. Например, та же вакцина Центра Гамалеи выполнена на аденовирусном векторе».
Аденовирусы — ДНК-вирусы. Относятся к группе острых респираторных вирусных инфекций (ОРВИ) и характеризуются поражением слизистых оболочек верхних дыхательных путей, конъюнктив, лимфоидной ткани. Большинство аденовирусных инфекций представляют собой легкую форму инфицирования. Существует семь видов аденовирусов человека (от А до G) и 57 серотипов. Подразделение на серотипы связано с различными способами заражения.
В качестве векторов для вакцин, аденовирусы применяются довольно давно. Эти вирусы хорошо изучены. Согласно данным сайта ClinicalTrials.gov, клинические испытания на людях успешно прошли или проходят более сотни различных вакцин на основе аденовирусных векторов.
Среди главных преимуществ этих вирусов — их естественный механизм взаимодействия с клетками человека. Они способны обеспечивать довольно длительную экспрессию антигена, а это успешно активирует врожденный иммунный ответ.
Антигены — это любые вещества, содержащиеся в микроорганизмах и других клетках (или выделяемые ими), которые несут в себе признаки генетически чужеродной информации, и которые потенциально могут быть распознаны иммунной системой организма.
Павел Волчков:
«При всех плюсах, у аденовирусов есть и ряд минусов. Первое — они обладают провоспалительным эффектом. То есть могут чрезмерно драйвить иммунную систему. Проще говоря — вызывать сильный иммунный ответ. Это один из возможных побочных эффектов вообще всех аденовирусных вакцин. Но есть еще один нюанс. Большинство аденовирусов — это естественные патогены человека. Многие из нас сталкивались в течение жизни с аденовирусными инфекциями. А что это значит? Что в крови у таких людей уже есть нейтрализирующие антитела к этому вирусу. Они могут связываться с компонентами вакцины и блокировать ее действие. Поэтому для некоторых из нас такая вакцина будет совершенно неэффективна».
Вакцина МФТИ: в чем инновация?
Поскольку у аденовирусных векторов есть существенные недостатки, ученые из МФТИ выбрали другие вирусы в качестве вектора — аденоассоциированные вирусы. Что любопытно, раньше никто в мире не использовал их в таком качестве.
Аденоассоциированные вирусы — мелкие ДНК-содержащие вирусы. Размер частиц 22-24 нм. Размножаются только в присутствии аденовирусов. Способны инфицировать клетки человека и некоторых других приматов. Аденоассоциированный вирус, по-видимому, не вызывает заболеваний у человека, поэтому провоцирует слабый иммунный ответ.
Один из плюсов аденоассоциированных вирусов — они давно и успешно используются в генной терапии. Сегодня зарегистрировано несколько лекарственных средств на их основе. Одно из самых нашумевших — Luxturna. Это первое генное лекарство, созданное для лечения наследственной слепоты, вызванной мутацией гена RPE65.
По аденоассоциированным вирусам также накоплена внушительная клиническая база. На сайте ClinicalTrials.gov можно увидеть, в каком количестве клинических экспериментов аденоассоциированные вирусы уже приняли участие. Это несколько сотен доклинических исследований и порядка 50 клинических экспериментов. Носитель хорошо охарактеризован и, что еще важнее, показана его безопасность. Все это делает аденоассоциированные вирусы весьма привлекательным кандидатом для создания вирусных векторов не только для генной терапии, но и для вакцин, уверены в Лаборатории геномной инженерии МФТИ.
Еще одной веской причиной создать вакцину на аденоассоциированном векторе стало то, что ученые из МФТИ уже давно придумывают, модифицируют и создают аденоассоциированные вирусы. На сегодняшний день в библиотеке МФТИ их более миллиона. Все они имеют разную специфичность и разные свойства. Что важно, к этим вирусам у человека не может быть иммунного ответа, который бы снизил эффективность вакцины. Поскольку все они созданы искусственно.
Павел Волчков:
«Мы с самого начала понимали, что сможем не только разработать вакцину, но и масштабировать ее производство. То есть произвести столько доз, сколько потребуется или столько, сколько захотим. В мире существует огромное количество аутсорсинговых компаний, которые по GMP сделают вам любое количество доз препарата.
Good Manufacturing Practice (GMP) — правила, которые устанавливают требования к организации производства и контроля качества лекарственных средств для медицинского и ветеринарного применения.
Поэтому с самого начала у нас было четкое понимание, что проблем с производством не будет. Как и проблем с лицензией на вирусный носитель. Это качественно отличает нашу лабораторию от многих других разработчиков вакцин в Российской Федерации. В современном мире все технологии так или иначе кому-то принадлежат, и аденовирусы, и прочие системы векторной доставки, аденоассоциированные в том числе. Живя по правилам свободного рынка, вы не можете просто взять и сделать вакцину на основе любого понравившегося вектора. Вы должны иметь разрешение от компании, которая обладает правами на технологию, либо владеет непосредственно интеллектуальной собственностью в области этого вектора. И тут у нас все хорошо — мы как раз владеем патентом по разработке аденоассоциированных вирусов. Нам не нужно просить ни у кого лицензию на производство данной вакцины, поскольку мы используем собственные же аденоассоциированные вирусы».
Вакцина МФТИ будет эффективна против разных штаммов SARS-CoV-2
Изначально ученые хотели разработать вакцину, которая бы вырабатывала иммунитет практически ко всем поверхностным белкам вируса SARS-CoV-2. А не только к S-белку, как это делают большинство разработчиков вакцин по всему миру (включая НИИ им. Гамалеи). Но в итоге разработчики остановились на конечном числе компонентов. Ими стали S-белок, Е-белок и М-белок.
Павел Волчков:
«По сути мы воплощаем идею совершенно нового типа вакцин — так называемых поливалентных вакцин. Это когда в одном препарате сразу несколько вирусных компонентов. Такой подход кажется нам крайне эффективным применительно к SARS-CoV-2. Ведь на самом деле это не один какой-то конкретный вирус, который распространился по планете. Если мы начнем секвенировать разные изоляты коронавируса, то они все будут отличаться друг от друга. Либо на одну аминокислотную замену, либо на несколько. Поливалентная вакцина как раз направлена на то, чтобы вырабатывать иммунный ответ не к одному поверхностному белку вируса, а сразу к нескольким. В том числе к консервативным поверхностным белкам, которые меньше остальных подвержены мутациям. Так наша вакцина поможет сформировать иммунитет к разным штаммам вируса SARS-CoV-2».
Если текущая разработка покажет свою эффективность и безопасность, ученые планируют пойти еще дальше и разработать вакцину, которая будет содержать не только различные компоненты SARS-CoV-2, но еще и вируса гриппа или других сезонных респираторных вирусов. То есть объединить в одной вакцине генетический материал от самых разных сезонных патогенов. По мнению ученых из МФТИ, такие ассемблированные, поливалентные вакцины могли бы готовить людей каждый сезон к новому остро-респираторному вирусному нашествию.
Что касается текущей разработки (вакцины от COVID-19), то на данный момент ее разработка завершена. Впереди подготовка к доклиническим испытаниям на китайских хомяках и приматах. Если они пройдут успешно, вакцину ожидают испытаниях на людях. Но торопиться и участвовать в текущей «вакцинной» гонке разработчики из МФТИ не собираются.
Павел Волчков:
«Дело в том, что в нашей вакцине слишком много новых компонентов. Несмотря на то, что аденоассоциированные вирусы используются в генной терапии, для создания вакцин их еще никто не применял. Спешка или сокращение сроков проведения доклинических и клинических исследований может обернуться ошибкой и поставить крест на такой многообещающей и перспективной платформе. Но это не значит, что сейчас мы создаем вакцину, что называется «в стол». Во-первых, когда она будет испытана, мы сможем ее продавать другим нуждающимся странам. Во-вторых, наша основная цель — получить опыт по созданию быстрых вакцин, который мы планируем применять в будущем. Как научная лаборатория мы можем проводить такие эксперименты — создавать платформу для вакцин совершенно нового типа. И если у нас все получится, то в следующий раз, когда в мире появится новость о новой вспышке заболевания, мы будем готовы пройти весь путь создания препарата гораздо быстрее, чем мы проходим его сейчас».
Массовая вакцинация от COVID-19 может не понадобиться?
Павел Волчков уверен, что сама по себе гонка по созданию вакцин от короновируса уже не имеет смысла. Он уверен, что к тому моменту, когда российские вакцины будут испытаны и наработаны для массовой вакцинации населения, потребность в них может отпасть. Ученый считает, что уже к осени мы все, так или иначе, переболеем COVID-19 и получим естественный иммунитет.
У этой оптимистичной гипотезы есть основания. Не так давно шведские ученые провели исследование и померяли иммунитет в шведской популяции. Измерялся и гуморальный иммунитет (то есть антитела в крови), и клеточный иммунитет. А именно Т-лимфоциты — так называемые клетки иммунной памяти, которые при повторной встрече с инфекцией «просыпаются» и активизируют иммунный ответ.
Исследование показало, что лишь у небольшой части шведов в крови присутствовали антитела, но примерно треть граждан имела ту самую клеточную память. Это говорит о том, что существенная часть популяции шведов в той или иной форме переболела COVID-19 или имела непродолжительный контакт с вирусом. В последнем случае большой продукции антител не происходит, но благодаря Т-лимфоцитам формируется иммунологическая память к COVID-19.
Павел Волчков:
«Согласно московской статистике, антитела к коронавирусу были определены в крови примерно у 20% жителей столицы. А это около 2 млн человек. Следуя логике шведского исследования, которому у меня лично нет причин не доверять, то скорее всего еще у 20% (а может и у 40% или даже 50-60%) людей уже есть клеточный иммунитет к COVID-19. Эти люди контактировали с небольшими дозами вируса, их иммунная система его детектировала и сформировала клетки памяти. Фактически, половина населения столицы естественным образом получила живую вакцину от COVID-19. Что примечательно, иммунитет, полученный в результате натуральной инфекции, оказывается более стойким, чем от гипотетической вакцины. Потому что в таком случае, иммунная система знакомится с полноценным вирусом (со всеми поверхностными белками), а не с его редуцированной версией, как это происходит при вакцинации. Я думаю, что такая ситуация с клеточным иммунитетом к COVID-19 обстоит не только в Москве, а во многих российских городах. То есть огромное количестве людей по всей России на самом деле уже имеет иммунитет к коронавирусной инфекции».
Крохотные курьеры: как аденоассоциированные вирусы спасают жизни
Крохотные курьеры: как аденоассоциированные вирусы спасают жизни
Авторы
Редакторы
Конкурс «Био/Мол/Текст»-2020/2021
Эта работа опубликована в номинации «Вирусы и микроорганизмы» конкурса «Био/Мол/Текст»-2020/2021.
Генеральный партнер конкурса — ежегодная биотехнологическая конференция BiotechClub, организованная международной инновационной биотехнологической компанией BIOCAD.
Спонсор конкурса — компания SkyGen: передовой дистрибьютор продукции для life science на российском рынке.
Спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Введение
Эта история началась в середине 1960-х, когда в препаратах аденовируса обезьян случайно было обнаружено загрязнение из маленьких неизвестных частиц [1]. Эти частицы были впоследствии названы аденоассоциированным вирусом (сокращенно ААВ, англ. adeno-associated virus, AAV). Тогда мало кто мог предположить, что именно эти крошечные вирусы дадут надежду многим неизлечимым больным. И лишь несколько исследовательских групп, движимых чисто научным любопытством, отправились изучать базовую биологию ААВ.
Прошло несколько десятков лет, и стало понятно, что ААВ обладает множеством уникальных свойств. Эти особенности позволяют использовать его в поистине революционном направлении — генной терапии. По разным оценкам, около 5% новорожденных детей страдает от различных генетических заболеваний [2]. Долгие годы такие болезни считались неизлечимыми, и для многих подобный диагноз приравнивался к приговору. К счастью, времена изменились. Мы находимся на пороге эры лекарств принципиально нового типа [3], и немаловажную роль в этом сыграл аденоассоциированный вирус [4].
Биология вируса
Какими же уникальными особенностями обладает ААВ? Чтобы ответить на этот вопрос, нужно подробнее поговорить про его жизненный цикл и строение.
Аденоассоциированный вирус принадлежит к роду Dependoparvovirus семейства Parvoviridae. Название рода отражает его необычный жизненный цикл, когда для размножения необходимо наличие вспомогательного вируса (от лат. Dependo — «зависеть»). В качестве такого вируса-помощника, как правило, выступает аденовирус (что явно следует из названия) или представители семейства герпесвирусов [5].
ААВ настолько безобиден, что помимо неспособности самостоятельно размножаться, он не вызывает никаких заболеваний человека и животных. Более того, согласно некоторым исследованиям, большинство людей (>70%) в течение жизни были заражены одним или несколькими серотипами ААВ [6]. (Серотип — вариант вируса, который отличается от других антигенами на своей белковой оболочке).
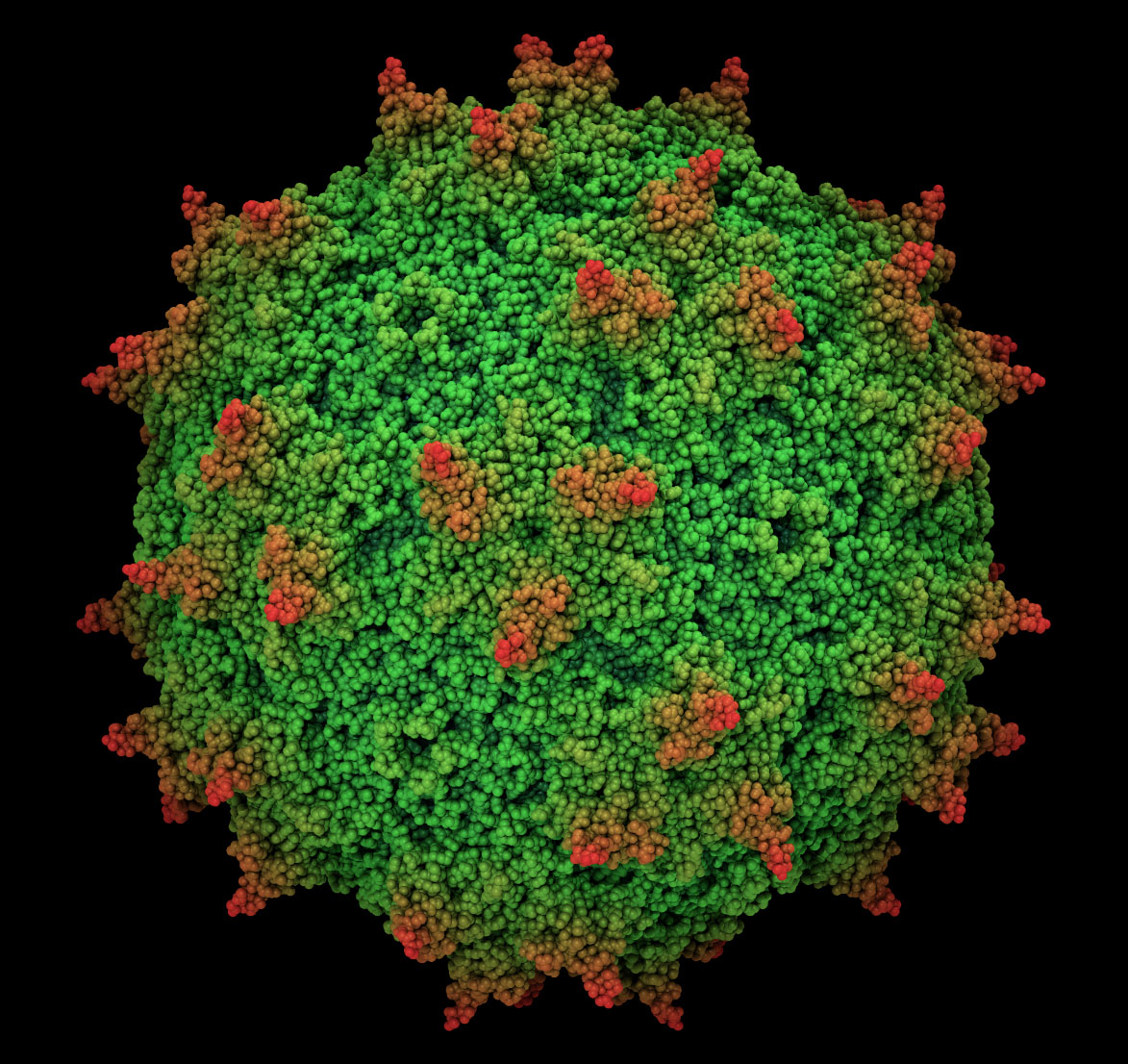
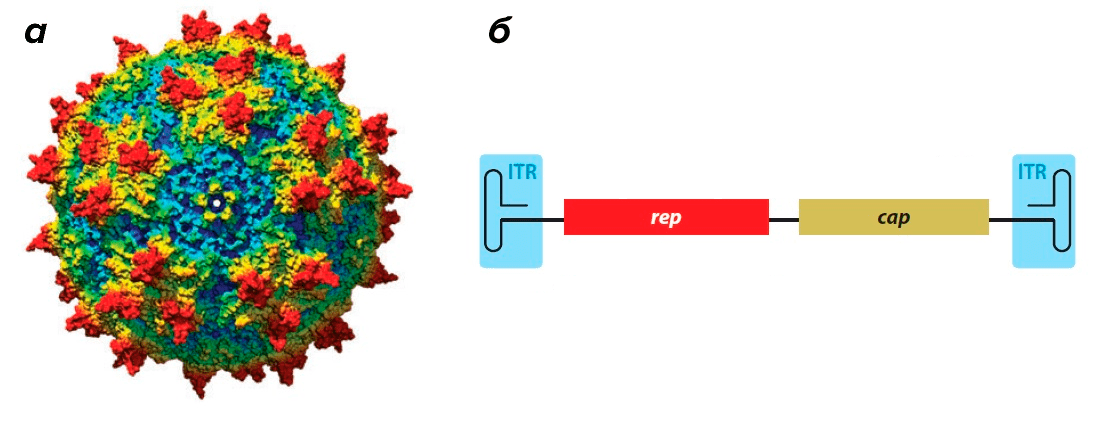
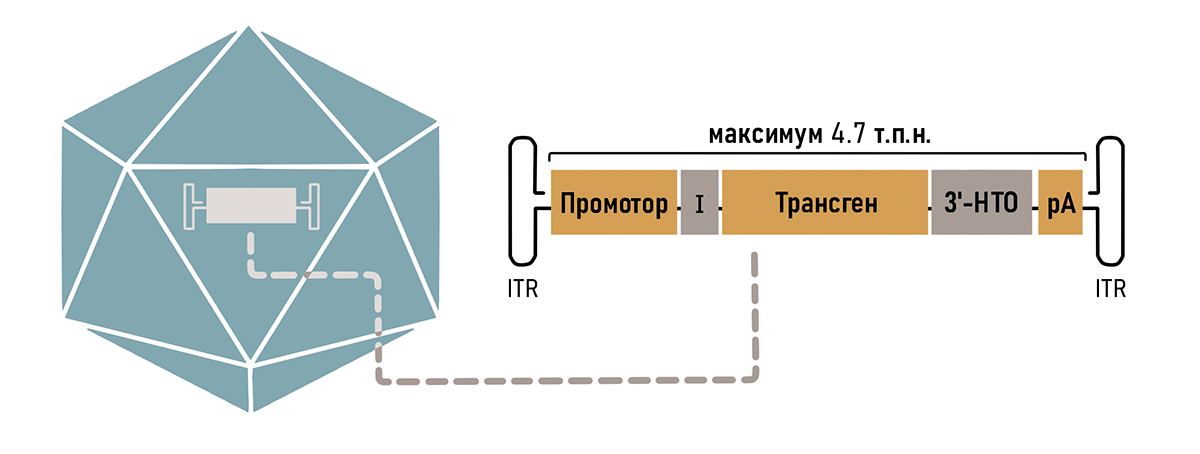
Вирус довольно мал — его икосаэдрическая белковая оболочка (капсид) в диаметре составляет всего около 25 нм (риc. 1а). Капсид необычайно стабилен: устойчив к кратковременному воздействию тепла, кислой среде и протеазам [7]. Геном, представленный одноцепочечной ДНК, по размерам также весьма скромен — всего 4,7 тысяч нуклеотидов [7].
Этот небольшой геном содержит минимальное количество генов. Ген rep (от слова replication) кодирует белки, необходимые для размножения вируса и его дальнейшей сборки внутри клетки (рис. 1б). Ген cap (от слова capsid) кодирует белки капсида (рис. 1б).
Геном ААВ обрамлен двумя Т-образными шпильками — инвертированными концевыми повторами (inverted terminal repeats, ITR) (рис. 1б).
Рисунок 1. Аденоассоциированный вирус. а — Модель капсида ААВ. б — Геном аденоассоциированного вируса. ITR (inverted terminal repeats) — инвертированные концевые повторы, образующие Т-образные шпильки; rep — ген, кодирующий белки, отвечающие за репликацию; cap — ген, кодирующий белки капсида.
Судьба вируса в клетке
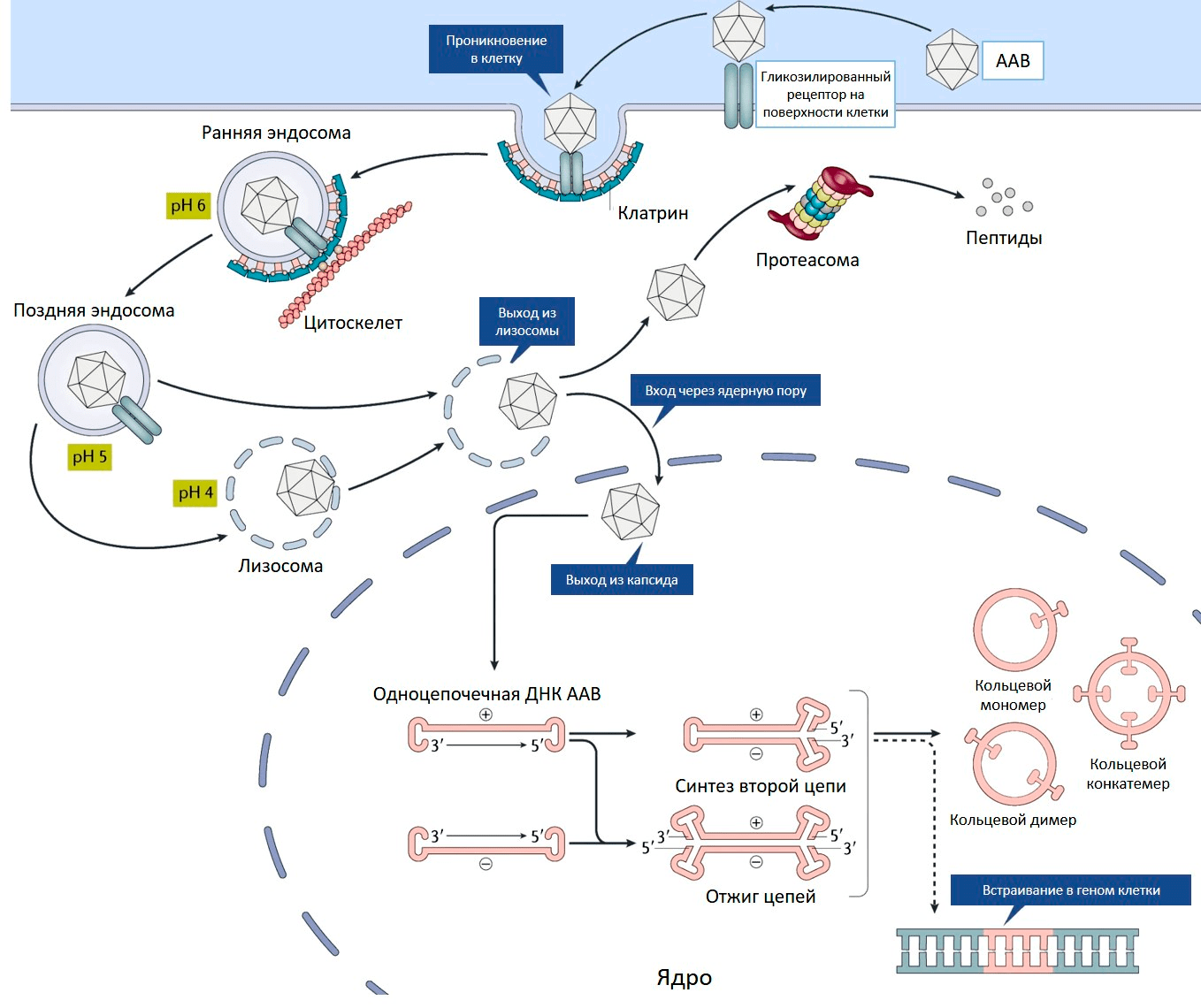
Ценное свойство ААВ — его способность проникать как в делящиеся, так и неделящиеся клетки [8]. На первом этапе аденоассоциированный вирус связывается с рецептором на поверхности клетки (рис. 2) [9]. Разные серотипы ААВ предпочтительно связываются со своими рецепторами, характерными для определенных типов клеток [10].
Рисунок 2. Проникновение ААВ внутрь клетки. Пояснения в тексте.
[9], рисунок с изменениями
И это важное свойство — определенный серотип преимущественно проникает лишь в конкретную ткань или орган, то есть обладает своим уникальным тропизмом.
Связывание вируса с рецептором запускает процесс проникновения внутрь клетки. Эндосома (мембранный пузырек, содержащий вирусную частицу) передвигается в цитоплазме по цитоскелету. Постепенно среда в эндосоме закисляется, что приводит к изменениям капсида, необходимым для дальнейшего успешного заражения клетки. После выхода из эндосомы у вируса два пути. Либо он попадает в клеточную машину по уничтожению белков (протеасому) и разрушается, либо переносится в ядро, где вирусный геном высвобождается из капсида (рис. 2) [10].
С одноцепочечного вирусного генома еще не могут нарабатываться белки, для этого необходимо достроить вторую цепь ДНК. Она синтезируется с помощью ДНК-полимеразы клетки-хозяина, используя шпильку ITR в качестве затравки для построения второй цепи.
Вирусные ITR помогают не только строить вторую цепь ДНК, но способствуют межмолекулярной и внутримолекулярной рекомбинации геномов вируса. В результате в ядре клетки образуются кольцевые молекулы ДНК — эписомы (рис. 2). В такой форме геномы ААВ могут в течение многих лет присутствовать в ядре [10].
Кроме того, геном ААВ может с низкой частотой встраиваться в определенный локус на 19 хромосоме человека [11]. Этот феномен обусловлен сходством последовательностей ДНК данного локуса и ITR вируса. У ААВ, лишенного гена rep, способность к встраиванию своего генома сильно снижена. Такие вирусные геномы присутствуют в клетках в виде эписом.
Модификация ААВ для применения в генной терапии
Если в гене человека произошла мутация, которая привела к развитию заболевания, то болезнь можно победить или облегчить, если доставить в клетки организма рабочую копию поломанного гена. Вот тут и выходит на сцену аденоассоциированный вирус.
Что же нужно было в нем изменить, чтобы он стал курьером для доставки таких терапевтических генов? Как это часто бывает в биологии, ученые просто воспользовались успешными решениями, уже созданными природой. Раз капсид ААВ сам по себе является ключом к входу в клетку и ядро, то можно смело этим воспользоваться. Остается только заменить гены самого вируса на гены, интересующие исследователя, и вирусный курьер готов!
Модификация генома ААВ
Оказалось, что от всего генома ААВ необходимо было оставить только концевые шпильки ITR, необходимые для сборки самого вируса и сохранения его генома в ядре (рис. 3) [12]. Таким образом, можно без последствий удалить до 96% генома ААВ, используя полученное пространство для кодирования нужных генов.
Так как ААВ вмещает в себя всего около 5000 пар нуклеотидов, то нужно очень тщательно продумать остальной состав кассеты. В первую очередь туда необходимо поместить рабочую копию гена (трансген), в зависимости от того генетического заболевания, на которое направлено лечение. Также обязательно наличие регуляторных последовательностей, таких как промотор и сигнал полиаденилирования (рис. 3). Разберем элементы кассеты подробнее.
Рисунок 3. Компоненты типичной кассеты ААВ вектора. Оранжевые блоки (промотор, трансген и сигнал полиаденилирования — рА) являются обязательными компонентами. Для повышения эффективности экспрессии могут быть включены необязательные регуляторные элементы, такие как интрон (I) и другие компоненты 3′-нетранслируемой области (НТО). Кассета обрамлена инвертированными терминальными повторами (ITR).
рисунок авторов статьи
Из-за ограниченной емкости вируса могут возникнуть трудности с доставкой больших терапевтических генов. Очевидное решение проблемы — разработка сокращенной версии гена, который кодирует усеченный, но функциональный белок. Создание таких укороченных генов требует глубокого понимания биологии терапевтического белка, взаимосвязи его структуры и функции. Такой подход уже успешно применяется в нескольких клинических испытаниях по лечению миодистрофии Дюшенна [13] (ссылки на клинические испытания: NCT03368742, NCT04281485, NCT03769116), в доклинических исследованиях по лечению дисферлинопатии, амавроза Лебера и многих других заболеваний.
Другим потенциально перспективным подходом для доставки слишком больших трансгенов может быть разделение гена между двумя ААВ-векторами [14]. Два этих векторных генома, попадая в одно и то же ядро клетки, могут подвергаться межмолекулярной рекомбинации с последующим восстановлением полноразмерного гена. Такой двухвекторный подход пока применяется лишь в редких клинических испытаниях (пример — NCT02710500). Низкая эффективность восстановления полноразмерного гена ограничивает более широкое применение этого приема.
Правильно выбранный промотор — во многом залог успешной генной терапии. Идеальный промотор должен запускать стабильную высокую экспрессию трансгена в пораженных органах в течение длительного периода, при этом быть неактивным в других тканях. Малая емкость ААВ также требует уменьшения размера промотора [15].
К кассету можно добавить необязательные элементы, способные улучшить экспрессию трансгена (рис. 3). Так, например, присутствие интрона повышает стабильность РНК в ядре [16], а также способствует эффективному транспорту мРНК из ядра в цитоплазму [17].
К обеспечению тканеспецифичности можно подойти с другой стороны — не только стимулируя экспрессию в целевых тканях, но и подавляя ее в нежелательных органах с помощью механизмов РНК-интерференции [18]. Для этого в 3′-НТО-кассеты добавляют сайты связывания микроРНК, присутствующих строго в нецелевых органах (рис. 3) [19]. Если трансген оказывается в нежелательном органе, то микроРНК связывается с комплементарными ей сайтами в транскрипте и запускает его деградацию.
Модификация капсида ААВ
Хотя капсид ААВ — сам по себе уже удачное изобретение природы, человечество не остановилось в своем научном поиске. Новые серотипы ААВ могут обладать рядом преимуществ:
Благодаря развитию новых методов анализа выделяют несколько основных направлений для создания или выявления новых серотипов.
К сожалению, всегда существует вероятность, что хорошо работающий in vitro модифицированный капсид в экспериментах на лабораторных животных продемонстрирует низкую эффективность или даже токсичность. Всестороннее изучение свойств разрабатываемых препаратов и строгий контроль качества призваны минимизировать риск неблагоприятного исхода исследований [23].
Применение ААВ в клинике
Целевые органы, на которые направлена терапия
К 14 декабря 2020 года 227 препаратов на основе ААВ проходят клинические испытания (по данным сайта ClinicalTrials.gov). Сегодня уже существует несколько препаратов на основе ААВ, которые получили одобрение от регулирующих органов для коммерческого использования у пациентов (подробнее про эти препараты можно почитать в [4]):
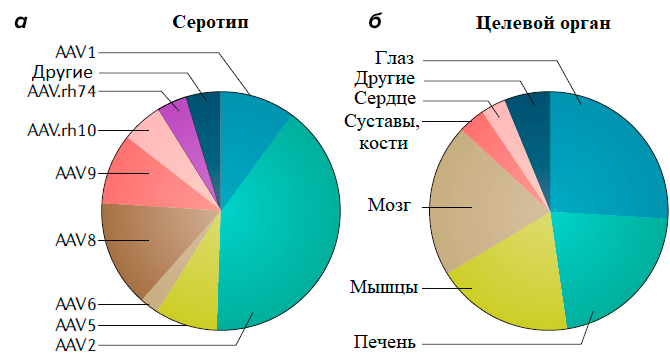
Большинство серотипов ААВ «предпочитают» проникать в такие органы, как печень, поперечно-полосатые мышцы и ЦНС, что и определило направление большинства программ генной терапии (рис. 4).
Рисунок 4. Данные с сайта ClinicalTrials.gov: на 13 ноября 2018 г. было зарегистрировано 145 клинических испытаний с использованием ААВ. а — Классифицикация клинических испытаний на основе примененного серотипа ААВ (AAV). б — Целевой орган, на который направлена терапия в указанных клинических испытаниях. Можно заметить, что спустя два года количество клинических испытаний с применением ААВ почти удвоилось (227 на сегодняшний день против 145 испытаний два года назад).
Почти все природные серотипы ААВ эффективно заражают печень после внутривенного введения. Благодаря данному свойству вируса в клинических испытаниях находятся препараты для лечения гемофилии A и B (NCT03392974, NCT03587116), семейной гиперхолестеринемии (NCT02651675), дефицита орнитинтранскарбамилазы (NCT02991144), мукополисахаридоза-IIIA (NCT03612869) и синдрома Криглера—Найяра (NCT03223194) [25].
Серотипы ААВ8 и ААВ9 могут эффективно заражать разные типы мышц по всему телу. Такое свойство делает их идеальными векторами для генной терапии множества мышечных заболеваний [26]. Так, активно исследуются в клинике препараты для лечения миодистрофии Дюшенна (NCT03375164), дисферлинопатии (NCT02710500), миотубулярной миопатии (NCT03199469), болезни Помпе (NCT03533673). Примечательно, что зараженная мышца может также служить биофабрикой для производства секретирующихся терапевтических белков для лечения немышечных заболеваний. Хотя большинство сердечных заболеваний полигенны и подвержены влиянию окружающей среды, ведется разработка препаратов генной терапии для лечения сердечной недостаточности [26].
Большой процент разрабатываемых препаратов на основе ААВ направлен на лечение неврологических и глазных болезней (рис. 4) [27], [28]. Глаз — весьма обособленный орган, обладающий уникальной иммунологической толерантностью, и легко доступный для прямого введения препарата. Нетрудно понять, почему один из первых одобренных препаратов, «Люкстурна», был направлен именно на лечение наследственной слепоты. Мозг, напротив, намного более крупный и сложно организованный орган. Прямая доставка препарата в мозг или спинномозговую жидкость позволяет локализовать вирус и снизить дозу препарата, но это инвазивная процедура, сопряженная со многими рисками. К счастью, такие серотипы, как ААВ9 или ААВrh.10, могут пересекать гематоэнцефалический барьер, что позволяет использовать рутинное внутривенное введение. В настоящий момент в клинических испытаниях уже находятся препараты для лечения болезни Паркинсона (NCT02418598), метахроматической лейкодистрофии (NCT01801709), болезни Баттена (NCT01414985), мукополисахаридоза 3 типа (NCT03300453).
Основные стратегии генной терапии на основе рААВ
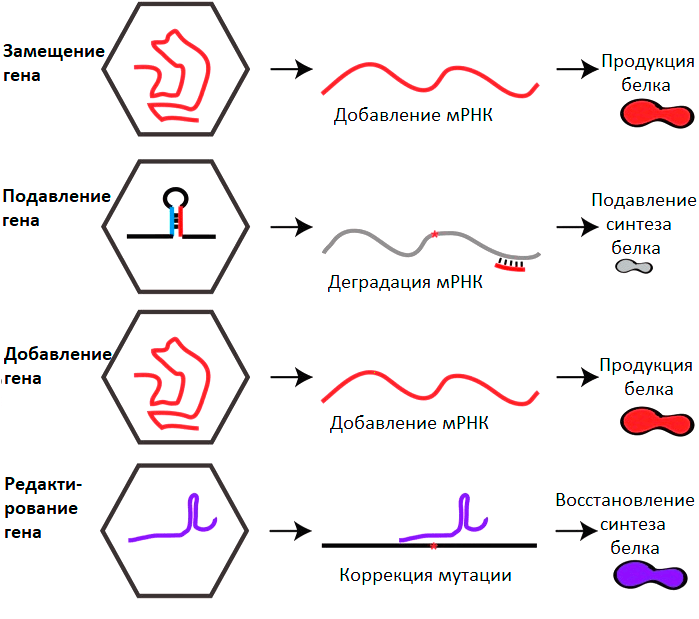
Можно выделить 4 глобальных направления генной терапии с применением ААВ (рис. 5).
Рисунок 5. Основные стратегии генной терапии на основе ААВ. Пояснения в тексте.
[29], рисунок с изменениями
Производство ААВ
Когда речь идет о клинических испытаниях, требуется очень большое количество вирусного препарата высокого качества. Его производство — весьма нетривиальная задача.
Вирусы не могут самостоятельно себя воспроизводить, им необходима помощь клеточной машинерии. Для наработки ААВ стали использовать культуры клеток. Вариантов может быть много: использование культуры дрожжей (Saccharomyces cerevisiae) [33], клеток насекомых (культура клеток Sf9 бабочки Spodoptera frugiperda) [34], человека — HEK293, HeLa. Некоторые из этих подходов, — скорее, экзотика, но использование культур клеток млекопитающих (HEK293) или насекомых (Sf9) уже прочно закрепилось на производстве.
Итак, для начала необходимо определиться с методикой производства, ведь от этого зависит, в чем будет расти сама культура. Вариантов масса: для клеток, растущих, прикрепившись к субстрату, это могут быть большие чашки Петри, специальные сосуды с множеством перегородок для увеличения площади поверхности (рис. 6а). Для культур, хорошо чувствующих себя в виде суспензии и при постоянном перемешивании, — колбы, герметичные пакеты и многое другое. При увеличении масштабов производства можно переходить на специальные биореакторы (рис. 6б). С их помощью можно следить за целой панелью важных для процесса параметров. Они делают производство более технологичным и позволяют увеличить объемы продукции до нескольких сотен литров вирус-содержащей суспензии за один цикл работы.
Рисунок 6. Производство ААВ: на культуральных чашках (а) и в биореакторе iCellis Nano (Pall corporation) (б)
фотографии авторов статьи
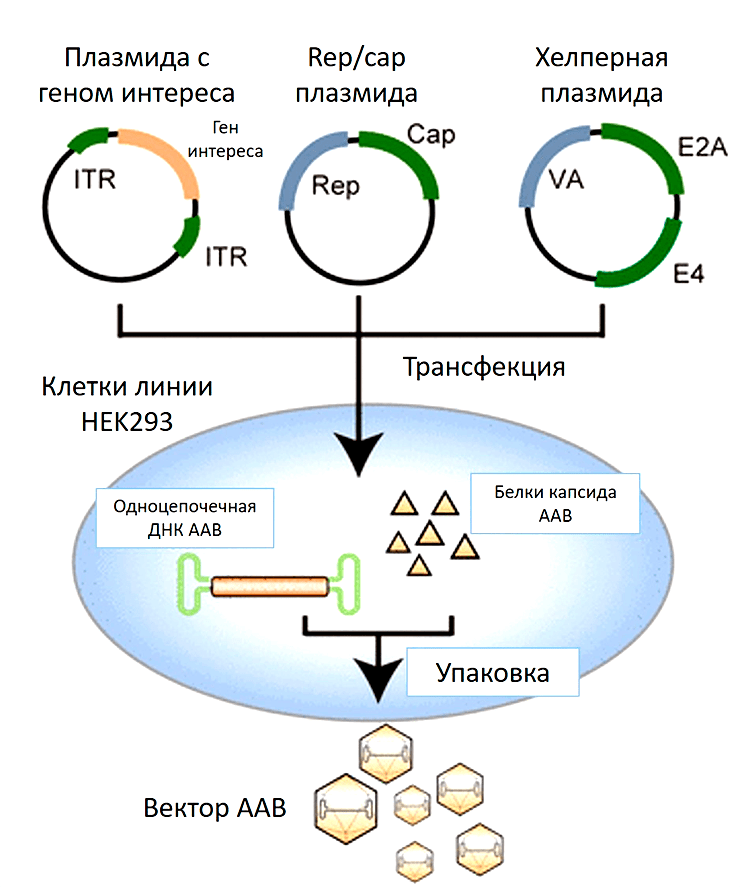
Что нужно сделать с культурой клеток, чтобы она стала биофабрикой по производству вирусных частиц? В такие клетки-производители вносят плазмидную ДНК, кодирующую необходимую для сборки вирусов информацию. Наиболее популярный протокол предполагает одновременное заражение клеток тремя плазмидами (рис. 7):
Кстати, вместо третьей плазмиды может быть добавлен сам вирус-помощник (аденовирус или герпесвирус), как это было в более ранних протоколах по производству частиц ААВ [35].
Рисунок 7. Производство ААВ, использующее в качестве клеток-производителей культуру клеток человека HEK293. Смесь трех плазмид доставляют внутрь клетки (плазмиду с терапевтическим геном, плазмиду, кодирующая гены rep/cap, и плазмиду с генами вируса помощника). Начинается наработка необходимых белков для сборки вирусных частиц. ДНК, содержащая терапевтический ген, упаковывается в готовый капсид ААВ.
Клетки начинают производить вирусные частицы, после чего их надо собрать и очистить.
Это критически важный этап, которому стоит уделить особое внимание [22], [23]. Любые примеси, которые будут содержаться в препарате, могут вызвать нежелательный иммунный ответ.
Вначале собирают сырой материал: это может быть клеточная среда, если вирусы выделяются клетками преимущественно в жидкость вокруг, а могут быть и сами клетки, если большинство вирусных частиц накапливается внутри. Как правило, это зависит от конкретного серотипа ААВ. Чтобы разрушить клеточные мембраны и высвободить вирус, клетки подвергают многочисленным циклам замораживания-оттаивания, ультразвуковой обработке или воздействию детергентов.
Теперь основная задача — очистить вирусные частицы от многочисленных примесей, находящихся в суспензии (рис. 8). В сыром материале находятся внутриклеточные свободные ДНК и РНК, белки и ферменты, крупные обломки клеточных мембран и многое другое. Способов очистки существует множество, и постоянно появляются как улучшенные версии уже применяемых методик, так и принципиально новые подходы. Все они различаются по уровням специфичности, эффективности и, разумеется, стоимости. Условно способы очистки можно разделить на серотип-специфичные и универсальные. К первой категории относится, например, аффинная хроматография [37], основанная на специфическом узнавании капсидов антителами. Ко второй — ультрацентрифугирование в градиентах плотности растворов йодиксанола или хлорида цезия, преципитация полиэтиленгликолем или сульфатом аммония, ионообменная хроматография и многие другие методы, основанные на общих физических свойствах вирусных частиц [38].
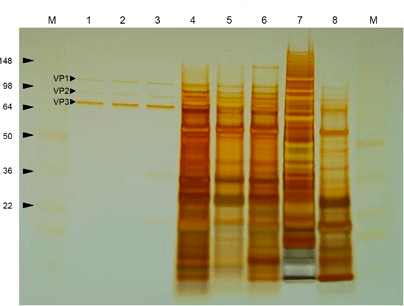
Рисунок 8. Окрашивание серебром очищенного (лунки 1–3) и загрязненного другими белками (лунки 4–8) препарата ААВ после гель-электрофореза [38].
Одна из неочевидных нежелательных примесей — так называемые пустые капсиды — вирусные частицы, не несущие в себе терапевтический ген, или содержащие внутри себя постороннюю ДНК. Дело в том, что изначально в клетке формируется пул пустых капсидов. Лишь потом ДНК связывается с пустым капсидом при помощи специальных сигналов на ITR и компактно упаковывается, формируя полноценную вирусную частицу. Но иногда пустой капсид может так и остаться пустым при нехватке вирусной ДНК или ее неэффективной упаковке. В пустой капсид может также упаковаться обрывок свободной ДНК, находящейся в клетке и содержащей последовательность, схожую с сигналом упаковки. Такие частицы (совсем пустые или несущие неправильную последовательность) не функциональны и подлежат удалению из очищаемого препарата. С определенной эффективностью их можно отделить от функциональных капсидов, используя градиенты плотности или методы хроматографии.
Основные проблемы
Наработка большого количества плазмид высокой степени очистки, поддержание культур клеток, дорогостоящие реактивы, сложный процесс очистки вирусных частиц и разработка аналитических методик для характеризации препаратов ведут к таким космическим ценам при масштабировании производства. На стоимость также влияет серьезный контроль качества вирусного препарата. Чтобы препарат вышел на рынок, проводятся исследования его токсичности, безопасности, биораспределения, эффективности. Оценивается содержание белковых примесей, бактериальных эндотоксинов, количество пустых капсидов, стерильность препарата, концентрация вирусных частиц в растворе и множество других характеристик [23]. В настоящий момент гиганты производств ААВ по всему миру работают над удешевлением препаратов, разрабатывая более эффективные протоколы сборки и очистки ААВ.
Иммунный ответ также представляет собой серьезную проблему. Потенциально иммунные реакции могут возникать на вирусный капсид, его геном, а также на белковый продукт трансгена. Препаратам на основе ААВ могут помешать нейтрализующие антитела к его капсиду [39]. Связываясь с вирусами в кровотоке, антитела препятствуют проникновению вирусных частиц в клетки, что ведет к низкой эффективности препарата. В настоящий момент обязательно проводится скрининг пациентов на наличие антител к применяемому серотипу ААВ [40]. В случае их обнаружения такой пациент исключается из клинических испытаний. Ведется разработка новых капсидов, которые не будут узнаваться нейтрализующими антителами [41]. После доставки терапевтических доз ААВ быстро развивается гуморальный иммунный ответ, который впоследствии помешает повторному введению препарата [42]. Именно поэтому большинство генотерапевтических препаратов на основе ААВ рассчитано на однократное введение. Для подавления Т-клеточного иммунного ответа у пациентов применяется фармакологическая супрессия стероидами [40].
Заключение
Генная терапия на основе ААВ — бурно развивающееся направление, и мы в данном обзоре затронули лишь небольшой кусочек этой удивительной области. Текущий экспоненциальный рост клинических испытаний с использованием ААВ предполагает, что мы находимся в самом начале эры новых генотерапевтических препаратов. Еще очень много задач предстоит решить, и для этого требуются мультидисциплинарные усилия. Дальнейшее развитие молекулярной биологии, биоинформатики, эпидемиологии, структурной биологии, иммунологии, геномики и других дисциплин, безусловно, будет способствовать совершенствованию технологии. Уже пройден длинный путь в попытке человечества победить генетические заболевания. Мы надеемся, что именно генная терапия приведет к окончательной победе!