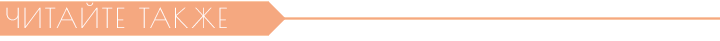Карбонат соды что это
Карбонаты натрия (Е500)

Раствор чаще всего применяют при готовке блюд в виде карбоната натрия, гидрокарбоната, их смеси.
Краткие сведения
Название походит из латыни, от наименования растения. В прошлые века ее усердно получали из золы. Кальцинированная сода была создана в конце 18-го века Лебланом, однако пищевая – в 1861 г. Сольвэ.
Карбонат натрия кислота получается несколькими способами. Наиболее распространенный из них – методика Сольве. Так добывают более 90% всех объемов промышленного вещества. Для этого нужен хлорид натрия, аммиак.
Вещество получается в процессе кальцинирования (увеличение температурных значений). От этого оно именуется кальцинированным. Ряд стран получает из месторождений. Также изготавливается промышленным способом в тех регионах, где отсутствуют залежи минералов.
Методики синтеза
Используют «сухой» и «мокрый» способы. В основе процесса – карбонизация (присоединение углекислоты). Отмечают перекристаллизационные преображения. Методики отличаются готовкой раствора. При сухом – кальцинированные элементы растворяются водой, а при мокром применяют технический бикарбонат.
Разложение вещества при постепенном возрастании температуры именуют декарбонизацией.
Содовые элементы раствора под влиянием диоксида углерода осаждаются. Чистая пищевая содовая часть отделяется, а маточные компоненты вновь идут на получение первичного раствора.
Главные свойства
| Систематическое наименование | Карбонат натрия |
|---|---|
| Традиционные наименования | Кальцинированная сода |
| Молекулярная масса | 105,99 г/моль |
| Плотность | 2,53 г/см3 |
| Растворимость | 21,8 г/100 мл |
Масса уникальных характеристик определила ценную роль элемента для человека. Внешний облик являет собой бесцветные кристаллические элементы. Иногда встречаются формы порошкообразного элемента беловатого окраса.
По общеобразовательным качествам пищевой эмульгатор отличается немаленькой температурой плавления (853 градуса).
Вещество не теряет своей способности отменно растворяться в водных структурах (в отличие от этанола). Особенность кроется в способности поглощать углекислоту.
Применение
Массовая доля карбоната натрия довольно весомая в кондитерстве и в кулинарии в целом. Ведь вещество просто незаменимо при приготовлении выпечки. Зачастую Е500 входит как в готовую продукцию, так и в смеси.

Сода также применяется в различных секторах промышленности. Больше всего ее применяют в стекольной промышленности, цветной металлургии, химическом производстве.
Особенности использования в кулинарии
Пищевая сода – незаменимый элемент добавки, который используется в составе изделий в роли разрыхлителя. Обнаружить ее возможно в сгущенном молоке, мармеладе, джеме, маргарине.
Взаимодействие карбоната натрия с продуктами используется во время приготовления брецелей и рулетов. Технология подобной нестандартной обработки разведенным щелочным веществом целиком оправдана. Так можно безопасно изменить кислотность продукции. В итоге это приводит к возникновению необычайно хрусткой корочки на поверхности продукции. Карбонат натрия — незаменимый элемент. Без него никогда не получится идеальная лапша. Все дело в том, что нежность содового элемента в рассоле сохраняет вкусовое качество макарон. Добавка используется при готовке шербета. Так действует карбонат и несильные кислотные элементы. При этом образуется углекислота из-за слюны.
Карбонат натрия серная кислота содержится в большинстве паст по уходу за ротовой полостью и зубными элементами. Это пенообразователь, абразив, который на время минимизирует кислотность во рту. Подобным образом предупреждаются многие недуги.
Влияние
По итогам численных мировых исследований, реакции карбоната натрия не причиняют никакого вреда клеткам организма. То есть вещество числится в категории неопасных добавок. Без передозировки никогда и никому не наносит вред.
Но определенный вред кислота карбоната все же несет.
Существуют доказанные факты, согласно которым чувствительный организм плохо переносит вещество. Возникает затруднение дыхания, обмороки.
В экспериментах показано, что формула данного вещества неблагоприятно влияет на печень и мозг живого организма. Длительное потребление продуктов с Е500 увеличивает риски появления аллергических реакций на руках и голове.
Карбонат натрия и соляная кислота – самые известные антагонисты. Об их противоположном влиянии ведомо давно. Существует даже старинный способ победить изжогу – размешать в воде соду. «Пожар» исчезнет в считанные минуты. Это никак не методика терапии. Методика действенно и скоро позволяет избавиться от изжоги на непродолжительный период. Переизбыток соды способен провоцировать рези, даже аллергические признаки.
На территории многих стран разрешено применение Е500 в качестве пищевой добавки.
Упаковка, транспортировка
Перемещают данное вещество любым транспортом, но исключительно в плотно закрытых объектах. Элемент совершенно безопасен, поскольку лишен даже минимальной токсичности. Сохраняется содовый элемент только в закрытых упаковках. Крайне важно не допустить присутствия влаги в данной структуре. На протяжении года истекает гарантийный срок на сохранение содового раствора. При этом общий срок пригодности не лимитирован.
Содовый элемент можно по праву назвать главным разрыхлителем при выпечке. Данное вещество при нагревании выделяет углекислоту. За счет этого тесто становится мягким, пушистым. Сода выступает как самостоятельное вещество для разрыхления либо в комплексном составе пекарского порошка. При этом важно не переусердствовать с дозировкой. Содовый элемент оставляет в готовом продукте довольно неприятный, но безвкусный привкус. Соду важно добавлять в муку, кислые компоненты – только в жидкость.
Кальцинированная сода: 33 способа применения в домашних условиях, в саду и огороде
Кальцинированная сода — ближайшая «родственница» соды пищевой. Первую хозяйки охотнее применяют в борьбе с загрязнениями, вторую — в кулинарии. И если для выпечки кальцинированную соду использовать нельзя, то в наведении порядка в жилище ей нет равных.
Формула и характеристика кальцинированной соды
Кальцинированная сода — химическое соединение со следующим составом:
Формула кальцинированной соды — Na2CO3.
Другое название химического соединения — карбонат натрия или бельевая сода.
Внешне это соединение выглядит как порошок белого цвета.
Основное свойство этой разновидности соды — водорастворимость. После взаимодействия с водой она образует щелочной раствор, который помогает удалять пятна.
Ещё одно свойство карбоната натрия — токсичность для различных микроорганизмов: вирусов, бактерий, микробов.
История открытия
С бельевой содой человечество познакомилось давно — 2 000 лет до н.э. Древние египтяне добывали её из вод озёр. Сода применялась для варки стекла и заменяла моющее средство.
Слово «сода» произошло от словосочетания «солянка содоносная». Этим термином обозначали растение, которое древние люди сжигали, получая золу. Затем ее нагревали до высоких температур, т.е. кальцинировали. Полученным в результате таких действий веществом и стала кальцинированная сода. Таким образом соду добывали вплоть до начала XIX века.
Идея получать бельевую соду искусственным путем принадлежит французскому фармацевту Н.Леблану. Он предложил добывать это вещество путем прокаливания смеси сульфата натрия, угля и измельченного мела. Из этого состава карбонат натрия выщелачивали водой, далее раствор упаривался, и выделялась чистая кальцинированная сода. Отходом производства считался выделившийся сульфат кальция.
Впоследствии были разработаны новые методы добычи бельевой соды, при которых образовывалось гораздо меньшее число отходов.
В природе большие количества карбоната натрия встречаются в виде поземных грунтовых рассолов, а также рапы в соляных озерах.
Крупные месторождения этого соединения расположены в Канаде, США, Мексике, Кении, ЮАР. Содовые озера есть в Западной Сибири и Забайкалье.
Отличие от другой соды
Бельевую соду следует отличать от пищевой и каустической
Пищевая, кальцинированная и каустическая сода — представители натриевых соединений. Но эти соединения отличаются друг от друга химической формулой.
Пищевая сода — продукт безопасный, может применяться в быту и кулинарии. Нанести вред здоровью может, только если большое ее количество человек употребил внутрь.
Кальцинированная сода имеет высокий водородный показатель (рН) — 11. Это соединение является сильной щелочью и способно спровоцировать ожоги и аллергию. Применяется только в быту. Кальцинированная сода обладает хорошими очищающими свойствами.
Каустическая сода — щелочь, которая хорошо устраняет загрязнения, но может разъедать органические вещества. Очищающий эффект каустической соды выражен более ярко в сравнении с пищевой и бельевой. Каустическая сода — токсичное вещество.
| Вид соды | Формула | pH | Химическое название | Внешний вид | Токсичность |
| Пищевая | NAHCO3 | 8 | Гидрокарбонат натрия | белый порошок (кристаллический) | Нетоксична |
| Кальцинированная | Na2CO3 | 11 | Карбонат натрия | бесцветный порошок (кристаллический) | + |
| Каустическая | NaOH | 13 | Гидроксид натрия | белая чешуйчатая масса (твердая) | + |
Польза и вред карбоната натрия
Кальцинированная сода — полезное соединение и вот почему:
Несмотря на множество преимуществ, у бельевой соды есть и недостатки:
Применение карбоната натрия
Карбонат натрия широко используется в самых различных сферах деятельности человека:
Это вещество применяют и для дезинфекции помещений, в которых содержатся животные, в текстильной, автомобильной и химической областях.
В быту
Для устранения различных загрязнений в жилище хозяйки часто используют и пищевую соду. Но бельевая справляется с трудновыводимыми пятнами гораздо эффективнее.
На кухне
Одно из самых излюбленных мест для скопления различного рода бактерий — кухонная раковина. Отмыть ее дочиста можно с помощью карбоната натрия.
Если в месте вокруг основания смесителя скопился известковый налет, загрязненную поверхность нужно посыпать бельевой содой. Порошок немного увлажнить водой и дать постоять 30 минут. Спустя положенное время удалить загрязнение губкой, протереть поверхность сухой чистой тряпкой.
Для чистки рабочих поверхностей, кафеля
Карбонат натрия — эффективное средство для удаления загрязнений с кафеля и рабочих поверхностей на кухне.
При стирке белья
Кальцинированную соду можно использовать для ручной стирки белья. Но не все ткани можно стирать таким средством. Шелковые, шерстяные и полностью синтетические вещи не будут рады встрече с бельевой содой — после стирки они станут жесткими и хрупкими.
Бытовые проблемы решит каустическая сода
Карбонат натрия в отличие от стиральных порошков не провоцирует аллергических реакций.
Кипячение белья
Кальцинированную соду используют также для дезинфекции и качественного отбеливания тканей.
Устранение засоров в трубах
Если вода из раковины в ванной комнате или кухне плохо уходит, не обязательно приглашать сантехника. Эту проблему легко устранит карбонат натрия. Он хорошо разъедает остатки пищи, жир и грязь, которые застряли в трубах
Важно защитить дыхательные пути респираторами — пары хлора опасны для здоровья. Очистив засор, нужно проветрить помещение.
Чистка стиральной машины, сантехники
Карбонат натрия эффективно устраняет мочевой камень, мыльные отложения, ржавчину, известковый налет. Поэтому порошок можно использовать для очистки поверхностей ванны, туалета или душа. Подойдет он также для чистки барабана стиральной машины.
Для очищения стиральной машинки.
Кальцинированная сода помогает устранить плесень с внутренних деталей стиральной машины, избавить прибор от неприятного запаха.
В садоводстве
Карбонат натрия поможет садоводу уничтожить огородных вредителей и сделать цветение растений более пышным.
Обработка растений от вредителей
Бельевая сода помогает защитить садовые растения от различных болезней. Благодаря этому белому порошку садовод может уничтожить вредителей, которые и провоцируют заболевания.
Спасти растения, пораженные мучнистой росой, можно с помощью раствора кальцинированной соды.
Раствор лучше использовать в ясную безветренную погоду.
Раствор для борьбы с калиновым листоедом.
Этот зловредный жук поражает не только листья калины, но и других культурных растений. Обилие этих вредителей на дереве сильно ослабляет его и провоцирует заболевания. Для борьбы с листоедом рекомендуется использовать карбонат натрия.
Омоложение растений
Этот простой и действенный рецепт садоводы применяют для омоложения роз.
Для пышного цветения
Бельевая сода — полезное удобрение для растений, которые любят щелочную почву. Карбонат натрия заставит их цвести пышным цветом. Обрабатывать этим раствором полезно бегонии гортензии и герани.
Приготовление и использование:
Мыловарение
Применяется карбонат натрия и в домашнем рукоделии. С его помощью можно создать мыло, которое очень хорошо устраняет загрязнения с вещей после работы в гараже или в саду. Также с его помощью можно выводить пятна с одежды путем вываривания белья. Эффективнее всего такое изделия будет работать на белых вещах при стирке выше 40 C°.
8 нестандартных способов применения соды на кухне
Смесь затвердевает уже через несколько суток, то есть гораздо раньше указанного срока. Пользоваться мылом сразу же не рекомендуется — оно будет плохо пениться. Все свойства настоящего мыла изделие приобретёт, когда «созреет».
Чтобы сделать мыло цветным, можно добавить в раствор зелёную глину, молоко, засушенные водоросли, мёд и т. д.
Снижение жесткости воды
Бельевая сода может быть использована для смягчения воды, которую затем применяют для хозяйственных нужд. Такую жидкость пить нельзя, а вот мыть руки и поливать растения — можно.
Где не рекомендуется использовать карбонат натрия
Кальцинированную сода не применяют для таких материалов:
Производители и марки
На территории России техническую кальцинированную соду (ГОСТ 5100-85) производят несколько предприятий:
На промышленных предприятиях производят кальцинированную соду 2 видов:
Где купить кальцинированную соду
Карбонат натрия реализуется в хозяйственных магазинах, в отделах, где торгуют бытовой химией.
Чаще всего, порошок расфасован в пакеты и пачки по 400 г, а также по 600 и 800 г.
Хранение кальцинированной соды
Карбонат натрия представляет собой рассыпчатый порошок без комков. В специальной упаковке она может храниться до 5 лет. После вскрытия тары бельевая сода хранится до 25 дней.
Карбонат натрия активно поглощает влагу из воздуха. Если пачка, в которой он содержится, открыта, соединение теряет свои свойства и постепенно слеживается.
Соду после вскрытия упаковки лучше хранить в стеклянной ёмкости, плотно закрыв пластиковой крышкой. Банку нужно непременно подписать.
Как сделать кальцинированную соду в домашних условиях
За карбонатом натрия необязательно отправляться в магазин, можно сделать этот порошок самостоятельно.
Меры предосторожности
Кальцинированная сода способна спровоцировать отравление, попадая в организм. Поэтому при использовании этого порошка нужно соблюдать правила безопасности:
Как приготовить раствор кальцинированной соды
Ещё несколько рецептов растворов на основе бельевой соды помогут хозяйке в решении бытовых проблем.
Для стирки белья в машинке
Бельевой содой допустимо заменить стиральный порошок.
В отделение для моющих средств высыпать 3 ст. л. соды. Если бельё очень загрязненное, можно засыпать 5 ст. л. Некоторые хозяйки высыпают порошок прямиком в барабан.
Использование соды и порошка совместно.
Для замачивания одежды
Простой и доступный по цене способ выведения пятен с одежды используется хозяйками вот уже несколько десятилетий подряд.
Замачивание с растительным маслом.
В результате такой обработки с белых простыней и салфеток отлично отстирываются жирные пятна.
Для мытья посуды
Карбонатом натрия эффективно очищать домашнюю утварь от загрязнений.
Для удаления нагара
Карбонат натрия особо эффективно растворяет нагар с кастрюль из керамики. Также её применяют для очистки эмалированной посуды.
10 способов использования соды в саду и огороде
Такой способ очистки не подходит для утвари из алюминия и чугуна. Щелочь действует на эти металлы разрушительно.
Для очистки чайника от накипи
Бельевой содой можно очистить от загрязнений заварочный чайник и удалить накипь со дна чайника, в котором кипятят воду на плите.
Чистим заварочный чайник от загрязнений.
Очистить дно и стенки чайника от накипи можно используя следующий рецепт.
Для чистки плиты
Духовки, печи и плиты засияют чистотой после использования клеево-содовой смеси.
Для мытья пола
После мытья полов этим раствором, поверхности засияют чистотой.
Для удаления старой краски
Бельевая сода может применяться как ингредиент для состава, который размягчает застарелую краску. С помощью такого раствора покрытие легче удалить с поверхности обычным шпателем.
Этот способ поможет удалить застарелую краску с деревянного пола.
Для обработки яиц
Бельевую соду используют также для дезинфекции яичной скорлупы. Это средство удаляет загрязнения и уничтожает поселившихся на поверхности яйца паразитов и вредоносные микроорганизмы.
Для дезинфекции
Карбонат натрия как дезинфицирующий состав применяют на предприятиях, где люди рискуют заразиться инфекционными заболеваниями: в больницах, кафе, ветеринарных клиниках. Раствором бельевой соды дезинфицируют склады, прилавки в магазинах, кипятят рабочую одежду, инструмент. В горячей воде бактерицидные свойства раствора увеличиваются.
Раствор карбоната натрия (2-3 %, разведенный в 80-градусном кипятке), за час полностью уничтожает вирус ящура. Через 10 минут — стрептококки, чрез 5 минут — кишечную палочку.
Это дезинфицирующее средство подойдет для обработки жилища, где находится пораженный вирусной или инфекционной болезнью человек.
Кальцинированная сода — универсальный состав для борьбы с бытовыми загрязнениями или огородными вредителями. Это вещество дезинфицирует и до блеска очищает поверхности. Но при работе с карбонатом натрия важно помнить о технике безопасности. Растворы готовят, предварительно защитив руки перчатками, а дыхательные пути — маской.
Сода – лучший помощник хозяйки: 5 советов по применению в уборке
10 способов использования соды в саду и огороде
Бытовые проблемы решит каустическая сода
5 рецептов с содой и уксусом для домашней дезинфекции
8 нестандартных способов применения соды на кухне
Применение соды для высокого урожая смородины
4 полезных подсказки по разведению огня в мангале во время дождя
Топка бани пеллетами: есть ли преимущества и можно ли использовать для этого обычную печь
Новые тапки из старых вещей: что кроме джинсов можно так переработать
10 способов использовать старый смартфон с пользой в доме
Карбонат натрия
| Карбонат натрия | |||
|---|---|---|---|
| |||
| Систематическое наименование | Карбонат натрия | ||
| Традиционные названия | кальцинированная сода, углекислый натрий | ||
| Хим. формула | Na 2 CO 3 | ||
| Молярная масса | 105,99 г/моль | ||
| Плотность | 2,53 г/см³ | ||
| Температура | |||
| • плавления | 854 °C | ||
| • разложения | 1000 °C | ||
| Константа диссоциации кислоты pKa | 10,33 | ||
| Растворимость | |||
| • в воде при 20 °C | 21,8 г/100 мл | ||
| ГОСТ | ГОСТ 5100-85 | ||
| Рег. номер CAS | 497-19-8 | ||
| PubChem | 10340 | ||
| Рег. номер EINECS | 207-838-8 | ||
| SMILES | |||
| Кодекс Алиментариус | E500(i) | ||
| RTECS | VZ4050000 | ||
| ChEBI | 29377 | ||
| ChemSpider | 9916 | ||
| ЛД50 | 4 г/кг (крысы, орально) | ||
| Пиктограммы СГС |  | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
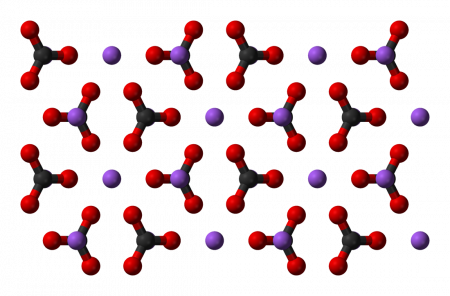
Карбонат натрия (кальцинированная сода) — неорганическое соединение, натриевая соль угольной кислоты с химической формулой Na 2 CO 3. Бесцветные кристаллы или белый порошок, хорошо растворимый в воде. В промышленности в основном получают из хлорида натрия по методу Солвэ. Применяют при изготовлении стекла, для производства моющих средств, используют в процессе получения алюминия из бокситов и при очистке нефти.
Содержание
Свойства
Имеет вид бесцветных кристаллов или белого порошка. Существует в нескольких разных модификациях: α-модификация с моноклинной кристаллической решеткой образуется при температуре до 350 °C, затем, при нагреве выше этой температуры и до 479 °C осуществляется переход в β-модификацию, также имеющую моноклинную кристаллическую решетку. При увеличении температуры выше 479 °C соединение переходит γ-модификацию с гексагональной решеткой. Плавится при 854 °C, при нагреве выше 1000 °C разлагается с образованием оксида натрия и диоксида углерода.
Кристаллогидраты карбоната натрия существуют в разных формах: бесцветный моноклинный Na2CO3·10H2O, при 32,017 °C переходит в бесцветный ромбический Na2CO3·7H2O, последний при нагревании до 35,27 °C бесцветный переходит в ромбический Na2CO3·H2O. В интервале 100—120 °C моногидрат теряет воду.
| Параметр | Безводный карбонат натрия | Декагидрат Na2CO3·10H2O |
|---|---|---|
| Молекулярная масса | 105,99 а. е. м. | 286,14 а. е. м. |
| Температура плавления | 854 °C | 32 °C |
| Растворимость | Не растворим в ацетоне, и сероуглероде, малорастворим в этаноле, хорошо растворим в глицерине и воде | |
| Плотность ρ | 2,53 г/см³ (при 20 °C) | 1,446 г/см³ (при 17 °C) |
| Стандартная энтальпия образования ΔH | −1131 кДж/моль (т) (при 297 К) | −4083,5 кДж/моль ((т) (при 297 К) |
| Стандартная энергия Гиббса образования G | −1047,5 кДж/моль (т) (при 297 К) | −3242,3 кДж/моль ((т) (при 297 К) |
| Стандартная энтропия образования S | 136,4 Дж/моль·K (т) (при 297 К) | |
| Стандартная мольная теплоёмкость Cp | 109,2 Дж/моль·K (жг) (при 297 К) |
| Температура, °C | 0 | 10 | 20 | 25 | 30 | 40 | 50 | 60 | 80 | 100 | 120 | 140 |
| Растворимость, г Na2CO3 на 100 г H2O | 7 | 12,2 | 21,8 | 29,4 | 39,7 | 48,8 | 47,3 | 46,4 | 45,1 | 44,7 | 42,7 | 39,3 |
В водном растворе карбонат натрия гидролизуется, что обеспечивает щелочную реакцию среды. Уравнение гидролиза (в ионной форме):
Нахождение в природе
В природе сода встречается в золе некоторых морских водорослей, а также в виде минералов:
Современные содовые озёра известны в Забайкалье и в Западной Сибири; большой известностью пользуется озеро Натрон в Танзании и озеро Сирлс в Калифорнии. Трона, имеющая промышленное значение, открыта в 1938 в составе эоценовой толщи Грин-Ривер (Вайоминг, США). Вместе с троной в этой осадочной толще обнаружено много ранее считавшихся редкими минералов, в том числе давсонит, который рассматривается как сырьё для получения соды и глинозёма. В США природная сода удовлетворяет более 40 % потребности страны в этом полезном ископаемом.
Получение
До начала XIX века карбонат натрия получали преимущественно из золы некоторых морских водорослей, прибрежных и солончаковых растений путём перекристаллизации относительно малорастворимого NaHCO3 из щёлока.
Способ Леблана
В 1791 году французский химик Никола Леблан получил патент на «Способ превращения глауберовой соли в соду». По этому способу при температуре около 1000 °C запекается смесь сульфата натрия («глауберовой соли»), мела или известняка (карбоната кальция) и древесного угля. Уголь восстанавливает сульфат натрия до сульфида:
Сульфид натрия реагирует с карбонатом кальция:
Полученный расплав обрабатывают водой, при этом карбонат натрия переходит в раствор, сульфид кальция отфильтровывают, затем раствор карбоната натрия упаривают. Сырую соду очищают перекристаллизацией. Процесс Леблана даёт соду в виде кристаллогидрата (см. выше), поэтому полученную соду обезвоживают кальцинированием.
Сульфат натрия получали обработкой каменной соли (хлорида натрия) серной кислотой:
Выделявшийся в ходе реакции хлороводород улавливали водой с получением соляной кислоты.
Первый содовый завод такого типа в России был основан промышленником М. Прангом и появился в Барнауле в 1864 году.
После появления более экономичного (не остаётся в больших количествах побочный сульфид кальция) и технологичного способа Сольве, заводы, работающие по способу Леблана, стали закрываться. К 1900 году 90 % предприятий производили соду по методу Сольве, а последние фабрики, работающие по методу Леблана, закрылись в начале 1920-х.
Промышленный аммиачный способ (способ Сольве)
В 1861 году бельгийский инженер-химик Эрнест Сольве запатентовал метод производства соды, который используется и по сей день.
В насыщенный раствор хлорида натрия пропускают эквимолярные количества газообразных аммиака и диоксида углерода, то есть как бы вводят гидрокарбонат аммония NH4HCO3:
Выпавший остаток малорастворимого (9,6 г на 100 г воды при 20 °C) гидрокарбоната натрия отфильтровывают и кальцинируют (обезвоживают) нагреванием до 140—160 °C, при этом он переходит в карбонат натрия:
Образовавшийся CO2 возвращают в производственный цикл. Хлорид аммония NH4Cl обрабатывают гидроксидом кальция Ca(OH)2:
Полученный NH3 также возвращают в производственный цикл.
Таким образом, единственным отходом производства является хлорид кальция.
Первый содовый завод такого типа в мире был открыт в 1863 в Бельгии; первый завод такого типа в России был основан в районе уральского города Березники фирмой «Любимов, Сольве и Ко» в 1883 году. Его производительность составляла 20 тысяч тонн соды в год. В 2010 году ФАС России отказала фирме Solvay в покупке этого завода, разрешив покупку группе Башкирская химия (ей также принадлежит завод Сода).
До сих пор этот способ остаётся основным способом получения соды во всех странах.
Способ Хоу
Разработан китайским химиком Хоу (Hou Debang) в 1930-х годах. Отличается от процесса Сольве тем, что не использует гидроксид кальция.
По способу Хоу в раствор хлорида натрия при температуре 40 градусов подается диоксид углерода и аммиак. Менее растворимый гидрокарбонат натрия в ходе реакции выпадает в осадок (как и в методе Сольве). Затем раствор охлаждают до 10 градусов. При этом выпадает в осадок хлорид аммония, а раствор используют повторно для производства следующих порций соды.
Сравнение способов
По методу Хоу в качестве побочного продукта образуется NH4Cl вместо CaCl2 по методу Сольве.
Способ Сольве был разработан до появления процесса Габера, в то время аммиак был в дефиците, поэтому регенерировать его из NH4Cl было необходимо. Метод Хоу появился позже, необходимость регенерации аммиака уже не стояла так остро, соответственно, аммиак можно было не извлекать, а использовать его как азотное удобрение в виде соединения NH4Cl.
Тем не менее NH4Cl содержит хлор, избыток которого вреден для многих растений, поэтому использование NH4Cl в качестве удобрения ограничено. В свою очередь рис хорошо переносит избыток хлора, и в Китае, где применяется NH4Cl для рисоводства, метод Хоу, дающий NH4Cl в качестве побочного продукта, более широко представлен по сравнению с другими регионами.
В настоящее время в ряде стран практически весь искусственно производящийся карбонат натрия вырабатывается по методу Сольве (включая метод Хоу как модификацию), а именно в Европе 94 % искусственно производимой соды, во всем мире — 84 % (2000 год).
Применение
Карбонат натрия используют в стекольном производстве; мыловарении и производстве стиральных и чистящих порошков; эмалей, для получения ультрамарина. Также он применяется для смягчения воды паровых котлов и вообще уменьшения жёсткости воды, для обезжиривания металлов и десульфатизации доменного чугуна. Карбонат натрия — исходный продукт для получения NaOH, Na2B4O7, Na2HPO4. Может использоваться в сигаретных фильтрах.
В пищевой промышленности карбонаты натрия зарегистрированы в качестве пищевой добавки E500, — регулятора кислотности, разрыхлителя, препятствующего комкованию и слёживанию. Карбонат натрия (кальцинированная сода, Na2CO3) имеет код 500i, гидрокарбонат натрия (пищевая сода, NaHCO3) — 500ii, их смесь — 500iii.
Одна из новейших технологий повышения нефтеотдачи пластов — АСП заводнение, в котором применяется сода в сочетании с ПАВ для снижения межфазного натяжения между водой и нефтью.
В фотографии используется в составе проявителей как ускоряющее средство.
Самостоятельно добавляется в моторное масло для предотвращения полимеризации. Концентрация 2 г на 1 л масла.
Безопасность
Тривиальные названия
Сода — общее название технических натриевых солей угольной кислоты.
«Сода» в европейских языках происходит, вероятно, от арабского «suwwad» — общего названия различных видов солянок, растений, из золы которых её добывали в средние века; существуют и другие версии. Кальцинированная сода (карбонат натрия) называется так потому, что для получения её из бикарбоната последний «кальцинируют» (лат. calcinatio, от calx, по сходству с процессом обжига извести), то есть прокаливают.