Реактив голубева что это
Юный техник 1961-02, страница 34
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ГУМУСА (ПЕРЕГНОЯ)
Для этого анализа понадобится реактив 0,2-нормальная хромовая смесь. 19,6 г К0Сг907 (двухромовокислый калий) растирают в ступке и растворяют в 1 л дистиллированной воды. В раствор осторожно, небольшими порциями доливается 1 л крепкой серной кислоты (H2SOj), с удельным весом 1,84
Из высушенной пробы почвы тщательно отбирают корешки растений, семена и другие органические остатки. Почва тщательно растирается в ступке и просеивается через сито с диаметром отверстий 0,25 мм. Навеска берется чроизвольной: для черноземов — от 0,05 до 0.3 г, а для дерново-подзолистых почв — до 1 г* Почву высыпают в колбочку и вне зависимости от навески приливают 10 мл 0,2-нормальной хромовой смеси. Колбочку закрывают воронкой и раствор кипятят в течение 5 минут. Кипение должно быть слабым и равномерным
После кипячения раствору дают отстояться в течение 2—3 часов, чтобы осела муть. Затем раствор осторожно, стараясь не замутить, выливают в кюветку и сравнивают с цветной шкалой диска.
Шкала составлена из расчета на 0,1 г почвы. Навеска была произвольной: необходим пересчет Если, например, было взято 0,3 г почвы, то полученный по шкале процент гумуса нужно разделить на 3(0,3: : 0,1=3), если 0,05 то на 0,5 (0,05:0,1=0,5) и т. д. Прн навеске в 0,1 г цифры, показывающие процент содержания гумуса, берутся прямо с диска.
Следует помнить, что при производстве анализов реактивы набираются т олько пипеткой с резиновой грушей или из бюретки. Работа с реактивами требует тщательности и осторожности. Проводить ее нужно в химическом кабинете, под руководством учителя химии.
Универсальный индикатор (реактив Голубева) и другие реактивы отпускаются Загорским заводом чистых солей (г Загорск Московской области), а также продаются в магазинах, торгующих химреак-
ПРИСПОСОБЛЕНИЕ ДЛЯ КРАНА
рели к водопроводному кра-ну прикрепить крюк из толстой проволоки, то можно налить воду в кастрюлю, держа ее одной рукой. При помощи такого приспособления нетрудно держать даже тяжелую кастрюлю.
Реактивы для золота
При определении золота 583-й и 585-й проб реактив хлорное золото более точен в сравнении с кислотным, и несмотря на узкую его направленность (опробование 583-й и 585-й проб) диапазон действия реактива достаточно велик. При навыке этим реактивом можно определять золотые сплавы от нижнего предела до 600-й пробы, определяя пробу по цвету и интенсивности окисления на золоте. Зная характер окисления, можно отличать и серебро от других белых металлов; Действие данного реактива на разные по пробам сплавы различно.
На золотые сплавы от «чистоты» до 585-й пробы реактив не действует; на сплавах 583-й пробы оставляет легкую тень; 500-й пробы — светло-коричневый оттенок; 375-й пробы — темный каштановый осадок.
Чем ниже проба, тем темнее и непрозрачнее осадок, переходящий из каштанового в черный.
Серебро, реагируя с хлорным золотом, оставляет темное пятно с зеленым оттенком.
Реактив хлорное золото не действует на платину, металлы платиновой группы и некоторые нержавеющие стали.
Универсальным реактивом для золотых сплавов можно считать также кислотный на 500-ю пробу золота. Это чистая азотная кислота, которая реагирует на все золотые сплавы ниже 583-й пробы. Реактив наиболее дешевый и доступный. На золотых сплавах ниже 500-й пробы металл под каплей реактива начинает выделять пузырьки. Чем ниже проба, тем интенсивнее выделение. На металлах, не содержащих золота, реакция мгновенная с выделением зеленой пены и шипением. На серебре от «чистоты» до 800-й пробы азотная кислота оставляет серовато-белое матовое пятно, с понижением пробы серебро под каплей реактива заметно выделяет пузырьки, ниже 600-й пробы — кипит. Реактив рекомендуется как начальный при неизвестном испытуемом материале.
Реактивы для серебра
Для серебра в основном используют два типа реактивов — азотнокислое серебро и хромпик. Азотнокислое серебро представляет собой водный раствор соли азотнокислого серебра в различных концентрациях.
Под действием данных реактивов на серебре, соответствующим реактиву, образуется слабый серовато-белый налет. На серебре низшей пробы относительно реактива интенсивность пятен возрастает. На изделиях высшей пробы относительно реактива пятна не образуется. При ослаблении действия реактива но его усилить добавлением капли азотной кислоты. Реактив хромпик — это водный раствор соли двухромовокислотного калия с добавлением серной кислоты. Несмотря на то что хромпик в сравнении с азотнокислым серебром дает менее точный диагноз, применяется он чаще. Приблизительный процент содержания серебра в сплаве хромпиком можно определить в интервале от «чистоты» до 600-й пробы. А в сочетании с другими реактивами можно определить серебряный сплав даже ниже пробы.
Под действием хромпика серебро 600-й пробы оставляет темный буро-красный осадок. Яркость пятна возрастает с повышением пробы. В пределах 780…820-й проб бурые оттенки исчезают, переходя в оранжевый цвет. С повышением пробы краснота возрастает, серебро 875-й пробы реагирует красным цветом. Яркость красного цвета возрастает, переходя в «кровавый» выше 900-й пробы. С понижением пробы ниже 600-й реакция прекращается, однако, если предварительно опробовать сплав азотной кислотой (реактив 500-й пробы для золота), на этом месте хромпик даст Красную реакцию серебра. При определенном навыке хромпиком можно опробовать серебряные сплавы с точностью до 20 единиц.
Химические реактивы. Понятия и классификация
Химические реактивы – это вещества, которые используются в химических и медицинских лабораториях для анализа веществ, приготовления растворов, проведения реакции, изготовлении красителей, моющих средств, ароматизаторов и т.п. Реактивы делятся на несколько основных видов:
Органические реагенты бывают трех видов: растворители; кислоты; соли и соединения. Чаще всего они используются для титриметрии, люминесцентного анализа, фотометрии и др. Преимуществом данных реактивов, пожалуй, является их высокая чувствительность и избирательность, благодаря которым можно использовать определенный реагент для определения какого-то одного иона даже в присутствии мешающих ионов.
Неорганические реагенты – это соли, кислоты, оксиды, гидроксиды, металлы и неметаллы. Реактив Несслера также является неорганическим веществом.
Аналитические реактивы используют для приготовления некоторых растворов и проведения аналитических опытов в учебных и научно-исследовательских заведениях.
Растворители в свою очередь тоже делятся на органические и неорганические. Они могут быть как одним веществом, так и смесью из двух, трех и т.д.
Индикаторы подразделяются на 4 группы: металлоиндикаторы; редокс-индикаторы; кислотно-основные и адсорбционные индикаторы. Меняя цвет раствора, в который их добавляют, они показывают, какая реакция произошла в растворе и какие ионы там присутствуют. Индикаторы по-разному проявляют себя в разных pH и при образовании комплексов, осадков и других соединений.
Практически все вещества в природе имеют в себе примеси. На заводе по производству реактивов, прежде чем получить нужное вещество, оно проходит множество этапов обработки. В связи с этим полученный реактив не всегда получается чистым и имеет до 5% примесей. По степени чистоты все химические реактивы классифицируются на 5 групп:
Помимо общепринятых сокращений, на банках с веществами ставятся метки – цветные полосы, которые помогают быстро сориентироваться, какой чистоты это вещество. Технические реактивы – это реактивы, содержащие в себе около 5% примесей и только 95% основного вещества. Эта квалификация считается самой низшей. На упаковке метка обозначается коричневым цветом.
Чистые реактивы содержат в себе от 98% основного вещества. Полоса на упаковке обозначается зеленым цветом.
Чистый для анализа реактив должен содержать в себе много больше 98% основного компонента и минимальное количество примесей. Цвет для такого реактива – синий.
Химически чистые реактивы являются высшей степенью чистоты реактива с содержанием в себе 99 и более процентов. Цвет – красный.
Примеси в растворах мешают проведению анализа, приготовлению растворов и т.д. Чем их больше, тем менее точным получится результат проделанного опыта. Особо чистые реактивы содержат настолько малую долю примеси, что ошибки такого рода практически сводятся к нулю.
ГСО и Стандарт-титры
ГСО – это некий образец вещества, либо материала, по химическому составу и физическим свойствам который схож с какой-то группой веществ или материалов и прошедший метрологическую аттестацию. Государственный стандартный образец нужен для метрологического анализа объектов окружающей среды, химической и нефтяной продукции.

Все химические реактивы по степени опасности согласно СанПиН и ГОСТу делятся на классы:
Приготовление растворов
Все вещества обладают таким свойством, как растворимость. Растворимость вещества выражается в граммах вещества на 100 граммов раствора (растворителя) – сколько граммов растворенного вещества содержится в 100 граммах раствора (растворителя).
Для приготовления раствора заданной концентрации необходимо пипеткой перенести нужный объем вещества в мерную колбу заданного объема и довести до метки дистиллированной водой. Для расчёта можно воспользоваться формулой C1V1=C2V2, где C1 – концентрация исходного раствора, а V1 – его объем; C2 – необходимая концентрация, а V2 – неизвестное, т.е. тот объем, который нужно найти для конечного раствора: V2= C1V1/ C2. Самое важное правильно при разбавлении концентрированных кислот – нужно добавлять кислоту в воду, а не наоборот: это чревато такими последствиями, как разбрызгивание кислоты и попадание ее на кожу и одежду. Это правило необходимо знать не только химикам, но и домашним хозяйкам, которые в быту пользуются разбавлением кислот, например, уксусной.
Хранение реактивов

Реактивы, которые нельзя хранить в стеклянных тарах (например, плавиковая кислота и щелочи), должны хранится в пластиковых бутылях.
Вещества, которые разлагаются или меняют свои свойства под действием света, хранятся в темных или желтых стеклянных тарах.
Некоторые реактивы нуждаются в герметичном хранении, добиться этого можно с помощью промазывания пробок парафином. На каждой таре необходимо указывать название, концентрацию и срок годности данного реактива. Сливать отработанные реактивы нужно в специально отведенные для этого склянки для последующей переработки или утилизации.
Химические лаборатории должны быть оборудованы специальными вытяжными и обычными шкафами для хранения, а также хорошо вентилируемыми помещениями, в которых непосредственно хранятся все реактивы.
Реактив Грисса для определения нитритов и нитрит-ионов
Реактивом Грисса называют раствор сульфаниловой кислоты и альфа-нафтиламина 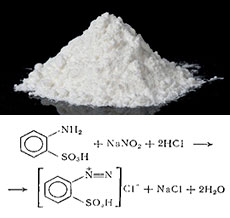
Помимо указанного выше применения в фотометрии, этот хим реактив используется в аналитической химии, в сельском хозяйстве, для определения качества воды, в том числе грунтовой, питьевой и бытовой. Определение азотосодержащих соединений в воде и почве имеет огромное хозяйственное значение, так как азот важен для жизнедеятельности живых организмов, особенно растений. Недостаток азота в воде или почве может вызвать прекращение роста растений, а его переизбыток приводит к ухудшению качества воды и условий для микроорганизмов и флоры.
Российский ГОСТ нормирует содержание нитритов в почвах и природных водах. Чувствительность определения количества нитритов методом Грисса составляет 0,002 мг/л. Диапазон измерений — от 0,1 до 15 мкг.
Метод Грисса
Для определения нитритов в органических объектах по методу Грисса исследуют их водные вытяжки. Сначала биологический материал настаивают в воде, потом раствор фильтруют, удаляя взвешенные частицы. В случае необходимости применяют коагулянт, добиваясь, чтобы вытяжка стала прозрачной и бесцветной. В конце раствор пропускают через мембранный фильтр. Полученную вытяжку доводят до нейтральной реакции и подвергают воздействию реактива Грисса. Если в вытяжке присутствуют нитриты, то образуется азокраситель красного цвета. Чем окраска раствора интенсивнее, тем больше в нем нитритов.
Количественные характеристики определяются с помощью фотометра или спектрофотометра на длине волны 520 нм по отношению к смеси дистиллированной воды и реактива Грисса. Содержание нитритов в микрограммах вычисляют по калибровочному графику или по шкале стандартных растворов.
Приготовление реактива Грисса из порошка или жидких компонентов
Реактив Грисса выпускается в виде растворимого в воде порошка белого, серого или розоватого цвета. В герметичной таре, без доступа света соединение в сухой форме может храниться до 3-х лет. Для аналитических работ применяется 10-процентный раствор вещества в 12%-ной уксусной кислоте. Приготовленный раствор не должен иметь окраски и может храниться в холодильнике в герметично укупоренной посуде из темного стекла до двух суток.
Также Реактив Грисса может поставляться в виде двух составляющих: альфа-нафтиламина и сульфаниловой кислоты. Для приготовления собственно реактива отдельно готовят в 30%-ном растворе уксусной кислоты:
— 1-процентный раствор сульфаниловой кислоты и
— 0,1-процентный раствор альфа-нафтиламина.
Потом оба раствора смешивают в равных пропорциях. Готовое соединение должно быть бесцветным. Приготовленный этим способом реактив следует использовать в тот же день. Отдельные составные части хранятся дольше и их можно готовить заранее. Раствор альфа-нафтиламина нужно хранить в герметично закрытой склянке из темного стекла.
Приготовление раствора Грисса требует от лаборанта умения работы с опасными 
Реактив Грисса относится к веществам 2-3 класса опасности. Соединение токсично, при попадании на кожу и слизистые вызывает химический ожог. Готовить реактив, а также проводить с ним анализы разрешается в проветриваемом помещении с общей приточно-вытяжной и местной вентиляцией, с применением защитных средств: резиновых перчаток, спецодежды, противогазов или защитных очков и респираторов.
Помимо реактива Грисса в порошке, в химическом магазине «ПраймКемикалсГрупп» можно купить необходимые принадлежности для работы с ним: мембранные фильтры, посуду из темного стекла, средства защиты.
Краткий обзор по методикам анализа белка в пищевых продуктах
В данном обзоре кратко описаны основные методы определения белка в пищевых продуктах. Указаны основные преимущества и недостатки имеющихся в настоящее время методик и оборудования. Данные обзор может быть полезен для специалистов пищевой промышленности и аналитических лабораторий на производстве продуктов питания. Для простоты восприятия текста при написании обзора авторы сознательно использовали упрощенную лексику и терминологию в описании химических процессов и молекулярной структуры соединений.
1. Введение
Белки ( пептиды) представляют собой « полимеры» аминокислот. Белки состоят из двадцати различных аминокислот. Белки отличаются друг от друга в зависимости от типа, количества и последовательности аминокислот, составляющих основу полипептида. В результате они имеют разные молекулярные структуры и физико-химические свойства. Белки являются основными структурными компонентами многих натуральных продуктов, и зачастую определяют их общую текстуру, например, нежность мяса или рыбопродуктов. Изолированные белки часто добавляются в пищевые продукты в качестве ингредиентов, благодаря своим уникальным функциональным свойствам, их способностью обеспечить внешний вид, структуру или стабильность продукта. Белки нередко используются в процессах гелеобразования, как эмульгаторы, пенообразователи или загустители. Поэтому так важно иметь полную информацию о массовом содержании, типе, молекулярной структуре и функциональных свойствах белков входящих в состав пищевых продуктов.
2. Определение общей концентрации белка
2.1 Метод Кьельдаля
Метод Кьельдаля был разработан в 1883 году пивоваром Иоганном Кьельдалем. Сущность методики заключается в том, что образец продукта разлагается ( сжигается) серной кислотой в присутствии катализатора, после чего полученный после разложения связанный в виде сульфата аммония азот может быть определен подходящей методикой титрования. Количество белка рассчитывается в зависимости от концентрации азота в продукте. В таком виде метод все еще используется и сегодня, хотя существует ряд усовершенствований для ускорения процесса и получения более точных данных. Данная методика считается арбитражным методом определения концентрации белка, например, в казеине. Поскольку метод Кьельдаля не измеряет содержание белка напрямую, необходим коэффициент преобразования ( К), для перерасчета измеренной концентрации азота в концентрацию белка. Коэффициент 6,25 ( что эквивалентно 0,16 г азота на грамм белка) используется для многих приложений, однако, это лишь среднее значение, и каждый белок имеет другой коэффициент преобразования в зависимости от его аминокислотного состава. Подробнее здесь
Метод Кьельдаля удобно разделить на три этапа: сжигание, нейтрализация и титрование.
Разложение. Образец анализируемой пробы взвешивается в специальную колбу, а затем разлагается при нагревании в присутствии серной кислоты ( окислитель), безводного сульфата натрия ( для ускорения реакции за счет повышения температуры кипения) и катализаторов, таких как медь, селен, титан, или ртуть. При разложении любого азота в продукте ( кроме азота, который находится в виде нитратов или нитритов) образуется аммиак, который в растворе сильной серной связывается в ион аммония ( NH 4 + ) и, следовательно, остается в растворе. Общий вид реакции будет следующим:
N ( food) ® ( NH 4) 2 SO 4 ( 1) N ( белков анализируемого продукта) ® ( NH 4) 2 SO 4 ( 1)
Нейтрализация. После разложения содержимое колбы количественно переносят в специальную пробирку для отгонки, добавляют щелочь и отгоняют выделяющийся аммиак. Наиболее полно и гладко этот процесс проходит при использовании метода перегонки с паром. Общий вид реакции будет следующим:
Газообразный аммиак, улавливается в отдельной колбе с избытком раствора бороной кислоты. Низкий рН раствора в колбе способствует переходу газообразного аммиака в ион аммония, и одновременно преобразует борную кислоту в борат ион: Общий вид реакции будет следующим:
Концентрации ионов водорода ( в молях), необходимое для достижения точки эквивалентности соответствует концентрации азота, в первоначальном образце ( уравнение 3). Уравнение ( 5) может быть использовано для определения концентрации азота в образце, который весит м граммов и для титрования которого потрачено х М соляной кислоты:
Где V S и V b объемы тирующей кислоты для образца и холостого опыта, 14g — молекулярная масса азота. Холостую пробу, как правило, используют, если требуется принять во внимание остаточный азот, который может содержаться в реагентах, используемых при проведении анализа. Как только содержание азота определено, можно рассчитать содержание белка с использованием соответствующего коэффициента преобразования:
Массовая доля белка = К * % N.
2.3. Преимущества и недостатки
Метод Кьельдаля широко используется в мире и до сих пор наравне со всеми другими методами. Его универсальность, высокая точность и хорошая воспроизводимость сделали его основным методом для оценки содержания белка в пищевых продуктах. Однако этот метод не отражает меру истинного белка, а определяет только общее содержание азота в образце, не выделяя небелковый азот. При этом в ряде случаев неучитывание при расчетах содержания небелкового азота может привести к критичным ошибкам при определении собственно белка. Более того, для различных белков требуются различные коэффициенты преобразования, вследствие отличия в аминокислотных последовательностях. Даже для различных белков одного продукта ( например, молочных белков молока) коэффициент может отличаться значительно.
Использования концентрированной серной кислоты при высоких температурах также создает значительную опасность, как и использование некоторых дорогостоящих катализаторов. Кроме этого метод Кьельдаля трудоемок и требует значительного времени для его проведения. В настоящее время для снижения трудоемкости, времени и минимизации случайных ошибок разработаны системы различной степени автоматизации для выполнения всех описанных выше стадий анализа.
3. Метод Дюма
Разработанный и принятый не так давно метод Дюма предназначен для быстрого измерения концентрации белка в пробах продуктов питания. Этот метод впервые описан полтора века назад. Он начинает конкурировать с методом Кьельдаля как арбитражный метод анализа белков для некоторых продуктов питания в первую очередь из-за его оперативности.
Образец известной массы сжигается при высокой температуре ( около 900 ° С) в специальной ячейке в присутствии кислорода. Углекислый газ и вода удаляются путем пропускания газов через специальные колонки, которые поглощают их. Содержание азота измеряется путем передачи оставшегося после очистки газа на делительную колонку, на конце которой имеется детектор по теплопроводности. Дополнительно на колонке отделяется остаточной CO 2 и H 2 O. Прибор калибруется путем анализа материала, с известной концентрацией азота, например, ЭДТА ( содержание азота 9,59%). После этого, сигнал с детектора по теплопроводности может быть преобразован в содержание азота. Как и для метода Кьельдаля необходимо преобразовывать концентрацию азота в образце, используя подходящие коэффициенты пересчета, которые зависят от точной аминокислотной последовательности белка.
3.2. Преимущества и недостатки
Основное преимущество — это скорость анализа, ( по несколько минут на измерение, по сравнению с несколькими часами для Кьельдаля). Метод не требует токсичных химических веществ или катализаторов. Многие образцы могут быть измерены в автоматическом режиме. Метод прост в использовании.
Недостатки: Высокая начальная стоимость. Кроме того, метод также не дает меру истинного белка и для различных белков нужны различные поправочные коэффициенты. Небольшая масса и размер пробы затрудняет получение репрезентативной выборки.
4. Методы с использованием УФ-видимой спектроскопии
Для измерения концентрации белка существует ряд методов, основанных на УФ-видимой спектроскопии. Эти методы используют либо природные способности белков в поглощении ( или рассеянии) света в УФ-видимой области электромагнитного спектра, либо предусматривает химическую или физическую модификацию белков, чтобы перевести их в форму, поглощающую ( или рассеивающую) свет в этой области. Основные принципы любой из перечисленных ниже методик сходен. Прежде всего, при разработке методики следует выбрать химические группы, которые будут нести ответственность за поглощения или рассеяния излучения, например, пептидные связи, ароматические групп, основные группы для поглощения, для рассеивания — количество агрегированных белков. Далее создается градуировочная ( калибровочная) зависимость поглощения ( или мутности) от концентрации белка, для чего используются ряд белковых растворов с известной концентрацией. Абсорбцию ( или мутность) анализируемой затем пробы определяется по построенной градуировочной зависимости.
Наиболее часто используемые УФ-методики для определения содержания белка в продуктах приводятся ниже:
Прямые измерения при 280 нм. Триптофан и тирозин интенсивно поглощает ультрафиолетовый свет при 280 нм. Во многих белках содержание триптофана и тирозина, остается практически неизменным, так что их поглощения при 280 нм может быть использован для определения их концентрации. Преимущества этого метода в том, что процедура проста для выполнения, метод является неразрушающим, и никаких специальных реагентов не требуется. Основным недостатком является то, что нуклеиновые кислоты поглощают сильно при 280 нм и поэтому могут препятствовать измерению белка, если они присутствуют в достаточной концентрации. Для нивелирования этой проблемы были разработаны методы, в которых поглощение измеряется на двух различных длинах волн.
Биуретовый метод. При взаимодействии ионов меди ( Cu 2 +) с пептидными связями в щелочных условиях продукт дает интенсивную фиолетово-пурпурную окраску. Биуретовый реагент, в готовой форме может быть приобретен как готовый реактив в специализированных магазинах. Его смешивают с белковым раствором, а затем выдерживают в течение 15−30 минут и определяют поглощение при 540 нм. Основным преимуществом этого метода это отсутствие помех от других соединений, которые поглощают на более низких волнах, и сама техника менее чувствительны к типу белка, поскольку она использует поглощения с участием пептидных связей, которые являются общими для всех белков, а не с отдельными его группами. Однако, метод имеет относительно низкую чувствительность по сравнению с другими УФ методами.
Методы со связыванием красителя ( метод Брэдфорда) Сущность таких методов заключается в добавлении « отрицательно заряженного» красителя в раствор белка, рН которого регулируется так, чтобы белок находился в «положительно заряженной» области ( т.е. меньше изоэлектрической точки). При этом белки образуют нерастворимый комплекс с красителем из-за электростатического притяжения между молекулами, а несвязанного краситель остается в растворе. Отрицательно заряженная часть красителя связывается с катионными группами основных аминокислот ( гистидина, лизина и арганина) и любыми свободными аминогруппами. Количество несвязанного красителя, остающегося в растворе, после того как нерастворимый комплекс « белок-краситель» удаляется ( например, центрифугированием) определяется при измерении его поглощения на соответствующей длине волны. Количество белка, которое присутствовало в исходном растворе пропорционально количеству красителя, добавленному первоначально и оставшемуся в растворе. ( Для метода Бредфорда белки и их комплексы с красителем остаются в растворе, меняется интенсивность поглощения ( визуально цвет) на анализируемой длине волны).
Турбометрический метод ( рассеивание). Любые белковые молекулы, растворимые при обычных условия можно перевести в нерастворимую форму путем добавления определенных химических веществ, например, трихлоруксусной кислоты. Таким образом, концентрация белка может быть определено путем измерения степени мутности пропорциональной рассеиванию проходящего через раствор светового луча.
4.2. Преимущества и недостатки
Преимущества: УФ-видимой методы довольно быстро и просто выполнять, и они чувствительны к низкой концентрации белков.
Недостатки: Для большинства методов УФ-видимой спектроскопии необходимо использовать разбавленные и прозрачные растворы, которые не содержат загрязняющих веществ способных поглощать или рассеивать свет на выбранной для анализа длине волне. Необходимость прозрачного раствора означает, что большинство пищевых продуктов, должны пройти длительную пробоподготовку, прежде чем они будут пригодны для анализа, например, гомогенизация, экстракция, центрифугирование, фильтрация. Такая пробоподготовка может занять много времени и быть чрезвычайно трудоемкий. А иногда бывает невозможно количественно извлечь белки из определенных видов пищевых продуктов, особенно после того, как при обработке белки перешли в агрегированное состояние или образовали ковалентные связи с другими веществами. Кроме того, степень абсорбции зависит от типа анализируемого белка, которые могут отличаться в аминокислотных последовательностях.
5. Другие инструментальные методы
Существуют самые различные инструментальные методы для определения общего содержания белка в пищевых продуктах. Их можно разделить на три категории в соответствии с их физико-химическим принципом: ( 1) измерение объемных физических свойств, ( 2) измерения адсорбции излучения, и ( 3) измерение рассеяния излучения. Каждый инструментальных методов имеет свои преимущества и недостатки, и ассортимент объектов, на которые он может быть применен.
Измерение физических свойств. Плотность: плотность белка больше, чем у большинства других компонентов пищи, таким образом, увеличение плотности пищи, напрямую связано с увеличением содержания белка. Следовательно, содержание белка в продукте может быть соотнесено с его плотностью. Показатель преломления: показатель преломления водных растворов увеличивается при увеличении концентрация белка, следовательно, результаты измерения этого показателя могут быть использованы для определения содержания белка.
Измерение адсорбции УФ-видимый: концентрация белков может быть определено путем измерения поглощения УФ-видимого излучения ( подробнее описано выше).
ИК-ближняя и средняя область: Инфракрасные методы могут быть использованы для определения концентрации белков в пищевых продуктах. Белки поглощают в ИК-области за счет собственных молекулярных колебаний ( растяжения и изгиба) определенных химических групп вдоль полипептидной цепочки. Таким образом, измеряя поглощение излучения на определенных длинах волн, можно рассчитать количественную концентрацию белка в образце. Он также не требует особой подготовки образца и является неразрушающим методом контроля. Его основные недостатки — высокая начальная стоимость и необходимость проведения комплексной и сложной калибровки.
Измерение рассеяния излучения. Рассеяние света: Концентрация белковых агрегатов в водных растворах может быть определена с помощью методов измерения рассеяния света, поскольку мутность раствора прямо пропорциональна концентрации белка. Ультразвуковое рассеяния: концентрация белковых агрегатов также может быть определена с помощью ультразвуковых методов рассеяния, поскольку скорость ультразвука и его поглощения связанны с концентрацией белка в растворе.
5.2. Преимущества и недостатки
Основные преимущества и недостатки инструментальных методов упоминалось выше. Также следует отметить, для всех этих методов должна существовать калибровочная кривая, которая с большой долей вероятности будет различной для различных типов белков и пищевых матриц, в которых они содержится. Как следствие все инструментальные методы наиболее корректно работают для анализа пищевых продуктов с относительно простыми композициями. Для продуктов питания, которые содержат множество различных компонентов, концентрация которых может варьироваться, определить вклад белка на фоне других компонентов зачастую бывает затруднительно.
При анализе конкретного пищевого продукта обычно всегда возникает задача выбора конкретной методики для измерения концентрации белка в образце. Как решить, какой метод является наиболее подходящим? Первое, с чем нужно определиться это для каких целей будет проводиться анализ. Если анализ будет проводиться для сторонних организаций, с целью проведения сличений, или же для расчета за товар, следует пользоваться официально признанным арбитражным методом. Так Кьельдаль, и все чаще метод Дюма, были официально утверждены для широкого спектра пищевой промышленности. В противоположность этому, только небольшое число методом УФ спектроскопии были признаны официально. Но к примеру, для молока все чаще используется метод Брэдфорда, поскольку определение белка без одновременного определения и учета небелкового азота в молоке может привести к завышенным результатом с неприемлемой ошибкой.
Для целей контроля качества, часто более полезно иметь быстрый и простой метод измерения содержания белка и, следовательно, методы ИК-спектроскопии являются наиболее подходящими. В лабораториях где проводятся фундаментальные исследования, и где обычно работы выдуться с уже выделенными и очищенными образцами, методы с использованием УФ спектроскопии зачастую предпочтительнее, поскольку они дают быстрые и надежные измерения, и чувствительны к крайне низкой ( до 0,001% масс.) концентрации белка.
Также следует учитывать и другие факторы, которые, возможно, придется рассматривать. В основном это:
Методы Кьельдаля, Дюма, акустические и ИК методы, как правило, не требует специальной пробоподготовки, либо пробопоготовка автоматизирована в соответствующем блоке прибора. Во многих случаях после репрезентативной выборки объект анализируется непосредственно. В противоположность, различные методы УФ спектроскопии, как указано выше, требуют серьезной подготовки образца перед анализом. Белок должен быть сепарирован от образца, что обычно означает различные процедуры гомогенизации, экстракции, фильтрации и центрифугирования. Время, необходимое на анализ, и количество образцов, которые могут быть проанализирован одновременно, также являются важными факторами, которые следует учитывать при определении того, какая методика будет выбрана для анализа.
Другие заслуживающие упоминания факторы — это время амортизации оборудования, его начальная стоимость, наличие или отсутствие требуемого вспомогательного оборудования, стоимость расходных материалов и сроком их годности.
7. Цена вопроса
В заключении приведем ориентировочную стоимость постановки методики [1] :





