Кислота вода что получится
Химические свойства кислот
8 класс, 9 класс, ЕГЭ/ОГЭ
Кислоты — это сложные химические вещества, состоящие из одного или нескольких атомов водорода, способных замещаться атомами металла, и кислотных остатков.
Рассмотрим подробнее общие свойства кислот.
Диссоциация
Кислоты — это электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка. Диссоциация кислот происходит ступенчато. По способности к диссоциации кислоты разделяют на две группы:
Хорошо диссоциирующие (сильные): H2SO4, HCl, HBr, HNO3, HClO4, HI.
Разложение
В результате реакций разложения кислородсодержащих кислот образуются кислотный оксид и вода. Бескислородные кислоты образуют простые вещества. Для разложения некоторых кислот необходимо нагревание или излучение (HCl, HNO3, H3PO4) другие же разлагаются самопроизвольно в момент образования (H2CO3, H2SO3, HNO2).
Взаимодействие кислот с металлами
Металл может вытеснять водород из кислоты только в том случае, если металл стоит левее водорода в ряду активности металлов. Продукты реакции — соль и водород.
При взаимодействии с кислотами-окислителями, например, азотной, образуется продукт восстановления кислоты, хотя протекание реакции также неоднозначно.
Высокая окислительная способность серной и азотной кислот позволяет им вступать в реакции с металлами. Продукты реакции будут зависеть от активности металла и от концентрации кислот.
Таблица: химические свойства кислот-окислителей
На холоду — пассивация
На холоду — пассивация
Реакция не проходит
На холоду — пассивация
На холоду — пассивация
Взаимодействие кислот с основаниями
Кислоты реагируют с основаниями и амфотерными гидроксидами, в результате образуются соль и вода. Взаимодействие кислот с основаниями называют реакцией нейтрализации.
NaOH + HCl = NaCl + H2O
Взаимодействие кислот с солями
Сильные кислоты вытесняют слабые из растворов их солей, при этом образуются новая соль и новая кислота. Условие протекания реакции кислот с солями — одним из продуктов реакции должны быть нерастворимая соль или слабая кислота, вода, газ.
Взаимодействие кислот с основными и амфотерными оксидами
Кислоты вступают в реакцию с основными и амфотерными оксидами (последние ведут себя как основные оксиды). В результате реакции образуется соль и вода.
Восстановительные свойства бескислородных кислот
Бескислородные кислоты (кроме HF) проявляют восстановительные свойства за счет химического элемента, который входит в состав аниона, при действии на них различных окислителей.
Например, в качестве окислителей для всех галогеноводородных кислот выступают диоксид марганца MnO2, перманганат калия KMnO4, дихромат калия K2Cr2O7.
Результат этих реакций — образование свободных галогенов.
Из галогеноводородных кислот наибольшая восстановительная активность — у йодоводородной. Ее могут окислять оксид железа (III) и соль трехвалентного железа.
Высокая восстановительная активность характерна для сероводородной кислоты, она может быть окислена диоксидом серы.
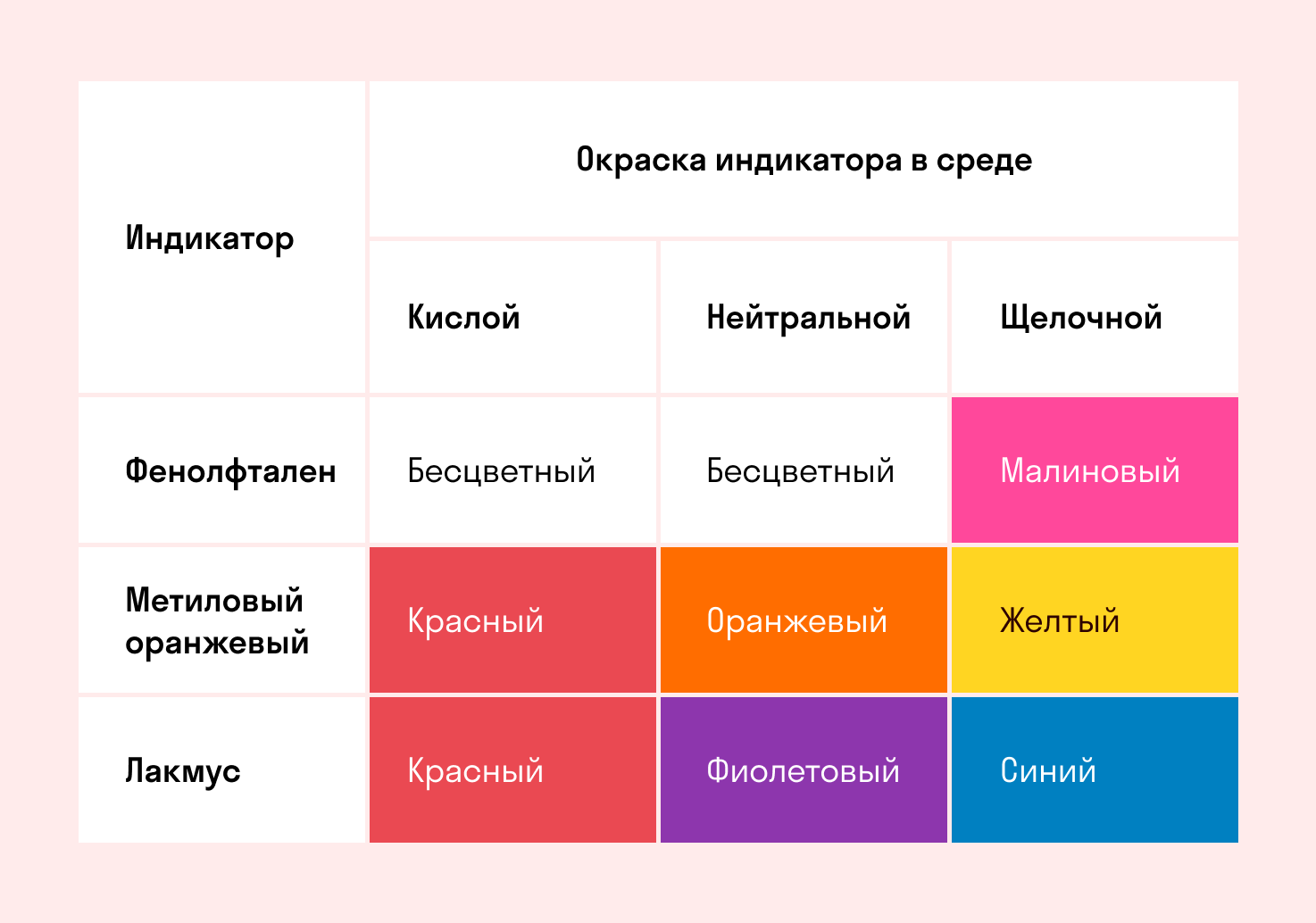
Способность окрашивать индикаторы
Индикаторы кислот — это специальные вещества, при помощи которых определяют наличие кислот в растворе.
Вопросы для самоконтроля
С чем реагируют кислоты?
При каких условиях кислоты взаимодействуют с солями? Приведите пример.
Составьте уравнения реакций и назовите продукты реакций:
Разбавленный раствор серной кислоты реагирует с: медью, хлоридом меди, сульфатом меди, цинком?
Соляная кислота вступает в реакцию с каждым из двух веществ:
Кислота вода что получится
Вот мне интересно, когда люди перестанут задавать очевидные вопросы?
Тавитима, вы а Гугле посмотрите отвтеты на эти ворпосы. Думаю, вас это не оставит равнодушной
дай бог памяти. скорее в воду. меньше выброс энергии будет. кажись. а воообще нужно сына спросить он это отлично знает
Нужно наливать серную кислоту в воду тогда все будет ОК.
А если наоборот. то как минимум разорвет сосуд.
У меня за плечами 12 лет работы в хим.лаборатории и все эти годы у нас висел плакат: Не лей воду в кислоту!
А у нас метель! Скоро гулять с собакой, караул!
Собака, это такое дело.
Ну да, ныть можно сколько угодно, а гулять придется.
Другими словами, всякая собака, в любую погоду хозяина на улицу выведет.
Запомните, мы сахар насыпаем в воду (чай), так и серная кислота или любая другая наливается в воду.
кислота. она тяжелее воды. если лить наоборот, вода будет расплёскиваться по поверхности кислоты.
Кислоту льют в воду, никак не наоборот))) Так концентрация кислоты уменьшается с малого объёма.
На уроках химии учили лить воду в кислоту, дабы избежать бурной реакции, насколько я помню.
Давно это было. забылось.
из курса химии знаю что серную кислоту надо лить в воду а не наоборот так что вы правы
Вопрос электромонтеру на засыпку. Если линуть воду в кислоту, можно получить травму.
Кислота в воду,потому,что она тяжелее,а вода легче и будет кипеть и разбрызгиваться
не темните. как спирт надо разбавить что ли..так и скажите! (шутка!)
Да. Чтобы концентрация повышалась постепенно. Иначе возможны брызги, обожгешься
Не думайте об этом, лучше загляните на наши платья они тут http://flfashion.com.ua/
Кислота на них не действует?
Давайте проверим. Выбирите одно тут http://flfashion.com.ua/
кислоту в воду т. к плотность воды меньше и вода может сильно нагреться
Что твердили это да а вот почему?кислота получается спокойно ныряет вглубь воды и растворяется а если на оборот вода на остаетчся на уровне кислоты и по границе может вскипеть. да?
Кислоты. Химические свойства и способы получения
Перед изучением этого раздела рекомендую прочитать следующую статью:
Кислоты – сложные вещества, которые при взаимодействии с водой образуют в качестве катионов только ионы Н + (или Н3О + ).
Получение кислот
1. Взаимодействие кислотных оксидов с водой. При этом с водой реагируют при обычных условиях только те оксиды, которым соответствует кислородсодержащая растворимая кислота.
кислотный оксид + вода = кислота
При этом оксид кремния (IV) с водой не реагирует:
2. Взаимодействие неметаллов с водородом. Таким образом получают только бескислородные кислоты.
Неметалл + водород = бескислородная кислота
H2 0 + Cl2 0 → 2 H + Cl —
3. Электролиз растворов солей. Как правило, для получения кислот электролизу подвергают растворы солей, образованных кислотным остатком кислородсодержащих кислот. Более подробно этот вопрос рассмотрен в статье Электролиз.
4. Кислоты образуются при взаимодействии других кислот с солями. При этом более сильная кислота вытесняет менее сильную.
Например: карбонат кальция CaCO3 (нерастворимая соль угольной кислоты) может реагировать с более сильной серной кислотой.
5. Кислоты можно получить окислением оксидов, других кислот и неметаллов в водном растворе кислородом или другими окислителями.
Химические свойства кислот
1. В водных растворах кислоты диссоциируют на катионы водорода Н + и анионы кислотных остатков. При этом сильные кислоты диссоциируют почти полностью, а слабые кислоты диссоциируют частично.
HCl → H + + Cl –
Если говорить точнее, происходит протолиз воды, и в растворе образуются ионы гидроксония:
HCl + H2O → H3O + + Cl –
Многоосновные кислоты диссоциируют cтупенчато.
HSO3 – ↔ H + + SO3 2–
2. Кислоты изменяют окраску индикатора. Водный раствор кислот окрашивает лакмус в красный цвет, метилоранж в красный цвет. Фенолфталеин не изменяет окраску в присутствии кислот.
С нерастворимыми основаниями и соответствующими им оксидами взаимодействуют только растворимые кислоты.
нерастворимое основание + растворимая кислота = соль + вода
основный оксид + растворимая кислота = соль + вода
При этом гидроксид меди (II) не взаимодействует с нерастворимой кремниевой кислотой.
С сильными основаниями (щелочами) и соответствующими им оксидами реагируют любые кислотами.
щёлочь(избыток)+ кислота = средняя соль + вода
щёлочь + многоосновная кислота(избыток) = кислая соль + вода
При этом дигидрофосфаты образуются в избытке кислоты, либо при мольном соотношении (соотношении количеств веществ) реагентов 1:1.
При мольном соотношении количества щелочи и кислоты 1:2 образуются гидрофосфаты:
В избытке щелочи, либо при мольном соотношении количества щелочи и кислоты 3:1 образуется фосфат щелочного металла.
4. Растворимые кислоты взаимодействуют с амфотерными оксидами и гидроксидами.
Растворимая кислота + амфотерный оксид = соль + вода
Растворимая кислота + амфотерный гидроксид = соль + вода
5. Некоторые кислоты являются сильными восстановителями. Восстановителями являются кислоты, образованные неметаллами в минимальной или промежуточной степени окисления, которые могут повысить свою степень окисления (йодоводород HI, сернистая кислота H2SO3 и др.).
4H I — + 2 Cu +2 Cl2 → 4HCl + 2 Cu + I + I2 0
6. Кислоты взаимодействуют с солями.
Кислота1 + растворимая соль1 = соль2 + кислота2/оксид + вода
Ag + NO3 — + H + Cl — → Ag + Cl — ↓ + H + NO3 —
7. Кислоты взаимодействуют с кислыми и основными солями. При этом более сильные кислоты вытесняют менее сильные из кислых солей. Либо кислые соли реагируют с кислотами с образованием более кислых солей.
кислая соль1 + кислота1 = средняя соль2 + кислота2/оксид + вода
KHCO3 + HCl → KCl + CO2 + H2O
Ещё пример : гидрофосфат калия взаимодействует с фосфорной кислотой с образованием дигидрофосфата калия:
При взаимодействии основных солей с кислотами образуются средние соли. Более сильные кислоты также вытесняют менее сильные из солей.
Основные соли могут взаимодействовать с собственными кислотами. При этом вытеснения кислоты из соли не происходит, а просто образуются более средние соли.
Al (OH) Cl2 + HCl → AlCl3 + H2O
8. Кислоты взаимодействуют с металлами.
При этом протекает окислительно-восстановительная реакция. Однако минеральные кислоты и кислоты-окислители взаимодействуют по-разному.
К минеральным кислотам относятся соляная кислота HCl, разбавленная серная кислота H2SO4, фосфорная кислота H3PO4, плавиковая кислота HF, бромоводородная HBr и йодоводородная кислоты HI.
Такие кислоты взаимодействуют только с металлами, расположенными в ряду активности до водорода:
При взаимодействии минеральных кислот с металлами образуются соль и водород:
минеральная кислота + металл = соль + H2↑
Fe + 2 H + Cl → Fe +2 Cl2 + H2 0
Сероводородная кислота H2S, угольная H2CO3, сернистая H2SO3 и кремниевая H2SiO3 с металлами не взаимодействуют.
Кислоты-окислители (азотная кислота HNO3 любой концентрации и серная концентрированная кислота H2SO4(конц)) при взаимодействии с металлами водород не образуют, т.к. окислителем выступает не водород, а азот или сера. Продукты восстановления азотной или серной кислот бывают различными. Определять их лучше по специальным правилам. Эти правила подробно разобраны в статье Окислительно-восстановительные реакции. Я настоятельно рекомендую выучить их наизусть.
9. Некоторые кислоты разлагаются при нагревании.
Угольная H2CO3, сернистая H2SO3 и азотистая HNO2 кислоты разлагаются самопроизвольно, без нагревания:
Кремниевая H2SiO3, йодоводородная HI кислоты разлагаются при нагревании:
Азотная кислота HNO3 разлагается при нагревании или на свету:
можно ли считать, что вода это кислота?
нет вода вообщето ш2о, а кислоты получаются на её основе
вода Н+ ОН-
одновременно и кислота и основание
потому и является таким хорошим растворителем (почти универсальным, чуть не дотянула)
вода является окислителем. вызывает корозии металов. а горячая вода быстро разъедает снег и лёд, однажды уничтожила мою любимую сосулю.
Одно и то же вещество в зависимости от условий взаимодействия может быть как кислотой, так и основанием (амфотерность).
считай, никто не запрещает, но одновременно она является и основанием.
вода является кислотой т. к. она реагирует с щёлочами как Li Na u K. Происходит тот же эфект как и с кислотой. Сами рассудите SH2, HCl, CH3 являются кислотами. Почему же вы считаете, что вода это
не кислота.
Кислота вода что получится
Не вздумайте при смешивании кислоты и воды, добавить воду в кислоту. Вода моментально вскипит и скорее всего выплеснется вам в лицо.
А оно вам нужно?
Только кислоту в воду! И потихоньку!
Следует заметить, что совет актуален для всех сильных кислот
Если Вы льете, например, воду в кислоту, то сразу пойдет химическая реакция с выделением тепла и поскольку удельный вес воды легче кислоты, то жидкости не будут перемешиваться и вода может закипеть с разбрызгиванием капель и попасть в глаза.
при растворении кистотыв воде происходит выделение тепла. Если в кислоту влить воду, то вероятность того, что эта вода закипит и вместе с кислотой выльется из пробирки очень высока. Поэтому в целях безопасности кислоту вливают в воду.
Кислоту в воду, потому что брызг будет меньше, а если, наоборот, то реакция идет с большим выделением тепла, брызг больше, и можно получить химический ожог. Помню со школы. Я даже задачки попроще могу решить при наличии учебника
Кислоту льют в воду.
Нарушение этого правила например, в случае с серной кислотой приводит к закипанию воды и выплескиванию горячего сернокислого раствора. Могут пострадать глаза, лицо, руки.
если вливать воду в серную кислоту, то вода закипит в процессе вливания и начнет разбрызгиваться.
Кислоту в воду.Чтобы реакция бурно не пошла с выделением теплоты и брызги кислоты не полетели.
По-моему воду в кислоту, но точно утверждать не буду. Чтобы реакция не шла слишком бурно.
Ну уж химию чуть-чуть знаю. Конечно, кислоту в воду. Тепловой эффект опасен АДНАКО.
Вспомни химию,какая реакция будет при соединении кислоты с водой.
Всё зависит от того, что тяжелее. Более лёгкое в более тяжёлое
я воду в кислоту уксусную. с химией не дружу пояснить не могу.
за свой ответ, я бы хотела, как минимум, нобелевскую премию)))
Смотря какая кислота?Но реакция произойдёт в любом случае.
если память не изменяет воду в кислоту, а то будут брызги